Array
(
[NAME] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[~NAME] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[PREVIEW_PICTURE] => Array
(
[ID] => 6113
[TIMESTAMP_X] => 12.05.2025 12:05:49
[MODULE_ID] => iblock
[HEIGHT] => 750
[WIDTH] => 1000
[FILE_SIZE] => 515585
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/02d/dd6y00xg7r54b34kwprbotancagip70s
[FILE_NAME] => 3258.jpg
[ORIGINAL_NAME] => 3258.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => ebcc3fa8cb4c58a890ccc140dd3821b4
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/02d/dd6y00xg7r54b34kwprbotancagip70s/3258.jpg
[UNSAFE_SRC] => /upload/iblock/02d/dd6y00xg7r54b34kwprbotancagip70s/3258.jpg
[SAFE_SRC] => /upload/iblock/02d/dd6y00xg7r54b34kwprbotancagip70s/3258.jpg
[ALT] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[TITLE] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
)
[~PREVIEW_PICTURE] => 6113
[DETAIL_TEXT] =>
SYSTEMATIC REVIEW
Amanda Y. Leong et al.
The association between pain, analgesia, and delirium among critically ill adults: a systematic review and meta-analysis
Intensive Care Med https://doi.org/10.1007/s00134-025-07784-6
Абстракт
Систематический обзор с мета-анализом, в котором изучали связь между болью или обезболивающими препаратами и возникновением, продолжительностью и тяжестью делирия.
Мы провели поиск в MEDLINE, EMBASE, CINAHL и Кокрановском центральном реестре контролируемых исследований с момента создания до 15 мая 2023 года. Мы включали рандомизированные или обсервационные исследования у взрослых в критическом состоянии, которые содержали данные о боли или воздействии анальгетиков, а также о наличии, продолжительности или тяжести делирия без языковых или региональных ограничений. IDPROSPERO: CRD42022367715. Два автора независимо друг от друга проверяли записи и извлекали данные. Риск необъективности оценивался с помощью Risk of Bias 2 или Risk of Bias In Non-randomized Studies of Interventions. Мы объединили данные с помощью модели случайных эффектов Hartung-Knapp Sidik-Jonkmann. Соблюдался стандарт PRISMA. Из 8 054 ссылок в систематический обзор было включено 90 исследований (119 230 пациентов), опубликованных в период с 2001 по 2023 год. 41 исследование было включено в первичный мета-анализ, изучающий распространенность делирия: семь исследований оценивали боль; 12 - фентанил; и пять - морфин. Наблюдалась тенденция к ассоциации между болью и возникновением делирия (ОР 2,49, 95% ДИ 0,98-6,30), а также значительная связь между болью и инцидентным делирием (ОР 3,70, 95% ДИ 1,73-7,93). Фентанил (ОР 2,49, 95% ДИ 1,45-4,27) и морфин (ОР 2,13, 95% ДИ 1,21-3,75) были связаны с возникновением делирия. Риск необъективности был критическим для многих исследований. Обнаружили ассоциацию между болью и возникновением делирия среди взрослых в критическом состоянии. Воздействие морфина или фентанила (но не других обезболивающих препаратов) было связано с повышенным риском возникновения делирия.
Ключевые слова: критическая медицина, анальгетики, боль, оценка боли, делирий
Введение
Боль - один из основных симптомов, с которым сталкиваются пациенты, находящиеся в критическом состоянии [1]. Последствия нелеченной боли включают посттравматическое стрессовое расстройство, депрессию и бессонницу [2]. Делирий - это острое состояние спутанности сознания, дефицита внимания и поведенческой дезорганизации [3]. Делирий часто встречается у больных в критическом состоянии и имеет последствия, включая увеличение продолжительности пребывания в отделении интенсивной терапии (ОРИТ) и когнитивные нарушения [1, 4-6]. Боль считается фактором риска развития делирия, однако данные, подтверждающие это мнение, ограничены [1, 7]. Симптомы делирия лечатся с помощью мультимодального подхода, который включает в себя обезболивание как ключевой принцип [1]. Однако препараты, используемые для лечения боли, связаны с нежелательными эффектами, включая дисфорию или галлюцинации, которые могут имитировать или способствовать развитию делирия [8].
Причинно-следственная связь между болью, обезболивающими препаратами и делирием неясна. Опиоиды, используемые для лечения боли, могут способствовать развитию делирия за счет изменения дофаминовой сигнализации [9, 10]. Duprey et al. сообщили, что на каждые 10 мг морфина вероятность развития делирия увеличивалась на 2,4 % [11]. Pandharipande et al. выявили, что у пациентов хирургических ОРИТ вероятность развития делирия была выше при воздействии фентанила, в то время как у пациентов с травмами вероятность развития делирия была ниже при использовании морфина [12]. В связи с неоднородностью данных о применении опиоидов и делирии неясно, связаны ли конкретные опиоиды или опиоиды как класс с наличием делирия. Для дальнейшего понимания взаимосвязи между болью и/или обезболивающими препаратами и делирием необходимо обобщить имеющуюся литературу. Это поможет врачам лучше понять, как оптимально управлять болью в контексте делирия, а ученым - узнать, на чем следует сосредоточить усилия по раскрытию взаимосвязи боли и делирия. Основной целью было изучить связь между болью (наличие и отсутствие) и делирием, а также между опиоидами (наличие и отсутствие) и делирием.
Методы
Данный систематический обзор и мета-анализ был представлен в соответствии с рекомендациями Preferred Reporting Items for Systematic Reviews and Meta-Analysis [13]. Протокол и поправки были представлены в Международный проспективный регистр систематических обзоров (PROSPERO ID: CRD42022367715) и ранее опубликованы [14].
Определение для факторов воздействия
Подробные определения приведены в онлайн-ресурсе 1. Вкратце, боль классифицировалась как отсутствие клинически значимой боли (цифровая шкала оценки 0-4, поведенческая шкала боли 3-4 или critical care pain observation tool (CPOT) 0-2) или как клинически значимая боль (цифровая шкала оценки ≥ 5, поведенческая шкала боли ≥ 5 или CPOT ≥ 3) [14]. Тяжесть боли определялась в соответствии с оценочным инструментом, использованным в опубликованном исследовании. Опиоиды классифицировались следующим образом: (1) фентанил; (2) морфин; (3) опиоиды, не указанные иначе; и (4) различные опиоиды, включая гидроморфон, метадон, меперидин и петидин. Классификация неопиоидов включала: (1) кетамин; (2) дексмедетомидин; (3) трамадол; (4) ацетаминофен; и (5) нестероидные противовоспалительные средства.
Определения исходов
Делирий определен как присутствующий или отсутствующий; наличие определялось в соответствии с опубликованными исследованиями. Чаще всего для определения делирияиспользовались confusion assessment method in ICU (CAM-ICU) или the intensive care delirium screening checklist (ICDSC). Степень тяжести делирия в данном исследовании указывалась только в том случае, если в исходном исследовании сообщалось об этом результате. Тяжесть определялась в соответствии с оценочным инструментом, использованным в исследовании. Встречаемость делирия определялась как количество всех случаев делирия (числитель) в исследуемой популяции (знаменатель) (подробные определения приведены Online Resource 1 и [14]). Заболеваемость делирием определялась как количество новых случаев делирия (числитель) в исследуемой популяции по отношению к численности исследуемой популяции- человек (знаменатель). Распространенность делирия определялась как количество случаев ранее существовавшего делирия, подсчитанное в исходный период времени исследования (числитель), по отношению к численности исследуемой популяции- человек (знаменатель).
Мы использовали показатель распространенности делирия в связи с неоднородностью исследований, в которых сообщалось о распространенности или заболеваемости делирием.
Стратегия поиска
Поиск проводился по четырем темам: (1) реанимация, (2) делирий, (3) боль и (4) обезболивающие препараты. Стратегия поиска была разработана при содействии медицинского библиотекаря и была рецензирована вторым медицинским библиотекарем с использованием методики Peer Review of Electronic Search Strategies. Поиск проводился в базах данных с момента создания до 15 мая 2023 г., включая: MEDLINE, EMBASE, Cumulative Index to Nursingand Allied Health Literature (CINAHL) и Кокрановский центральный регистр контролируемых исследований (CENTRAL). Авторы провели ручной поиск тезисов пяти крупных конференций по реаниматологии и делирию с января 2020 года по 15 мая 2023 года (подробная информация о конференциях доступна Online Resource 1). Ограничений по языку, дате и стране публикации не было.
Отбор исследований
Для проверки названий и аннотаций использовалась программа Covidence (Covidence systematic review software , Veritas Health Innovation, Мельбурн, Австралия). Программа Endnoteиспользовалась для отслеживания отобранных исследований и исследований для полнотекстового обзора. Скрининг названий (AL, LL, HW), аннотаций (AL, LL, HW) и полнотекстовых (AL, SE, HW) исследований проводился независимо и в двух экземплярах двумя исследователями. На этапе отбора названий и рефератов, если один из рецензентов считал цитату потенциально релевантной, исследование переходило на этап полнотекстового обзора. На этапе полнотекстового обзора разногласия разрешались путем обсуждения или арбитража третьим рецензентом (DJN). Критерии включения и исключения были опубликованы ранее [14]; вкратце, мы включали рандомизированные контролируемые исследования, нерандомизированные квазиэкспериментальные, когортные исследования, исследования «случай-контроль» или их вторичные анализы; пациентов, поступивших в любое ОРИТ; тех, кто мог получить данные о боли или обезболивающих препаратах и о частоте, распространенности или тяжести делирия. Мы исключали неоригинальные исследования; которые сообщали только о делирии при алкогольной абстиненции, делирии при наркотической абстиненции, делирии при тремоне или сообщали о нефармакологических методах в качестве основного метода обезболивания.
Извлечение данных
Данные извлекались независимо и в двух экземплярах с помощью инструмента извлечения данных, созданного в Microsoft Excel для Microsoft 365 MSO Version 2201 (Microsoft, Redmond, USA) (AL, SE, LL, NJ, HW) (подробности опубликованы [14] или в Online Resource 1).
Риск необъективности
Качество включенных исследований оценивалось с помощью Cochrane Collaborative Risk of Bias 2 assessment tool for randomised controlled trials, or Risk of Bias in Non-randomised Studies of Interventions tool for cohort studies [15-17]. Риск необъективности оценивался независимо двумя исследователями, расхождения решались путем обсуждения или третьим исследователем (DJN).
Статистический анализ
Для дихотомических исходов использовалась модель мета-анализа случайных эффектов Hartung-Knapp Sidik-Jonkmann с методом обратной дисперсии для оценки объединенного отношения шансов (ОР) и 95% доверительных интервалов (ДИ) для развития делирия. Выбор этой модели был обусловлен ее повышенной точностью при оценке доверительных интервалов в условиях неоднородности. Мы объединили данные только тех исследований, в которых связь между воздействием и делирием была представлена в виде таблицы 2 × 2, чтобы избежать нарушения статистических предпосылок при объединении точечных оценок, полученных в разных моделях. Для измеренных исходов была проведена модель мета-анализа со случайными эффектами с использованием метода обратной дисперсии для оценки стандартизированной средней разницы и 95%-ного ДИ. Первичным результатом было возникновение делирия, который представлял собой комбинацию распространенного и случайного делирия. В первичном анализе в порядке убывания изучалась связь между: (1) болью (клинически значимой и не клинически значимой) и возникновением делирия; (2) опиоидами и возникновением делирия; (3) неопиоидными обезболивающими препаратами и возникновением делирия. В связи с неоднородностью опиоидов и неопиоидов, использованных в исследованиях, эти классы препаратов анализировались по подтипам, чтобы избежать дополнительного влияния механизма действия, типа и силы связывания с рецепторами. Вторичным результатом была частота делирия. Для оценки выраженности боли мы использовали стандартизированную среднюю разницу, которая представляет собой абсолютную разницу между средним значением боли среди пациентов с делирием и без делирия с учетом вариабельности исследования.
В некоторых исследованиях сообщалось о небольшом количестве событий в группах, подвергшихся и не подвергшихся воздействию. Метод фиксированных эффектов Peto применялся к анализам, в которых в обеих группах произошло пять или менее событий, поскольку он хорошо работает с редкими событиями и не требует коррекции для исследований с нулевым числом событий [18, 19]. Предварительно проведенные анализы представлены в Online Resource 1 (или опубликованы ранее [14]). Статистическая неоднородность оценивалась с помощью статистики I2 [14]. Предвзятость публикаций оценивали с помощью воронкообразных диаграмм и регрессии Egger [20]. Анализ проводился с использованием программы Rstudio.
Анализ чувствительности и анализ подгрупп
Там, где это было возможно, анализ чувствительности проводился с использованием инцидентного делирия в качестве исхода для точного определения связи между воздействием и новыми случаями делирия. Анализ чувствительности был проведен для опиоидов, не указанных в других источниках, и делирия путем исключения исследований (Bose et al. [21] и Kalra et al. [22]), которые в которых были получены большие точечные оценки по методу Peto . Для изучения неоднородности анализа мы провели анализ подгрупп по типу ОРИТ, тяжести заболевания, а также по наличию бреда или болевого синдрома. Для оценки тяжести заболевания мы преобразовали показатель тяжести заболевания в прогнозируемую долю смертности, затем провели дихотомию на прогнозируемую смертность ≥ 50% или < 50% [23-25]. Мы не изучали гетерогенность из-за риска предвзятости, поскольку большинство включенных исследований имели высокий риск предвзятости. Также не удалось изучить гетерогенность по статусу седации, поскольку вариабельность представления данных во включенных исследованиях не позволила провести значимый анализ.
Результаты
Отбор и скрининг исследований
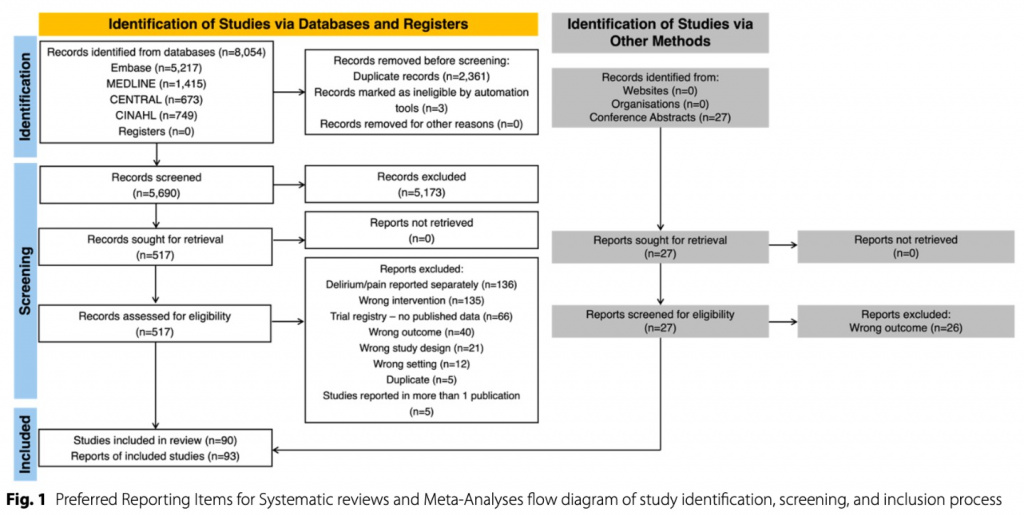
В результате электронного поиска по базам данных и ручного поиска было найдено 8 054 уникальных ссылок, 517 исследований прошли полнотекстовый обзор, и 90 из них были включены в систематический обзор (Fig. 1). Наиболее частой причиной исключения после полнотекстового обзора были данные о боли и делирии, которые не могли быть извлечены в связи друг с другом.
Характеристика включенных исследований
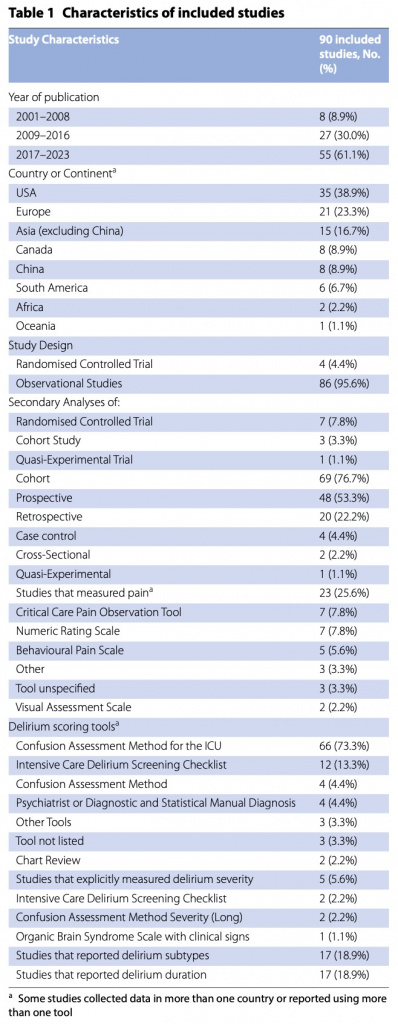
Характеристики включенных исследований представлены в Table 1. Среди 90 включенных исследований (n = 119 230 пациентов) четыре были рандомизированными контролируемыми исследованиями, 48 - проспективными когортными исследованиями и 20 - ретроспективными когортными исследованиями. Исследования проводились преимущественно в США (n = 35, 38,9%), Европе (n = 21, 23,3%) и Азии (n = 15, 16,7%). Исследования были опубликованы в период с 2001 по 2023 год и включали от 12 до 78 364 пациентов. Делирий был выявлен с помощью валидированного инструмента в 86 (95,6%) исследованиях (Table 1). Среди них 66 (73,3%) использовали CAM-ICU и 12 (13,3%) - ICDSC. О выраженности делирия сообщалось в пяти (5,6%) исследованиях. О боли сообщалось в 23 (25,6%) исследованиях; среди них в семи (7,8%) использовался инструмент наблюдения за болью в реанимации, в восьми (8,9%) - цифровая рейтинговая шкала и в пяти (5,6%) - поведенческая шкала боли. Об анальгетиках сообщалось в 89 (98,9%) исследованиях. Полная библиография включенных исследований приведена в Table S1 (Online Resource 2).
Риск необъективности
В Tables S2 и S3 (Online Resource 2) представлены оценки риска необъективности. Для первичного результата «боль и делирий» (n = 16 исследований) 3 исследования были классифицированы как умеренный риск необъективности, 2 - как серьезный риск необъективности и 11 - как критический риск необъективности. Для первичного результата «опиоиды и делирий» (n = 58 исследований) одно исследование было отнесено к категории «некоторые опасения», 12 - к категории «умеренный риск необъективности», 11 - к категории «серьезный риск необъективности» и 34 - к категории «критический риск необъективности».
Первичныq анализ
Боль и делирий
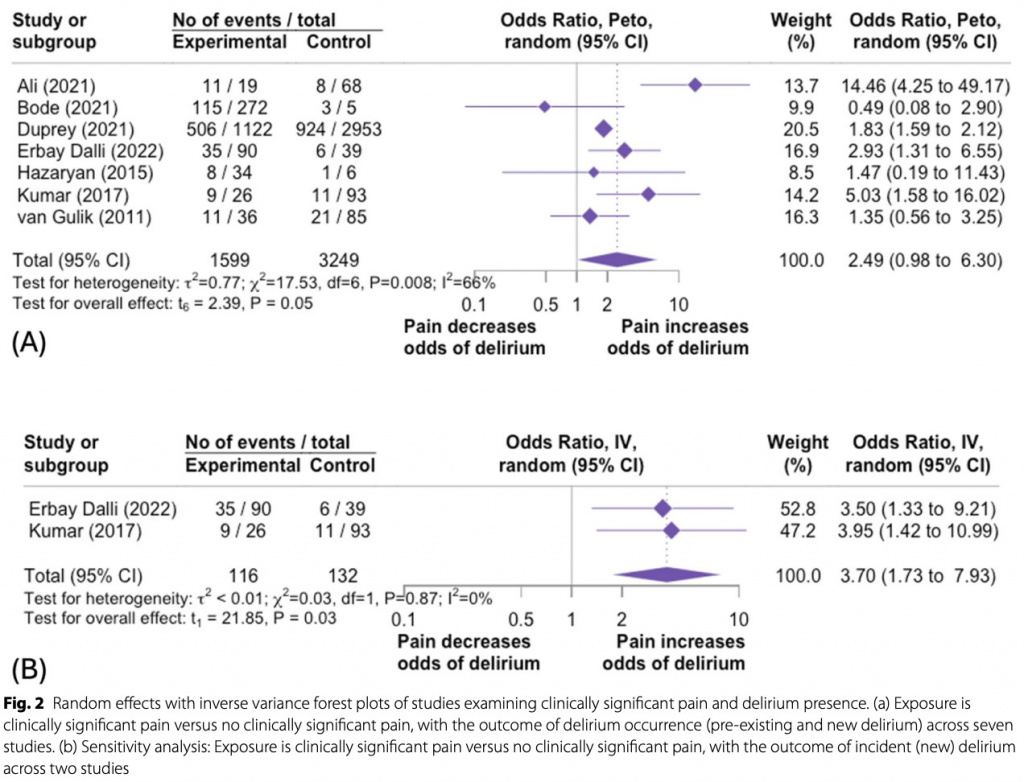
Шестнадцать исследований предоставили данные о боли и делирии. Из-за различий в представлении данных, касающихся боли и делирия, семь исследований (n = 4 848 пациентов) были включены в мета-анализ клинически значимой боли по сравнению с отсутствием клинически значимой боли и возникновением делирия (ранее существовавшие и новые случаи делирия). Наблюдалась тенденция к ассоциации между клинически значимой болью и делирием (ОР 2,49, 95% ДИ 0,98-6,30, p = 0,054, Fig. 2a). Анализ чувствительности среди исследований, в которых сообщалось о новых случаях делирия (инцидентный делирий), выявил связь между клинически значимой болью и инцидентным делирием (ОР 3,70, 95% ДИ 1,73-7,93, p = 0,03, Fig. 2b).
Опиоиды и возникновение делирия
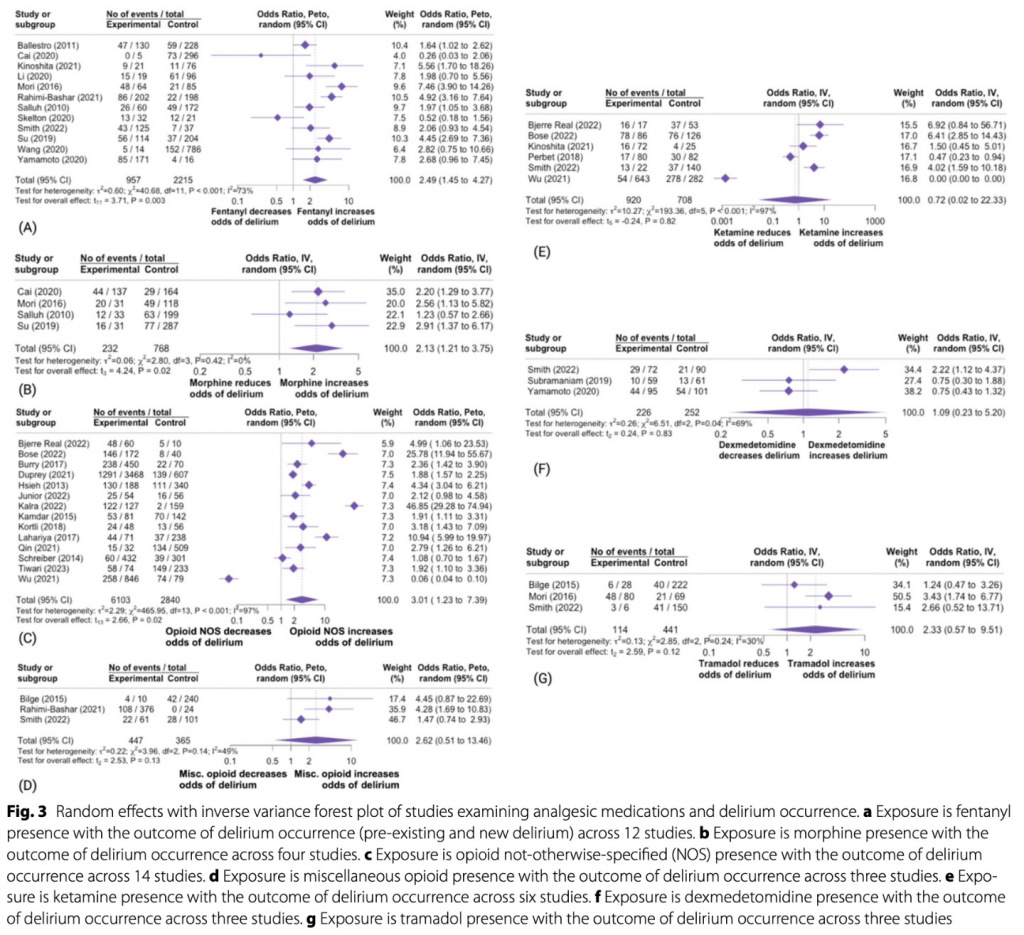
Среди 33 исследований, в которых сообщалось о воздействии фентанила и появления делирия, 12 исследований (n = 3 172 пациента) представили данные в формате 2 × 2, что позволило провести метаанализ. Была выявлена связь между воздействием фентанила и возникновением делирия (ОР 2,49, 95% ДИ 1,45-4,27, р = 0,003, Fig. 3а). Эта связь сохранилась при анализе чувствительности среди исследований, в которых сообщалось о возникновении делирия (ОР 2,21, 95% ДИ 1,69-2,89, p = 0,02, Fig. S1). Аналогичным образом, по результатам пяти исследований (n = 1 000 пациентов), посвященных морфину и делирию, мета-анализ выявил связь между воздействием морфина и возникновением делирия (ОР 2,13, 95% ДИ 1,21-3,75, p = 0,02, рис. 3b). В тех случаях, когда воздействие опиоидов не уточнялось, объединенный анализ 14 исследований (n = 8 943 пациента) выявил ассоциацию между опиоидами и возникновением делирия (ОР 3,01, 95% ДИ 1,23-7,39, p = 0,02, рис. 3c). Однако сила этой ассоциации была уменьшена после исключения двух исследований (Bose et al. [21] и Kalra et al. [22]), которые плохо сходились по методу Peto (ОР 1,98, 95% ДИ 0,89-4,38, p = 0,09, Fig. S2). В трех исследованиях (n = 812 пациентов), в которых изучалась разнородная группа опиоидов (гидроморфон, меперидин, метадон), объединенный анализ не выявил связи с возникновением делирия (ОР 2,62, 95% ДИ 0,51-13,46, p = 0,13, Fig. 3d).
Вторичный анализ
Тяжесть боли и возникновение делирия
Объединенный анализ четырех исследований (n = 4 602 пациента) показал, что умеренная или сильная боль не связана с возникновением делирия (ОР 1,07, 95% ДИ 0,13-8,52, p = 0,92, Fig. 4). Стандартизированная средняя разница - это абсолютная разница (с учетом вариабельности исследования) в баллах боли между пациентами с делирием и без него. Среди трех исследований (n = 1 736 пациентов), в которых приводилась средняя числовая оценка по шкале, объединенный анализ не выявил связи между средней разницей в оценке боли и возникновением делирия (стандартизированная средняя разница 0,09, 95% ДИ -0,50-0,68, p = 0,77, Fig. S3). Среди двух исследований (n = 656 пациентов), в которых сообщалось о средних показателях Critical Care Pain Observation Tool, объединенный анализ показал, что наличие делирия было связано с более высоким баллом боли (стандартизированная средняя разница 0,69, 95% ДИ 0,43-0,95, p < 0,001, Fig. S4).
Неопиоидные обезболивающие препараты и возникновение делирия
В шести исследованиях (n = 1628 пациентов) с адекватными данными о воздействии кетамина и делирии объединенный анализ не выявил связи между кетамином и возникновением делирия (ОР 0,72, 95% ДИ 0,02-22,33, p = 0,82, рис. 3e). Эта связь не изменилась при анализе чувствительности среди исследований, в которых сообщалось о возникновении делирия (Fig.S5). Аналогичным образом, не наблюдалось связи между другими неопиоидными анальгетиками (ацетаминофен, нестероидные противовоспалительные препараты) и возникновением делирия (Fig. 3f, 3g, S6, S7).
Обезболивающие препараты и продолжительность или тяжесть делирия
В двух исследованиях изучались обезболивающие препараты (дексмедетомидин, ацетаминофен) и тяжесть делирия (Table S4). В семи исследованиях изучались обезболивающие препараты (опиоиды, кетамин, ацетаминофен, дексмедетомидин) и продолжительность делирия. Метаанализ не проводился, так как в исследованиях были представлены различные препараты и единицы измерения времени (данные сведены в Table S5 систематического обзора).
Анализ подгрупп, изучающий источники гетерогенности в рамках первичного анализа
Первичный анализ, изучающий воздействие опиоидов и возникновение делирия, был повторен в подгруппах, определенных по: тип ОРИТ, инструмент для лечения делирия и тяжесть заболевания (Online Resource 3). Среди исследований, включавших пациентов с более низкой прогнозируемой смертностью (< 50%), воздействие опиоидов, не указанных в других источниках, было связано с возникновением делирия (ОР 2,34, 95% ДИ 1,85-2,96, p < 0,001, Fig. S8). Анализ подгрупп по фентанилу и делирию показал, что у пациентов, поступивших в ОРИТ смешанного профиля , вероятность возникновения делирия была выше (ОР 2,93, 95% ДИ 1,49-5,75, p = 0,01), в то время как у пациентов, поступивших в специализированные или соматические ОРИТ, она была выше. (Figure S9).
Предвзятость публикаций
По данным воронкообразной диаграммы или регрессии Egger для первичных и вторичных исходов не было обнаружено доказательств предвзятости публикаций (Fig. S10-S23).
Обсуждение
В нашем исследовании обобщены данные 90 исследований, охвативших 119 230 пациентов за 22 года изучения. Это исследование представляет собой всестороннее изучение связи между болью, обезболивающими препаратами и делирием. В соответствии с давними представлениями [1], мы наблюдали тенденцию к ассоциации между клинически значимой болью и уже существующим делирием, а также значительную связь между клинически значимой болью и новым развитием делирия. Мы также отметили, что воздействие морфина на взрослых в критическом состоянии связано с увеличением вероятности возникновения делирия, а фентанила - с увеличением вероятности новых случаев делирия. Воздействие других опиоидов и неопиоидных обезболивающих препаратов не связано с делирием. Объединенные точечные оценки, как правило, имели низкую точность, и лишь немногие исследования имели низкий риск предвзятости, что подчеркивает необходимость получения более надежных данных, оценивающих связь между болью, обезболивающими препаратами и делирием.
Взаимосвязь между болью и делирием является сложной. С биологической точки зрения, боль и делирий потенциально связаны через общие и перекрывающиеся пути [26]. Повышенная реакция на болевые стимулы модулируется через высвобождение хемокинов, цитокинов и глутамата, которые также могут вызывать разрушение гематоэнцефалического барьера [27, 28]. Биомаркеры, связанные с болью и гипералгезией, включают снижение уровня ацетилхолина и повышение уровня провоспалительных цитокинов, таких как интерлейкины-6, -8 и фактор некроза опухоли-α [27, 28]. При делирии "прилипание" лейкоцитов к гематоэнцефалическому барьеру повышает его проницаемость, что приводит к повышению уровня таких медиаторов воспаления, как интерлейкины-6, -8 и фактор некроза опухоли-α [26, 29].
Боль и делирий могут быть связаны между собой повышением уровня провоспалительных цитокинов, снижением уровня ацетилхолина и разрушением гематоэнцефалического барьера [9, 29]. С клинической точки зрения понимание этой взаимосвязи является сложной задачей, поскольку боль очень динамична, и лишь немногие исследования оценивают инцидентный делирий, используют методы, изменяющиеся во времени, или изучают выраженность боли в связи с делирием. Наше исследование предполагает связь между болью и новыми случаями делирия. Однако это противоречит результатам недавних исследований: Duprey et al. установили, что наличие умеренной или сильной боли снижает вероятность развития делирия у взрослых в критическом состоянии (ОР 0,71, 95% ДИ 0,60-0,85, p < 0,01) [11], а Wu et al. обнаружили, что любая степень боли не связана с развитием делирия даже с поправкой на воздействие опиоидов (ОР 0,96, 95% ДИ 0,76-1,21) [30]. И Duprey, и Wu использовали аналитические методы, изменяющиеся во времени.
В отличие от этого, два исследования, включенные в наш мета-анализ, в которых изучались боль и инцидентный делирий, были одноцентровыми проспективными обсервационными когортными исследованиями, в которых использовались модели логистической регрессии прямого отбора, не скорректированные на известные факторы, сдерживающие или изменяющие эффект [31, 32]. Erbay Dalli et al. определили, что оценка по шкале CPOT ≥ 3 ассоциируется с повышенной вероятностью возникновения делирия (ОР 4,70, 95% ДИ 1,05-20,93, p = 0,042) [31]. Среди критически больных пациентов после кардиохирургических операций Kumar et al. выявили, что послеоперационная боль была связана с возникновением делирия (ОР 2,50, 95% ДИ 1,29-4,81, р = 0,0063) [32]. Вариабельность данных о связи между болью и делирием потенциально отражает методологические различия, но оставляет клиницистов в неведении относительно того, как интегрировать лечение боли в широкую стратегию лечения делирия. В дальнейших исследованиях следует использовать строгие методы для анализа изменений во времени, а также изучать тяжесть или траекторию развития боли и делирия, чтобы информировать клиницистов о том, как лучше оптимизировать взаимосвязанное лечение боли и делирия.
Любое исследование взаимосвязи между болью и делирием должно учитывать сложное взаимодействие роли обезболивающих препаратов как потенциальных факторов, сдерживающих или изменяющих эффект. Опиоиды являются краеугольным камнем в лечении критически больных пациентов [1], их используют для анальгезии, а также с учетом их известных побочных эффектов, таких как купирование диспноэ, и в качестве дополнения к седации. Взаимосвязь между опиоидным делирием и его последствиями сложно выяснить из-за динамического дозирования и эффектов, которые могут различаться в зависимости от подтипа опиоида. Опиоиды имеют известные побочные эффекты, включая сонливость и спутанность сознания, которые могут усиливаться и ослабевать в зависимости от пиковых и низких концентраций опиоидов в сыворотке крови. Таким образом, опиоиды могут влиять на инструменты скрининга делирия, которые используют колебания психического статуса, невнимательность, дезориентацию и дезорганизованное мышление в своих параметрах оценки.
Патофизиология опиоидов и делирия может включать изменения дофамина, памяти и циклов сон-бодрствование. В делириозных состояниях высокий и низкий уровни дофамина могут иметь U-образную связь с делирием [29]. Концентрация дофамина повышается в ответ на острую боль. Опиоиды, используемые в качестве лечения, могут еще больше увеличить высвобождение дофамина [10]. Длительное воздействие опиоидов и хроническая боль нарушают сигнализацию дофамина, способствуя развитию делирия [10]. Опиоиды изменяют гиппокампальную синаптическую пластичность и нейрогенез, влияя на аффект и память, что может способствовать развитию делирия [33]. Нарушение цикла сон-бодрствование связано с делирием [26, 29]. Морфин нарушает сон и усиливает бодрствование [34]. Проведенный нами анализ свидетельствует о наличии связи между воздействием фентанила и морфина и возникновением делирия.
Mori et al. сообщили о значительной связи между морфином и распространенным делирием (ОР 2,95, 95% ДИ 1,07-8,12, p = 0,036) [35]. Среди двух исследований, включенных в наш мета-анализ, в которых изучалась экспозиция фентанила и распространенный делирий, Li et al. не обнаружили значимой связи между экспозицией фентанила и делирием (ОР 3,00, 95% ДИ 0,40-22,59, p = 0,29) [36], тогда как Smith et al. сообщили, что опиоиды, в основном фентанил, были связаны с развитием делирия (ОР опиоидов 24, 95% ДИ 16-27, p < 0,001) [37]. Подгрупповой анализ связи фентанила с делирием показал, что у пациентов, поступивших в смешанные ОРИТ, вероятность развития делирия была выше. Присутствие хирургических пациентов в общей популяции ОРИТ может повысить значимость этой взаимосвязи; предыдущие исследования показали, что фентанил повышает вероятность делирия среди хирургических пациентов [12].
В нашем обзоре исследования, в которых изучались опиоиды, отличные от фентанила и морфина (например, гидроморфон, метадон, меперидин), или изучались неопиоидные обезболивающие препараты, не выявили связи с делирием. Возможно, эти сравнения были недостаточно эффективными. Зависимость между дозой и реакцией помогла бы лучше понять связь между обезболивающими препаратами и делирием. Однако лишь немногие исследования изучали дозировку обезболивающих препаратов и делирий, а вариабельность доз (суточная доза или кумулятивная доза или доза, основанная на весе) затрудняет проведение объединенного анализа. Smith et al. сообщили о более высоких дозах фентанила и морфина у тех, у кого развился делирий, по сравнению с теми, у кого его не было [37].
Используя методы изменения во времени, Duprey et al. определили, что вероятность развития делирия возрастала с увеличением дозы синтетических опиоидов и морфина [11]. С клинической точки зрения, относительное постоянство взаимосвязи между фентанилом и морфином и развитием делирия предполагает потенциал для улучшения лечения делирия с помощью стратегий обезболивания, которые направленных на минимизацию или отказ от применения опиоидов, таких как фентанил или морфин. Будущие исследования должны быть направлены на изучение случайного делирия, обеспечение того, чтобы воздействие опиоидов предшествовало развитию делирия, использование методов анализа, изменяющихся во времени, для контроля известных факторов, четко указывающих тип опиоида при воздействии, и сообщение о дозе обезболивающего препарата.
Сильные стороны и ограничения
Данное исследование следует интерпретировать в контексте его сильных и слабых сторон. Мы использовали строгие методы, включая рецензируемую стратегию поиска и широкие критерии включения исследований, которые не ограничивались по языку, размеру выборки, инструментам для лечения делирия или популяциям пациентов ОРИТ. Хотя это внесло клиническую и статистическую неоднородность в наш объединенный анализ, полученная в результате когорта статей представляет собой современный обзор современных научных исследований по этой важной теме. К основным ограничениям данной работы относятся ограниченное количество исследований в рамках более крупного систематического обзора, которые можно было включить в мета-анализ, и небольшое количество включенных исследований, которые имели низкий риск предвзятости. Из-за неоднородности данных о боли, обезболивающих препаратах и делирии объединенный анализ этих взаимосвязей был затруднен, многие исследования были исключены из мета-анализа из-за отсутствия необходимых данных.
С точки зрения определения и для облегчения совместного анализа мы представляли боль и делирий как дихотомии (наличие или отсутствие). Следствием такого решения является потенциальное чрезмерное упрощение этой сложной взаимосвязи за счет предположения о едином эффекте при широком воздействии и/или тяжести исхода. Чтобы решить эту проблему, мы отдельно рассматривали тяжесть боли и делирия. Во многих исследованиях также не выделялся случайный делирий. Поэтому наше определение возникновения делирия может переоценить ассоциацию, поскольку у некоторых пациентов делирий мог быть исходно. Мы рассмотрели эту потенциальную переоценку, проведя анализ чувствительности среди исследований, включавших данные об инцидентах. Что касается возникновения делирия, то многие включенные исследования имели высокий риск предвзятости из-за неадекватного контроля сопутствующих факторов.
Это может преувеличить связь между болью или обезболивающими препаратами и делирием. Среди исследований, включавших данные об инцидентах, одно было с низким риском необъективности, одно - с некоторыми опасениями, а четыре - с серьезным риском необъективности. В исследованиях часто не учитывались сопутствующие факторы или модификаторы эффекта, такие как седация, не учитывались изменяющиеся во времени сопутствующие факторы или множественные подходы к оценки интенсивности боли и/или делирия, а также не всегда обеспечивалась последовательная связь между воздействием и исходом.
Выводы
В соответствии с давними представлениями, в нашем систематическом обзоре и мета-анализе была выявлена связь между болью и развитием делирия. Мы также отметили, что фентанил и морфин связаны с возникновением делирия. Мы не обнаружили связи между другими опиоидами и неопиоидными обезболивающими препаратами и делирием. Многие включенные исследования имели высокий риск необъективности из-за неадекватного контроля сопутствующих факторов. Чтобы глубже понять взаимосвязь между болью, обезболивающими препаратами и делирием, в будущих исследованиях необходимо использовать надежные методы, которые учитывали бы динамическую, изменяющуюся во времени природу потенциально многократно запутанной взаимосвязи. Наблюдаемая связь между болью и делирием в сочетании с устойчивой связью между фентанилом и морфином и развитием делирия позволяет предположить, что в ожидании дальнейших исследований один из компонентов плана лечения делирия должен включать оптимальное обезболивание с помощью стратегии, направленной на минимизацию или отказ от морфина и фентанила.
Дополнительные данные исследования (Supplementary)
References
1. Devlin JW, Skrobik Y, Gйlinas C, Needham DM, Slooter AJC, Pandharipande
PP, Watson PL, Weinhouse GL, Nunnally ME, Rochwerg B, Balas MC, van den Boogaard M, Bosma KJ, Brummel NE, Chanques G, Denehy L, Drouot X, Fraser GL, Harris JE, Joffe AM, Kho ME, Kress JP, Lanphere JA, McKinley S, Neufeld KJ, Pisani MA, Payen J-F, Pun BT, Puntillo KA, Riker RR, Robinson BRH, Shehabi Y, Szumita PM, Winkelman C, Centofanti JE, Price C, Nikayin S, Misak CJ, Flood PD, Kiedrowski K, Alhazzani W (2018) Clinical practice guidelines for the prevention and management of pain, agitation/ sedation, delirium, immobility, and sleep disruption in adult patients in the ICU. Crit Care Med 46:e825–e873
2. Martyn JAJ, Mao J, Bittner EA (2019) Opioid tolerance in critical illness. N
Engl J Med 380:365–378
3. (2013) Diagnostic and statistical manual of mental disorders : DSM-5™.
American Psychiatric Publishing, a division of American Psychiatric Association,
Washington, DC
4. Krewulak KD, Stelfox HT, Leigh JP, Wesley Ely E, Fiest KM (2018) Incidence
and prevalence of delirium subtypes in an adult ICU: A systematic review and meta-analysis. Crit Care Med 46:2029–2035
5. Krewulak KD, Stelfox HT, Ely EW, Fiest KM (2020) Risk factors and outcomes
among delirium subtypes in adult ICUs: a systematic review. J Crit Care 56:257–264
6. Goldberg TE, Chen C, Wang Y, Jung E, Swanson A, Ing C, Garcia PS,Whittington RA, Moitra V (2020) Association of delirium with long-term
cognitive decline: a meta-analysis. JAMA Neurol 77:1373–1381
7. Barr J, Fraser GL, Puntillo K, Ely EW, Gйlinas C, Dasta JF, Davidson JE,
Devlin JW, Kress JP, Joffe AM, Coursin DB, Herr DL, Tung A, Robinson BRH,
Fontaine DK, Ramsay MA, Riker RR, Sessler CN, Pun B, Skrobik Y, Jaeschke R
(2013) Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Crit Care Med 41:263–306
8. Rang HP, Dale MM (2012) Rang and dale’s pharmacology. Churchill Livingstone,Edinburgh
9. Khan BA, Perkins AJ, Campbell NL, Gao S, Farber MO, Wang S, Khan SH, Zarzaur BL, Boustani MA (2019) Pharmacological management of delirium in the intensive care unit: a randomized pragmatic clinical trial. J Am Geriatr Soc 67:1057–1065
10. Taylor AMW, Becker S, Schweinhardt P, Cahill C (2016) Mesolimbic dopamine signaling in acute and chronic pain: implications for motivation,
analgesia, and addiction. Pain 157:1194–1198
11. Duprey MS, Dijkstra-Kersten SMA, Zaal IJ, Briesacher BA, Saczynski JS,
Griffith JL, Devlin JW, Slooter AJC (2021) Opioid use increases the risk of
delirium in critically ill adults independently of pain. Am J Respir Crit Care
Med 204:566–572
12. Pandharipande P, Cotton BA, Shintani A, Thompson J, Pun BT, Morris JA
Jr, Dittus R, Ely EW (2008) Prevalence and risk factors for development of delirium in surgical and trauma intensive care unit patients. J Trauma 65:34–41
13. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD,
Shamseer L, Tetzlaff JM, Akl EA, Brennan SE, Chou R, Glanville J, Grimshaw
JM, Hrуbjartsson A, Lalu MM, Li T, Loder EW, Mayo-Wilson E, McDonald S, McGuinness LA, Stewart LA, Thomas J, Tricco AC, Welch VA, Whiting P, Moher D (2021) The PRISMA 2020 statement: An updated guideline for reporting systematic reviews. BMJ 372:n71–n79
14. Leong AY, Burry L, Fiest KM, Doig CJ, Niven DJ (2024) Does pain optimisation impact delirium outcomes in critically ill patients? A systematic
review and meta-analysis protocol. BMJ Open 14:e078395
15. Sterne JAC, Hernan MA, McAleenan A, Reeves BC, Higgins JPT (2021)
Assessing risk of bias in a non-randomized study. In: Higgins JPT, Thomas J, Chandler J, Cumpston m, Li T, Page MJ, Welch VA (eds) Cochrane Handbook
for Systematic Reviews of Interventions. Cochrane
16. Higgins JPT, Altman DG, Gшtzsche PC, Jьni P, Moher D, Oxman AD, Savović J, Schulz KF, Weeks L, Sterne JAC, (2011) The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. British Medical Journal 343
17. Sterne JAC, Savović J, Page MJ, Elbers RG, Blencowe NS, Boutron I, Cates
CJ, Cheng HY, Corbett MS, Eldridge SM, Emberson JR, Hernбn MA, Hopewell S, Hrуbjartsson A, Junqueira DR, Jьni P, Kirkham JJ, Lasserson T, Li T, McAleenan A, Reeves BC, Shepperd S, Shrier I, Stewart LA, Tilling K, White IR, Whiting PF, Higgins JPT (2019) RoB 2: A revised tool for assessing risk of bias in randomised trials. BMJ 366:l4898. https:// doi. org/ 10. 1136/bmj. l4898
18. Schwarzer G, Carpenter JR, Rucker G (2015) Meta-Analysis with R. In: Editor
(ed) (eds) Book Meta-Analysis with R. Springer International Publishing AG Switzerland, City, pp.
19. Cochrane (2023) Cochrane Handbook for Systematic Reviews of Interventions.
In: Editor (ed) (eds) Book Cochrane Handbook for Systematic Reviews of Interventions. Cochrane, City, pp.
20. Egger M, Smith GD, Minder C (1997) Bias in meta-analysis detected by a
simple, graphical test. BMJ 315:629–634
21. Bose S, Kelly L, Shahn Z, Novack L, Banner-Goodspeed V, Subramaniam B
(2022) Sedative polypharmacy mediates the effect of mechanical ventilation on delirium in critically ill COVID-19 patients: a retrospective cohort study. Acta Anaesthesiol Scand 66:1099–1106
22. Kalra SS, Jaber J, Alzghoul BN, Hyde R, Parikh S, Urbine D, Reddy R (2022)
Pre-existing psychiatric illness is associated with an increased risk of delirium in patients with acute respiratory distress syndrome. J Intensive Care Med 37:647–654
23. Le Gall J-R, Lemeshow S, Saulnier F (1993) A new Simplified Acute Physiology Score (SAPS II) based on a European/North American Multicenter
Study. JAMA 270:2957–2963
24. Vincent JL, Moreno R, Takala J, Willatts S, De Mendonзa A, Bruining H,
Reinhart CK, Suter PM, Thijs LG (1996) The SOFA (Sepsis-related Organ Failure Assessment) score to describe organ dysfunction/failure. On behalf of the Working Group on Sepsis-Related Problems of the European Society of Intensive Care Medicine. Intensive Care Med 22:707–710
25. Knaus WA, Draper EA, Wagner DP, Zimmerman JE (1985) APACHE II: a
severity of disease classification system. Crit Care Med 13:818–829
26. Maldonado JR (2018) Delirium pathophysiology: an updated hypothesis
of the etiology of acute brain failure. Int J Geriatr Psychiatry 33:1428–1457
27. Sampson EL, West E, Fischer T (2020) Pain and delirium: mechanisms,
assessment, and management. European Geriatric Medicine 11:45–52
28. DeVon HA, Piano MR, Rosenfeld AG, Hoppensteadt DA (2014) The association of pain with protein inflammatory biomarkers: a review of the literature. Nurs Res 63:51–62
29. Gunther ML, Morandi A, Ely EW (2008) Pathophysiology of delirium in the
intensive care unit. Crit Care Clin 24:45–65
30. Wu TT, Vernooij LM, Duprey MS, Zaal IJ, Gйlinas C, Devlin JW, Slooter AJC
(2023) Relationship between pain and delirium in critically ill adults. Crit Care Explor 5:e1012
31. Erbay Dalli O, Kelebek Girgin N, Kahveci F (2022) Incidence, characteristics
and risk factors of delirium in the intensive care unit: an observational study. J Clin Nurs 32(1–2):96–105
32. Kumar AK, Jayant A, Arya VK, Magoon R, Sharma R (2017) Delirium after
cardiac surgery: a pilot study from a single tertiary referral center. Ann Card Anaesth 20:76–82
33. Kibaly C, Xu C, Cahill CM, Evans CJ, Law P-Y (2019) Non-nociceptive roles
of opioids in the CNS: opioids’ effects on neurogenesis, learning, memory and affect. Nat Rev Neurosci 20:5–18
34. Eacret D, Manduchi E, Noreck J, Tyner E, Fenik P, Dunn AD, Schug J, Veasey
SC, Blendy JA (2023) Mu-opioid receptor-expressing neurons in the paraventricular thalamus modulate chronic morphine-induced wake alterations. Transl Psychiatry 13:78
35. Mori S, Takeda JRT, Carrara FSA, Cohrs CR, Zanei SSV, Whitaker IY (2016)
Incidence and factors related to delirium in an intensive care unit. Rev Esc Enferm USP 50:587–593
36. Li X, Zhang L, Gong F, Ai Y (2020) Incidence and risk factors for delirium
in older patients following intensive care unit admission: a prospective observational study. J Nurs Res JNR 28:e101
37. Smith RJ, Lachner C, Singh VP, Cartin-Ceba R (2022) Intensive care unit
delirium in patients with severe COVID-19: A prospective observational cohort study. Int J Crit Illn Inj Sci 12:61–69
[~DETAIL_TEXT] =>
SYSTEMATIC REVIEW
Amanda Y. Leong et al.
The association between pain, analgesia, and delirium among critically ill adults: a systematic review and meta-analysis
Intensive Care Med https://doi.org/10.1007/s00134-025-07784-6
Абстракт
Систематический обзор с мета-анализом, в котором изучали связь между болью или обезболивающими препаратами и возникновением, продолжительностью и тяжестью делирия.
Мы провели поиск в MEDLINE, EMBASE, CINAHL и Кокрановском центральном реестре контролируемых исследований с момента создания до 15 мая 2023 года. Мы включали рандомизированные или обсервационные исследования у взрослых в критическом состоянии, которые содержали данные о боли или воздействии анальгетиков, а также о наличии, продолжительности или тяжести делирия без языковых или региональных ограничений. IDPROSPERO: CRD42022367715. Два автора независимо друг от друга проверяли записи и извлекали данные. Риск необъективности оценивался с помощью Risk of Bias 2 или Risk of Bias In Non-randomized Studies of Interventions. Мы объединили данные с помощью модели случайных эффектов Hartung-Knapp Sidik-Jonkmann. Соблюдался стандарт PRISMA. Из 8 054 ссылок в систематический обзор было включено 90 исследований (119 230 пациентов), опубликованных в период с 2001 по 2023 год. 41 исследование было включено в первичный мета-анализ, изучающий распространенность делирия: семь исследований оценивали боль; 12 - фентанил; и пять - морфин. Наблюдалась тенденция к ассоциации между болью и возникновением делирия (ОР 2,49, 95% ДИ 0,98-6,30), а также значительная связь между болью и инцидентным делирием (ОР 3,70, 95% ДИ 1,73-7,93). Фентанил (ОР 2,49, 95% ДИ 1,45-4,27) и морфин (ОР 2,13, 95% ДИ 1,21-3,75) были связаны с возникновением делирия. Риск необъективности был критическим для многих исследований. Обнаружили ассоциацию между болью и возникновением делирия среди взрослых в критическом состоянии. Воздействие морфина или фентанила (но не других обезболивающих препаратов) было связано с повышенным риском возникновения делирия.
Ключевые слова: критическая медицина, анальгетики, боль, оценка боли, делирий
Введение
Боль - один из основных симптомов, с которым сталкиваются пациенты, находящиеся в критическом состоянии [1]. Последствия нелеченной боли включают посттравматическое стрессовое расстройство, депрессию и бессонницу [2]. Делирий - это острое состояние спутанности сознания, дефицита внимания и поведенческой дезорганизации [3]. Делирий часто встречается у больных в критическом состоянии и имеет последствия, включая увеличение продолжительности пребывания в отделении интенсивной терапии (ОРИТ) и когнитивные нарушения [1, 4-6]. Боль считается фактором риска развития делирия, однако данные, подтверждающие это мнение, ограничены [1, 7]. Симптомы делирия лечатся с помощью мультимодального подхода, который включает в себя обезболивание как ключевой принцип [1]. Однако препараты, используемые для лечения боли, связаны с нежелательными эффектами, включая дисфорию или галлюцинации, которые могут имитировать или способствовать развитию делирия [8].
Причинно-следственная связь между болью, обезболивающими препаратами и делирием неясна. Опиоиды, используемые для лечения боли, могут способствовать развитию делирия за счет изменения дофаминовой сигнализации [9, 10]. Duprey et al. сообщили, что на каждые 10 мг морфина вероятность развития делирия увеличивалась на 2,4 % [11]. Pandharipande et al. выявили, что у пациентов хирургических ОРИТ вероятность развития делирия была выше при воздействии фентанила, в то время как у пациентов с травмами вероятность развития делирия была ниже при использовании морфина [12]. В связи с неоднородностью данных о применении опиоидов и делирии неясно, связаны ли конкретные опиоиды или опиоиды как класс с наличием делирия. Для дальнейшего понимания взаимосвязи между болью и/или обезболивающими препаратами и делирием необходимо обобщить имеющуюся литературу. Это поможет врачам лучше понять, как оптимально управлять болью в контексте делирия, а ученым - узнать, на чем следует сосредоточить усилия по раскрытию взаимосвязи боли и делирия. Основной целью было изучить связь между болью (наличие и отсутствие) и делирием, а также между опиоидами (наличие и отсутствие) и делирием.
Методы
Данный систематический обзор и мета-анализ был представлен в соответствии с рекомендациями Preferred Reporting Items for Systematic Reviews and Meta-Analysis [13]. Протокол и поправки были представлены в Международный проспективный регистр систематических обзоров (PROSPERO ID: CRD42022367715) и ранее опубликованы [14].
Определение для факторов воздействия
Подробные определения приведены в онлайн-ресурсе 1. Вкратце, боль классифицировалась как отсутствие клинически значимой боли (цифровая шкала оценки 0-4, поведенческая шкала боли 3-4 или critical care pain observation tool (CPOT) 0-2) или как клинически значимая боль (цифровая шкала оценки ≥ 5, поведенческая шкала боли ≥ 5 или CPOT ≥ 3) [14]. Тяжесть боли определялась в соответствии с оценочным инструментом, использованным в опубликованном исследовании. Опиоиды классифицировались следующим образом: (1) фентанил; (2) морфин; (3) опиоиды, не указанные иначе; и (4) различные опиоиды, включая гидроморфон, метадон, меперидин и петидин. Классификация неопиоидов включала: (1) кетамин; (2) дексмедетомидин; (3) трамадол; (4) ацетаминофен; и (5) нестероидные противовоспалительные средства.
Определения исходов
Делирий определен как присутствующий или отсутствующий; наличие определялось в соответствии с опубликованными исследованиями. Чаще всего для определения делирияиспользовались confusion assessment method in ICU (CAM-ICU) или the intensive care delirium screening checklist (ICDSC). Степень тяжести делирия в данном исследовании указывалась только в том случае, если в исходном исследовании сообщалось об этом результате. Тяжесть определялась в соответствии с оценочным инструментом, использованным в исследовании. Встречаемость делирия определялась как количество всех случаев делирия (числитель) в исследуемой популяции (знаменатель) (подробные определения приведены Online Resource 1 и [14]). Заболеваемость делирием определялась как количество новых случаев делирия (числитель) в исследуемой популяции по отношению к численности исследуемой популяции- человек (знаменатель). Распространенность делирия определялась как количество случаев ранее существовавшего делирия, подсчитанное в исходный период времени исследования (числитель), по отношению к численности исследуемой популяции- человек (знаменатель).
Мы использовали показатель распространенности делирия в связи с неоднородностью исследований, в которых сообщалось о распространенности или заболеваемости делирием.
Стратегия поиска
Поиск проводился по четырем темам: (1) реанимация, (2) делирий, (3) боль и (4) обезболивающие препараты. Стратегия поиска была разработана при содействии медицинского библиотекаря и была рецензирована вторым медицинским библиотекарем с использованием методики Peer Review of Electronic Search Strategies. Поиск проводился в базах данных с момента создания до 15 мая 2023 г., включая: MEDLINE, EMBASE, Cumulative Index to Nursingand Allied Health Literature (CINAHL) и Кокрановский центральный регистр контролируемых исследований (CENTRAL). Авторы провели ручной поиск тезисов пяти крупных конференций по реаниматологии и делирию с января 2020 года по 15 мая 2023 года (подробная информация о конференциях доступна Online Resource 1). Ограничений по языку, дате и стране публикации не было.
Отбор исследований
Для проверки названий и аннотаций использовалась программа Covidence (Covidence systematic review software , Veritas Health Innovation, Мельбурн, Австралия). Программа Endnoteиспользовалась для отслеживания отобранных исследований и исследований для полнотекстового обзора. Скрининг названий (AL, LL, HW), аннотаций (AL, LL, HW) и полнотекстовых (AL, SE, HW) исследований проводился независимо и в двух экземплярах двумя исследователями. На этапе отбора названий и рефератов, если один из рецензентов считал цитату потенциально релевантной, исследование переходило на этап полнотекстового обзора. На этапе полнотекстового обзора разногласия разрешались путем обсуждения или арбитража третьим рецензентом (DJN). Критерии включения и исключения были опубликованы ранее [14]; вкратце, мы включали рандомизированные контролируемые исследования, нерандомизированные квазиэкспериментальные, когортные исследования, исследования «случай-контроль» или их вторичные анализы; пациентов, поступивших в любое ОРИТ; тех, кто мог получить данные о боли или обезболивающих препаратах и о частоте, распространенности или тяжести делирия. Мы исключали неоригинальные исследования; которые сообщали только о делирии при алкогольной абстиненции, делирии при наркотической абстиненции, делирии при тремоне или сообщали о нефармакологических методах в качестве основного метода обезболивания.
Извлечение данных
Данные извлекались независимо и в двух экземплярах с помощью инструмента извлечения данных, созданного в Microsoft Excel для Microsoft 365 MSO Version 2201 (Microsoft, Redmond, USA) (AL, SE, LL, NJ, HW) (подробности опубликованы [14] или в Online Resource 1).
Риск необъективности
Качество включенных исследований оценивалось с помощью Cochrane Collaborative Risk of Bias 2 assessment tool for randomised controlled trials, or Risk of Bias in Non-randomised Studies of Interventions tool for cohort studies [15-17]. Риск необъективности оценивался независимо двумя исследователями, расхождения решались путем обсуждения или третьим исследователем (DJN).
Статистический анализ
Для дихотомических исходов использовалась модель мета-анализа случайных эффектов Hartung-Knapp Sidik-Jonkmann с методом обратной дисперсии для оценки объединенного отношения шансов (ОР) и 95% доверительных интервалов (ДИ) для развития делирия. Выбор этой модели был обусловлен ее повышенной точностью при оценке доверительных интервалов в условиях неоднородности. Мы объединили данные только тех исследований, в которых связь между воздействием и делирием была представлена в виде таблицы 2 × 2, чтобы избежать нарушения статистических предпосылок при объединении точечных оценок, полученных в разных моделях. Для измеренных исходов была проведена модель мета-анализа со случайными эффектами с использованием метода обратной дисперсии для оценки стандартизированной средней разницы и 95%-ного ДИ. Первичным результатом было возникновение делирия, который представлял собой комбинацию распространенного и случайного делирия. В первичном анализе в порядке убывания изучалась связь между: (1) болью (клинически значимой и не клинически значимой) и возникновением делирия; (2) опиоидами и возникновением делирия; (3) неопиоидными обезболивающими препаратами и возникновением делирия. В связи с неоднородностью опиоидов и неопиоидов, использованных в исследованиях, эти классы препаратов анализировались по подтипам, чтобы избежать дополнительного влияния механизма действия, типа и силы связывания с рецепторами. Вторичным результатом была частота делирия. Для оценки выраженности боли мы использовали стандартизированную среднюю разницу, которая представляет собой абсолютную разницу между средним значением боли среди пациентов с делирием и без делирия с учетом вариабельности исследования.
В некоторых исследованиях сообщалось о небольшом количестве событий в группах, подвергшихся и не подвергшихся воздействию. Метод фиксированных эффектов Peto применялся к анализам, в которых в обеих группах произошло пять или менее событий, поскольку он хорошо работает с редкими событиями и не требует коррекции для исследований с нулевым числом событий [18, 19]. Предварительно проведенные анализы представлены в Online Resource 1 (или опубликованы ранее [14]). Статистическая неоднородность оценивалась с помощью статистики I2 [14]. Предвзятость публикаций оценивали с помощью воронкообразных диаграмм и регрессии Egger [20]. Анализ проводился с использованием программы Rstudio.
Анализ чувствительности и анализ подгрупп
Там, где это было возможно, анализ чувствительности проводился с использованием инцидентного делирия в качестве исхода для точного определения связи между воздействием и новыми случаями делирия. Анализ чувствительности был проведен для опиоидов, не указанных в других источниках, и делирия путем исключения исследований (Bose et al. [21] и Kalra et al. [22]), которые в которых были получены большие точечные оценки по методу Peto . Для изучения неоднородности анализа мы провели анализ подгрупп по типу ОРИТ, тяжести заболевания, а также по наличию бреда или болевого синдрома. Для оценки тяжести заболевания мы преобразовали показатель тяжести заболевания в прогнозируемую долю смертности, затем провели дихотомию на прогнозируемую смертность ≥ 50% или < 50% [23-25]. Мы не изучали гетерогенность из-за риска предвзятости, поскольку большинство включенных исследований имели высокий риск предвзятости. Также не удалось изучить гетерогенность по статусу седации, поскольку вариабельность представления данных во включенных исследованиях не позволила провести значимый анализ.
Результаты
Отбор и скрининг исследований
В результате электронного поиска по базам данных и ручного поиска было найдено 8 054 уникальных ссылок, 517 исследований прошли полнотекстовый обзор, и 90 из них были включены в систематический обзор (Fig. 1). Наиболее частой причиной исключения после полнотекстового обзора были данные о боли и делирии, которые не могли быть извлечены в связи друг с другом.

Характеристика включенных исследований
Характеристики включенных исследований представлены в Table 1. Среди 90 включенных исследований (n = 119 230 пациентов) четыре были рандомизированными контролируемыми исследованиями, 48 - проспективными когортными исследованиями и 20 - ретроспективными когортными исследованиями. Исследования проводились преимущественно в США (n = 35, 38,9%), Европе (n = 21, 23,3%) и Азии (n = 15, 16,7%). Исследования были опубликованы в период с 2001 по 2023 год и включали от 12 до 78 364 пациентов. Делирий был выявлен с помощью валидированного инструмента в 86 (95,6%) исследованиях (Table 1). Среди них 66 (73,3%) использовали CAM-ICU и 12 (13,3%) - ICDSC. О выраженности делирия сообщалось в пяти (5,6%) исследованиях. О боли сообщалось в 23 (25,6%) исследованиях; среди них в семи (7,8%) использовался инструмент наблюдения за болью в реанимации, в восьми (8,9%) - цифровая рейтинговая шкала и в пяти (5,6%) - поведенческая шкала боли. Об анальгетиках сообщалось в 89 (98,9%) исследованиях. Полная библиография включенных исследований приведена в Table S1 (Online Resource 2).

Риск необъективности
В Tables S2 и S3 (Online Resource 2) представлены оценки риска необъективности. Для первичного результата «боль и делирий» (n = 16 исследований) 3 исследования были классифицированы как умеренный риск необъективности, 2 - как серьезный риск необъективности и 11 - как критический риск необъективности. Для первичного результата «опиоиды и делирий» (n = 58 исследований) одно исследование было отнесено к категории «некоторые опасения», 12 - к категории «умеренный риск необъективности», 11 - к категории «серьезный риск необъективности» и 34 - к категории «критический риск необъективности».
Первичныq анализ
Боль и делирий
Шестнадцать исследований предоставили данные о боли и делирии. Из-за различий в представлении данных, касающихся боли и делирия, семь исследований (n = 4 848 пациентов) были включены в мета-анализ клинически значимой боли по сравнению с отсутствием клинически значимой боли и возникновением делирия (ранее существовавшие и новые случаи делирия). Наблюдалась тенденция к ассоциации между клинически значимой болью и делирием (ОР 2,49, 95% ДИ 0,98-6,30, p = 0,054, Fig. 2a). Анализ чувствительности среди исследований, в которых сообщалось о новых случаях делирия (инцидентный делирий), выявил связь между клинически значимой болью и инцидентным делирием (ОР 3,70, 95% ДИ 1,73-7,93, p = 0,03, Fig. 2b).

Опиоиды и возникновение делирия
Среди 33 исследований, в которых сообщалось о воздействии фентанила и появления делирия, 12 исследований (n = 3 172 пациента) представили данные в формате 2 × 2, что позволило провести метаанализ. Была выявлена связь между воздействием фентанила и возникновением делирия (ОР 2,49, 95% ДИ 1,45-4,27, р = 0,003, Fig. 3а). Эта связь сохранилась при анализе чувствительности среди исследований, в которых сообщалось о возникновении делирия (ОР 2,21, 95% ДИ 1,69-2,89, p = 0,02, Fig. S1). Аналогичным образом, по результатам пяти исследований (n = 1 000 пациентов), посвященных морфину и делирию, мета-анализ выявил связь между воздействием морфина и возникновением делирия (ОР 2,13, 95% ДИ 1,21-3,75, p = 0,02, рис. 3b). В тех случаях, когда воздействие опиоидов не уточнялось, объединенный анализ 14 исследований (n = 8 943 пациента) выявил ассоциацию между опиоидами и возникновением делирия (ОР 3,01, 95% ДИ 1,23-7,39, p = 0,02, рис. 3c). Однако сила этой ассоциации была уменьшена после исключения двух исследований (Bose et al. [21] и Kalra et al. [22]), которые плохо сходились по методу Peto (ОР 1,98, 95% ДИ 0,89-4,38, p = 0,09, Fig. S2). В трех исследованиях (n = 812 пациентов), в которых изучалась разнородная группа опиоидов (гидроморфон, меперидин, метадон), объединенный анализ не выявил связи с возникновением делирия (ОР 2,62, 95% ДИ 0,51-13,46, p = 0,13, Fig. 3d).

Вторичный анализ
Тяжесть боли и возникновение делирия
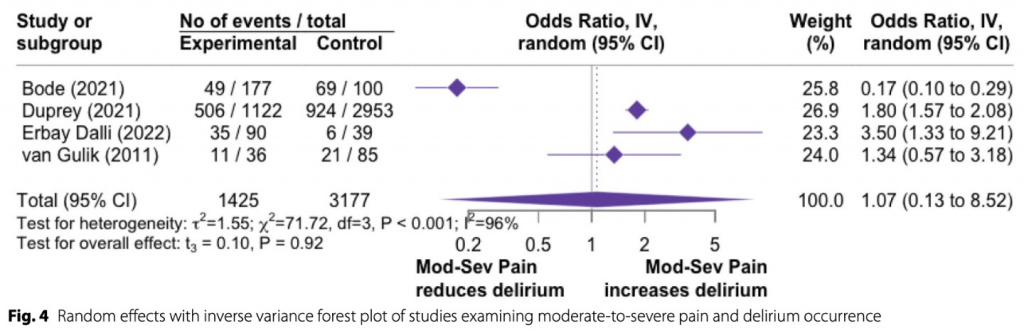
Объединенный анализ четырех исследований (n = 4 602 пациента) показал, что умеренная или сильная боль не связана с возникновением делирия (ОР 1,07, 95% ДИ 0,13-8,52, p = 0,92, Fig. 4). Стандартизированная средняя разница - это абсолютная разница (с учетом вариабельности исследования) в баллах боли между пациентами с делирием и без него. Среди трех исследований (n = 1 736 пациентов), в которых приводилась средняя числовая оценка по шкале, объединенный анализ не выявил связи между средней разницей в оценке боли и возникновением делирия (стандартизированная средняя разница 0,09, 95% ДИ -0,50-0,68, p = 0,77, Fig. S3). Среди двух исследований (n = 656 пациентов), в которых сообщалось о средних показателях Critical Care Pain Observation Tool, объединенный анализ показал, что наличие делирия было связано с более высоким баллом боли (стандартизированная средняя разница 0,69, 95% ДИ 0,43-0,95, p < 0,001, Fig. S4).

Неопиоидные обезболивающие препараты и возникновение делирия
В шести исследованиях (n = 1628 пациентов) с адекватными данными о воздействии кетамина и делирии объединенный анализ не выявил связи между кетамином и возникновением делирия (ОР 0,72, 95% ДИ 0,02-22,33, p = 0,82, рис. 3e). Эта связь не изменилась при анализе чувствительности среди исследований, в которых сообщалось о возникновении делирия (Fig.S5). Аналогичным образом, не наблюдалось связи между другими неопиоидными анальгетиками (ацетаминофен, нестероидные противовоспалительные препараты) и возникновением делирия (Fig. 3f, 3g, S6, S7).
Обезболивающие препараты и продолжительность или тяжесть делирия
В двух исследованиях изучались обезболивающие препараты (дексмедетомидин, ацетаминофен) и тяжесть делирия (Table S4). В семи исследованиях изучались обезболивающие препараты (опиоиды, кетамин, ацетаминофен, дексмедетомидин) и продолжительность делирия. Метаанализ не проводился, так как в исследованиях были представлены различные препараты и единицы измерения времени (данные сведены в Table S5 систематического обзора).
Анализ подгрупп, изучающий источники гетерогенности в рамках первичного анализа
Первичный анализ, изучающий воздействие опиоидов и возникновение делирия, был повторен в подгруппах, определенных по: тип ОРИТ, инструмент для лечения делирия и тяжесть заболевания (Online Resource 3). Среди исследований, включавших пациентов с более низкой прогнозируемой смертностью (< 50%), воздействие опиоидов, не указанных в других источниках, было связано с возникновением делирия (ОР 2,34, 95% ДИ 1,85-2,96, p < 0,001, Fig. S8). Анализ подгрупп по фентанилу и делирию показал, что у пациентов, поступивших в ОРИТ смешанного профиля , вероятность возникновения делирия была выше (ОР 2,93, 95% ДИ 1,49-5,75, p = 0,01), в то время как у пациентов, поступивших в специализированные или соматические ОРИТ, она была выше. (Figure S9).
Предвзятость публикаций
По данным воронкообразной диаграммы или регрессии Egger для первичных и вторичных исходов не было обнаружено доказательств предвзятости публикаций (Fig. S10-S23).
Обсуждение
В нашем исследовании обобщены данные 90 исследований, охвативших 119 230 пациентов за 22 года изучения. Это исследование представляет собой всестороннее изучение связи между болью, обезболивающими препаратами и делирием. В соответствии с давними представлениями [1], мы наблюдали тенденцию к ассоциации между клинически значимой болью и уже существующим делирием, а также значительную связь между клинически значимой болью и новым развитием делирия. Мы также отметили, что воздействие морфина на взрослых в критическом состоянии связано с увеличением вероятности возникновения делирия, а фентанила - с увеличением вероятности новых случаев делирия. Воздействие других опиоидов и неопиоидных обезболивающих препаратов не связано с делирием. Объединенные точечные оценки, как правило, имели низкую точность, и лишь немногие исследования имели низкий риск предвзятости, что подчеркивает необходимость получения более надежных данных, оценивающих связь между болью, обезболивающими препаратами и делирием.
Взаимосвязь между болью и делирием является сложной. С биологической точки зрения, боль и делирий потенциально связаны через общие и перекрывающиеся пути [26]. Повышенная реакция на болевые стимулы модулируется через высвобождение хемокинов, цитокинов и глутамата, которые также могут вызывать разрушение гематоэнцефалического барьера [27, 28]. Биомаркеры, связанные с болью и гипералгезией, включают снижение уровня ацетилхолина и повышение уровня провоспалительных цитокинов, таких как интерлейкины-6, -8 и фактор некроза опухоли-α [27, 28]. При делирии "прилипание" лейкоцитов к гематоэнцефалическому барьеру повышает его проницаемость, что приводит к повышению уровня таких медиаторов воспаления, как интерлейкины-6, -8 и фактор некроза опухоли-α [26, 29].
Боль и делирий могут быть связаны между собой повышением уровня провоспалительных цитокинов, снижением уровня ацетилхолина и разрушением гематоэнцефалического барьера [9, 29]. С клинической точки зрения понимание этой взаимосвязи является сложной задачей, поскольку боль очень динамична, и лишь немногие исследования оценивают инцидентный делирий, используют методы, изменяющиеся во времени, или изучают выраженность боли в связи с делирием. Наше исследование предполагает связь между болью и новыми случаями делирия. Однако это противоречит результатам недавних исследований: Duprey et al. установили, что наличие умеренной или сильной боли снижает вероятность развития делирия у взрослых в критическом состоянии (ОР 0,71, 95% ДИ 0,60-0,85, p < 0,01) [11], а Wu et al. обнаружили, что любая степень боли не связана с развитием делирия даже с поправкой на воздействие опиоидов (ОР 0,96, 95% ДИ 0,76-1,21) [30]. И Duprey, и Wu использовали аналитические методы, изменяющиеся во времени.
В отличие от этого, два исследования, включенные в наш мета-анализ, в которых изучались боль и инцидентный делирий, были одноцентровыми проспективными обсервационными когортными исследованиями, в которых использовались модели логистической регрессии прямого отбора, не скорректированные на известные факторы, сдерживающие или изменяющие эффект [31, 32]. Erbay Dalli et al. определили, что оценка по шкале CPOT ≥ 3 ассоциируется с повышенной вероятностью возникновения делирия (ОР 4,70, 95% ДИ 1,05-20,93, p = 0,042) [31]. Среди критически больных пациентов после кардиохирургических операций Kumar et al. выявили, что послеоперационная боль была связана с возникновением делирия (ОР 2,50, 95% ДИ 1,29-4,81, р = 0,0063) [32]. Вариабельность данных о связи между болью и делирием потенциально отражает методологические различия, но оставляет клиницистов в неведении относительно того, как интегрировать лечение боли в широкую стратегию лечения делирия. В дальнейших исследованиях следует использовать строгие методы для анализа изменений во времени, а также изучать тяжесть или траекторию развития боли и делирия, чтобы информировать клиницистов о том, как лучше оптимизировать взаимосвязанное лечение боли и делирия.
Любое исследование взаимосвязи между болью и делирием должно учитывать сложное взаимодействие роли обезболивающих препаратов как потенциальных факторов, сдерживающих или изменяющих эффект. Опиоиды являются краеугольным камнем в лечении критически больных пациентов [1], их используют для анальгезии, а также с учетом их известных побочных эффектов, таких как купирование диспноэ, и в качестве дополнения к седации. Взаимосвязь между опиоидным делирием и его последствиями сложно выяснить из-за динамического дозирования и эффектов, которые могут различаться в зависимости от подтипа опиоида. Опиоиды имеют известные побочные эффекты, включая сонливость и спутанность сознания, которые могут усиливаться и ослабевать в зависимости от пиковых и низких концентраций опиоидов в сыворотке крови. Таким образом, опиоиды могут влиять на инструменты скрининга делирия, которые используют колебания психического статуса, невнимательность, дезориентацию и дезорганизованное мышление в своих параметрах оценки.
Патофизиология опиоидов и делирия может включать изменения дофамина, памяти и циклов сон-бодрствование. В делириозных состояниях высокий и низкий уровни дофамина могут иметь U-образную связь с делирием [29]. Концентрация дофамина повышается в ответ на острую боль. Опиоиды, используемые в качестве лечения, могут еще больше увеличить высвобождение дофамина [10]. Длительное воздействие опиоидов и хроническая боль нарушают сигнализацию дофамина, способствуя развитию делирия [10]. Опиоиды изменяют гиппокампальную синаптическую пластичность и нейрогенез, влияя на аффект и память, что может способствовать развитию делирия [33]. Нарушение цикла сон-бодрствование связано с делирием [26, 29]. Морфин нарушает сон и усиливает бодрствование [34]. Проведенный нами анализ свидетельствует о наличии связи между воздействием фентанила и морфина и возникновением делирия.
Mori et al. сообщили о значительной связи между морфином и распространенным делирием (ОР 2,95, 95% ДИ 1,07-8,12, p = 0,036) [35]. Среди двух исследований, включенных в наш мета-анализ, в которых изучалась экспозиция фентанила и распространенный делирий, Li et al. не обнаружили значимой связи между экспозицией фентанила и делирием (ОР 3,00, 95% ДИ 0,40-22,59, p = 0,29) [36], тогда как Smith et al. сообщили, что опиоиды, в основном фентанил, были связаны с развитием делирия (ОР опиоидов 24, 95% ДИ 16-27, p < 0,001) [37]. Подгрупповой анализ связи фентанила с делирием показал, что у пациентов, поступивших в смешанные ОРИТ, вероятность развития делирия была выше. Присутствие хирургических пациентов в общей популяции ОРИТ может повысить значимость этой взаимосвязи; предыдущие исследования показали, что фентанил повышает вероятность делирия среди хирургических пациентов [12].
В нашем обзоре исследования, в которых изучались опиоиды, отличные от фентанила и морфина (например, гидроморфон, метадон, меперидин), или изучались неопиоидные обезболивающие препараты, не выявили связи с делирием. Возможно, эти сравнения были недостаточно эффективными. Зависимость между дозой и реакцией помогла бы лучше понять связь между обезболивающими препаратами и делирием. Однако лишь немногие исследования изучали дозировку обезболивающих препаратов и делирий, а вариабельность доз (суточная доза или кумулятивная доза или доза, основанная на весе) затрудняет проведение объединенного анализа. Smith et al. сообщили о более высоких дозах фентанила и морфина у тех, у кого развился делирий, по сравнению с теми, у кого его не было [37].
Используя методы изменения во времени, Duprey et al. определили, что вероятность развития делирия возрастала с увеличением дозы синтетических опиоидов и морфина [11]. С клинической точки зрения, относительное постоянство взаимосвязи между фентанилом и морфином и развитием делирия предполагает потенциал для улучшения лечения делирия с помощью стратегий обезболивания, которые направленных на минимизацию или отказ от применения опиоидов, таких как фентанил или морфин. Будущие исследования должны быть направлены на изучение случайного делирия, обеспечение того, чтобы воздействие опиоидов предшествовало развитию делирия, использование методов анализа, изменяющихся во времени, для контроля известных факторов, четко указывающих тип опиоида при воздействии, и сообщение о дозе обезболивающего препарата.
Сильные стороны и ограничения
Данное исследование следует интерпретировать в контексте его сильных и слабых сторон. Мы использовали строгие методы, включая рецензируемую стратегию поиска и широкие критерии включения исследований, которые не ограничивались по языку, размеру выборки, инструментам для лечения делирия или популяциям пациентов ОРИТ. Хотя это внесло клиническую и статистическую неоднородность в наш объединенный анализ, полученная в результате когорта статей представляет собой современный обзор современных научных исследований по этой важной теме. К основным ограничениям данной работы относятся ограниченное количество исследований в рамках более крупного систематического обзора, которые можно было включить в мета-анализ, и небольшое количество включенных исследований, которые имели низкий риск предвзятости. Из-за неоднородности данных о боли, обезболивающих препаратах и делирии объединенный анализ этих взаимосвязей был затруднен, многие исследования были исключены из мета-анализа из-за отсутствия необходимых данных.
С точки зрения определения и для облегчения совместного анализа мы представляли боль и делирий как дихотомии (наличие или отсутствие). Следствием такого решения является потенциальное чрезмерное упрощение этой сложной взаимосвязи за счет предположения о едином эффекте при широком воздействии и/или тяжести исхода. Чтобы решить эту проблему, мы отдельно рассматривали тяжесть боли и делирия. Во многих исследованиях также не выделялся случайный делирий. Поэтому наше определение возникновения делирия может переоценить ассоциацию, поскольку у некоторых пациентов делирий мог быть исходно. Мы рассмотрели эту потенциальную переоценку, проведя анализ чувствительности среди исследований, включавших данные об инцидентах. Что касается возникновения делирия, то многие включенные исследования имели высокий риск предвзятости из-за неадекватного контроля сопутствующих факторов.
Это может преувеличить связь между болью или обезболивающими препаратами и делирием. Среди исследований, включавших данные об инцидентах, одно было с низким риском необъективности, одно - с некоторыми опасениями, а четыре - с серьезным риском необъективности. В исследованиях часто не учитывались сопутствующие факторы или модификаторы эффекта, такие как седация, не учитывались изменяющиеся во времени сопутствующие факторы или множественные подходы к оценки интенсивности боли и/или делирия, а также не всегда обеспечивалась последовательная связь между воздействием и исходом.
Выводы
В соответствии с давними представлениями, в нашем систематическом обзоре и мета-анализе была выявлена связь между болью и развитием делирия. Мы также отметили, что фентанил и морфин связаны с возникновением делирия. Мы не обнаружили связи между другими опиоидами и неопиоидными обезболивающими препаратами и делирием. Многие включенные исследования имели высокий риск необъективности из-за неадекватного контроля сопутствующих факторов. Чтобы глубже понять взаимосвязь между болью, обезболивающими препаратами и делирием, в будущих исследованиях необходимо использовать надежные методы, которые учитывали бы динамическую, изменяющуюся во времени природу потенциально многократно запутанной взаимосвязи. Наблюдаемая связь между болью и делирием в сочетании с устойчивой связью между фентанилом и морфином и развитием делирия позволяет предположить, что в ожидании дальнейших исследований один из компонентов плана лечения делирия должен включать оптимальное обезболивание с помощью стратегии, направленной на минимизацию или отказ от морфина и фентанила.
Дополнительные данные исследования (Supplementary)
References
1. Devlin JW, Skrobik Y, Gйlinas C, Needham DM, Slooter AJC, Pandharipande
PP, Watson PL, Weinhouse GL, Nunnally ME, Rochwerg B, Balas MC, van den Boogaard M, Bosma KJ, Brummel NE, Chanques G, Denehy L, Drouot X, Fraser GL, Harris JE, Joffe AM, Kho ME, Kress JP, Lanphere JA, McKinley S, Neufeld KJ, Pisani MA, Payen J-F, Pun BT, Puntillo KA, Riker RR, Robinson BRH, Shehabi Y, Szumita PM, Winkelman C, Centofanti JE, Price C, Nikayin S, Misak CJ, Flood PD, Kiedrowski K, Alhazzani W (2018) Clinical practice guidelines for the prevention and management of pain, agitation/ sedation, delirium, immobility, and sleep disruption in adult patients in the ICU. Crit Care Med 46:e825–e873
2. Martyn JAJ, Mao J, Bittner EA (2019) Opioid tolerance in critical illness. N
Engl J Med 380:365–378
3. (2013) Diagnostic and statistical manual of mental disorders : DSM-5™.
American Psychiatric Publishing, a division of American Psychiatric Association,
Washington, DC
4. Krewulak KD, Stelfox HT, Leigh JP, Wesley Ely E, Fiest KM (2018) Incidence
and prevalence of delirium subtypes in an adult ICU: A systematic review and meta-analysis. Crit Care Med 46:2029–2035
5. Krewulak KD, Stelfox HT, Ely EW, Fiest KM (2020) Risk factors and outcomes
among delirium subtypes in adult ICUs: a systematic review. J Crit Care 56:257–264
6. Goldberg TE, Chen C, Wang Y, Jung E, Swanson A, Ing C, Garcia PS,Whittington RA, Moitra V (2020) Association of delirium with long-term
cognitive decline: a meta-analysis. JAMA Neurol 77:1373–1381
7. Barr J, Fraser GL, Puntillo K, Ely EW, Gйlinas C, Dasta JF, Davidson JE,
Devlin JW, Kress JP, Joffe AM, Coursin DB, Herr DL, Tung A, Robinson BRH,
Fontaine DK, Ramsay MA, Riker RR, Sessler CN, Pun B, Skrobik Y, Jaeschke R
(2013) Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Crit Care Med 41:263–306
8. Rang HP, Dale MM (2012) Rang and dale’s pharmacology. Churchill Livingstone,Edinburgh
9. Khan BA, Perkins AJ, Campbell NL, Gao S, Farber MO, Wang S, Khan SH, Zarzaur BL, Boustani MA (2019) Pharmacological management of delirium in the intensive care unit: a randomized pragmatic clinical trial. J Am Geriatr Soc 67:1057–1065
10. Taylor AMW, Becker S, Schweinhardt P, Cahill C (2016) Mesolimbic dopamine signaling in acute and chronic pain: implications for motivation,
analgesia, and addiction. Pain 157:1194–1198
11. Duprey MS, Dijkstra-Kersten SMA, Zaal IJ, Briesacher BA, Saczynski JS,
Griffith JL, Devlin JW, Slooter AJC (2021) Opioid use increases the risk of
delirium in critically ill adults independently of pain. Am J Respir Crit Care
Med 204:566–572
12. Pandharipande P, Cotton BA, Shintani A, Thompson J, Pun BT, Morris JA
Jr, Dittus R, Ely EW (2008) Prevalence and risk factors for development of delirium in surgical and trauma intensive care unit patients. J Trauma 65:34–41
13. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD,
Shamseer L, Tetzlaff JM, Akl EA, Brennan SE, Chou R, Glanville J, Grimshaw
JM, Hrуbjartsson A, Lalu MM, Li T, Loder EW, Mayo-Wilson E, McDonald S, McGuinness LA, Stewart LA, Thomas J, Tricco AC, Welch VA, Whiting P, Moher D (2021) The PRISMA 2020 statement: An updated guideline for reporting systematic reviews. BMJ 372:n71–n79
14. Leong AY, Burry L, Fiest KM, Doig CJ, Niven DJ (2024) Does pain optimisation impact delirium outcomes in critically ill patients? A systematic
review and meta-analysis protocol. BMJ Open 14:e078395
15. Sterne JAC, Hernan MA, McAleenan A, Reeves BC, Higgins JPT (2021)
Assessing risk of bias in a non-randomized study. In: Higgins JPT, Thomas J, Chandler J, Cumpston m, Li T, Page MJ, Welch VA (eds) Cochrane Handbook
for Systematic Reviews of Interventions. Cochrane
16. Higgins JPT, Altman DG, Gшtzsche PC, Jьni P, Moher D, Oxman AD, Savović J, Schulz KF, Weeks L, Sterne JAC, (2011) The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. British Medical Journal 343
17. Sterne JAC, Savović J, Page MJ, Elbers RG, Blencowe NS, Boutron I, Cates
CJ, Cheng HY, Corbett MS, Eldridge SM, Emberson JR, Hernбn MA, Hopewell S, Hrуbjartsson A, Junqueira DR, Jьni P, Kirkham JJ, Lasserson T, Li T, McAleenan A, Reeves BC, Shepperd S, Shrier I, Stewart LA, Tilling K, White IR, Whiting PF, Higgins JPT (2019) RoB 2: A revised tool for assessing risk of bias in randomised trials. BMJ 366:l4898. https:// doi. org/ 10. 1136/bmj. l4898
18. Schwarzer G, Carpenter JR, Rucker G (2015) Meta-Analysis with R. In: Editor
(ed) (eds) Book Meta-Analysis with R. Springer International Publishing AG Switzerland, City, pp.
19. Cochrane (2023) Cochrane Handbook for Systematic Reviews of Interventions.
In: Editor (ed) (eds) Book Cochrane Handbook for Systematic Reviews of Interventions. Cochrane, City, pp.
20. Egger M, Smith GD, Minder C (1997) Bias in meta-analysis detected by a
simple, graphical test. BMJ 315:629–634
21. Bose S, Kelly L, Shahn Z, Novack L, Banner-Goodspeed V, Subramaniam B
(2022) Sedative polypharmacy mediates the effect of mechanical ventilation on delirium in critically ill COVID-19 patients: a retrospective cohort study. Acta Anaesthesiol Scand 66:1099–1106
22. Kalra SS, Jaber J, Alzghoul BN, Hyde R, Parikh S, Urbine D, Reddy R (2022)
Pre-existing psychiatric illness is associated with an increased risk of delirium in patients with acute respiratory distress syndrome. J Intensive Care Med 37:647–654
23. Le Gall J-R, Lemeshow S, Saulnier F (1993) A new Simplified Acute Physiology Score (SAPS II) based on a European/North American Multicenter
Study. JAMA 270:2957–2963
24. Vincent JL, Moreno R, Takala J, Willatts S, De Mendonзa A, Bruining H,
Reinhart CK, Suter PM, Thijs LG (1996) The SOFA (Sepsis-related Organ Failure Assessment) score to describe organ dysfunction/failure. On behalf of the Working Group on Sepsis-Related Problems of the European Society of Intensive Care Medicine. Intensive Care Med 22:707–710
25. Knaus WA, Draper EA, Wagner DP, Zimmerman JE (1985) APACHE II: a
severity of disease classification system. Crit Care Med 13:818–829
26. Maldonado JR (2018) Delirium pathophysiology: an updated hypothesis
of the etiology of acute brain failure. Int J Geriatr Psychiatry 33:1428–1457
27. Sampson EL, West E, Fischer T (2020) Pain and delirium: mechanisms,
assessment, and management. European Geriatric Medicine 11:45–52
28. DeVon HA, Piano MR, Rosenfeld AG, Hoppensteadt DA (2014) The association of pain with protein inflammatory biomarkers: a review of the literature. Nurs Res 63:51–62
29. Gunther ML, Morandi A, Ely EW (2008) Pathophysiology of delirium in the
intensive care unit. Crit Care Clin 24:45–65
30. Wu TT, Vernooij LM, Duprey MS, Zaal IJ, Gйlinas C, Devlin JW, Slooter AJC
(2023) Relationship between pain and delirium in critically ill adults. Crit Care Explor 5:e1012
31. Erbay Dalli O, Kelebek Girgin N, Kahveci F (2022) Incidence, characteristics
and risk factors of delirium in the intensive care unit: an observational study. J Clin Nurs 32(1–2):96–105
32. Kumar AK, Jayant A, Arya VK, Magoon R, Sharma R (2017) Delirium after
cardiac surgery: a pilot study from a single tertiary referral center. Ann Card Anaesth 20:76–82
33. Kibaly C, Xu C, Cahill CM, Evans CJ, Law P-Y (2019) Non-nociceptive roles
of opioids in the CNS: opioids’ effects on neurogenesis, learning, memory and affect. Nat Rev Neurosci 20:5–18
34. Eacret D, Manduchi E, Noreck J, Tyner E, Fenik P, Dunn AD, Schug J, Veasey
SC, Blendy JA (2023) Mu-opioid receptor-expressing neurons in the paraventricular thalamus modulate chronic morphine-induced wake alterations. Transl Psychiatry 13:78
35. Mori S, Takeda JRT, Carrara FSA, Cohrs CR, Zanei SSV, Whitaker IY (2016)
Incidence and factors related to delirium in an intensive care unit. Rev Esc Enferm USP 50:587–593
36. Li X, Zhang L, Gong F, Ai Y (2020) Incidence and risk factors for delirium
in older patients following intensive care unit admission: a prospective observational study. J Nurs Res JNR 28:e101
37. Smith RJ, Lachner C, Singh VP, Cartin-Ceba R (2022) Intensive care unit
delirium in patients with severe COVID-19: A prospective observational cohort study. Int J Crit Illn Inj Sci 12:61–69
[DETAIL_PICTURE] =>
[~DETAIL_PICTURE] =>
[DATE_ACTIVE_FROM] => 07.05.2025 00:01:00
[~DATE_ACTIVE_FROM] => 07.05.2025 00:01:00
[ACTIVE_FROM_X] => 2025-05-07 00:01:00
[~ACTIVE_FROM_X] => 2025-05-07 00:01:00
[ACTIVE_FROM] => 07.05.2025 00:01:00
[~ACTIVE_FROM] => 07.05.2025 00:01:00
[SHOW_COUNTER] => 353
[~SHOW_COUNTER] => 353
[ID] => 8524
[~ID] => 8524
[IBLOCK_ID] => 2
[~IBLOCK_ID] => 2
[IBLOCK_SECTION_ID] =>
[~IBLOCK_SECTION_ID] =>
[DETAIL_TEXT_TYPE] => html
[~DETAIL_TEXT_TYPE] => html
[PREVIEW_TEXT] =>
[~PREVIEW_TEXT] =>
[PREVIEW_TEXT_TYPE] => html
[~PREVIEW_TEXT_TYPE] => html
[TIMESTAMP_X] => 12.05.2025 12:05:49
[~TIMESTAMP_X] => 12.05.2025 12:05:49
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/svyaz-mezhdu-bolyu-analgeziey-i-deliriem-u-vzroslykh-v-kriticheskom-sostoyanii-sistematicheskiy-obzo/
[~DETAIL_PAGE_URL] => /library/articles/svyaz-mezhdu-bolyu-analgeziey-i-deliriem-u-vzroslykh-v-kriticheskom-sostoyanii-sistematicheskiy-obzo/
[LANG_DIR] => /
[~LANG_DIR] => /
[CODE] => svyaz-mezhdu-bolyu-analgeziey-i-deliriem-u-vzroslykh-v-kriticheskom-sostoyanii-sistematicheskiy-obzo
[~CODE] => svyaz-mezhdu-bolyu-analgeziey-i-deliriem-u-vzroslykh-v-kriticheskom-sostoyanii-sistematicheskiy-obzo
[EXTERNAL_ID] => 8524
[~EXTERNAL_ID] => 8524
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[IBLOCK_CODE] => articles
[~IBLOCK_CODE] => articles
[IBLOCK_EXTERNAL_ID] => content-articles
[~IBLOCK_EXTERNAL_ID] => content-articles
[LID] => s1
[~LID] => s1
[NAV_RESULT] =>
[NAV_CACHED_DATA] =>
[DISPLAY_ACTIVE_FROM] => 7 мая 2025
[IPROPERTY_VALUES] => Array
(
)
[FIELDS] => Array
(
[NAME] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[PREVIEW_PICTURE] => Array
(
[ID] => 6113
[TIMESTAMP_X] => 12.05.2025 12:05:49
[MODULE_ID] => iblock
[HEIGHT] => 750
[WIDTH] => 1000
[FILE_SIZE] => 515585
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/02d/dd6y00xg7r54b34kwprbotancagip70s
[FILE_NAME] => 3258.jpg
[ORIGINAL_NAME] => 3258.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => ebcc3fa8cb4c58a890ccc140dd3821b4
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/02d/dd6y00xg7r54b34kwprbotancagip70s/3258.jpg
[UNSAFE_SRC] => /upload/iblock/02d/dd6y00xg7r54b34kwprbotancagip70s/3258.jpg
[SAFE_SRC] => /upload/iblock/02d/dd6y00xg7r54b34kwprbotancagip70s/3258.jpg
[ALT] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[TITLE] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
)
[DETAIL_TEXT] =>
SYSTEMATIC REVIEW
Amanda Y. Leong et al.
The association between pain, analgesia, and delirium among critically ill adults: a systematic review and meta-analysis
Intensive Care Med https://doi.org/10.1007/s00134-025-07784-6
Абстракт
Систематический обзор с мета-анализом, в котором изучали связь между болью или обезболивающими препаратами и возникновением, продолжительностью и тяжестью делирия.
Мы провели поиск в MEDLINE, EMBASE, CINAHL и Кокрановском центральном реестре контролируемых исследований с момента создания до 15 мая 2023 года. Мы включали рандомизированные или обсервационные исследования у взрослых в критическом состоянии, которые содержали данные о боли или воздействии анальгетиков, а также о наличии, продолжительности или тяжести делирия без языковых или региональных ограничений. IDPROSPERO: CRD42022367715. Два автора независимо друг от друга проверяли записи и извлекали данные. Риск необъективности оценивался с помощью Risk of Bias 2 или Risk of Bias In Non-randomized Studies of Interventions. Мы объединили данные с помощью модели случайных эффектов Hartung-Knapp Sidik-Jonkmann. Соблюдался стандарт PRISMA. Из 8 054 ссылок в систематический обзор было включено 90 исследований (119 230 пациентов), опубликованных в период с 2001 по 2023 год. 41 исследование было включено в первичный мета-анализ, изучающий распространенность делирия: семь исследований оценивали боль; 12 - фентанил; и пять - морфин. Наблюдалась тенденция к ассоциации между болью и возникновением делирия (ОР 2,49, 95% ДИ 0,98-6,30), а также значительная связь между болью и инцидентным делирием (ОР 3,70, 95% ДИ 1,73-7,93). Фентанил (ОР 2,49, 95% ДИ 1,45-4,27) и морфин (ОР 2,13, 95% ДИ 1,21-3,75) были связаны с возникновением делирия. Риск необъективности был критическим для многих исследований. Обнаружили ассоциацию между болью и возникновением делирия среди взрослых в критическом состоянии. Воздействие морфина или фентанила (но не других обезболивающих препаратов) было связано с повышенным риском возникновения делирия.
Ключевые слова: критическая медицина, анальгетики, боль, оценка боли, делирий
Введение
Боль - один из основных симптомов, с которым сталкиваются пациенты, находящиеся в критическом состоянии [1]. Последствия нелеченной боли включают посттравматическое стрессовое расстройство, депрессию и бессонницу [2]. Делирий - это острое состояние спутанности сознания, дефицита внимания и поведенческой дезорганизации [3]. Делирий часто встречается у больных в критическом состоянии и имеет последствия, включая увеличение продолжительности пребывания в отделении интенсивной терапии (ОРИТ) и когнитивные нарушения [1, 4-6]. Боль считается фактором риска развития делирия, однако данные, подтверждающие это мнение, ограничены [1, 7]. Симптомы делирия лечатся с помощью мультимодального подхода, который включает в себя обезболивание как ключевой принцип [1]. Однако препараты, используемые для лечения боли, связаны с нежелательными эффектами, включая дисфорию или галлюцинации, которые могут имитировать или способствовать развитию делирия [8].
Причинно-следственная связь между болью, обезболивающими препаратами и делирием неясна. Опиоиды, используемые для лечения боли, могут способствовать развитию делирия за счет изменения дофаминовой сигнализации [9, 10]. Duprey et al. сообщили, что на каждые 10 мг морфина вероятность развития делирия увеличивалась на 2,4 % [11]. Pandharipande et al. выявили, что у пациентов хирургических ОРИТ вероятность развития делирия была выше при воздействии фентанила, в то время как у пациентов с травмами вероятность развития делирия была ниже при использовании морфина [12]. В связи с неоднородностью данных о применении опиоидов и делирии неясно, связаны ли конкретные опиоиды или опиоиды как класс с наличием делирия. Для дальнейшего понимания взаимосвязи между болью и/или обезболивающими препаратами и делирием необходимо обобщить имеющуюся литературу. Это поможет врачам лучше понять, как оптимально управлять болью в контексте делирия, а ученым - узнать, на чем следует сосредоточить усилия по раскрытию взаимосвязи боли и делирия. Основной целью было изучить связь между болью (наличие и отсутствие) и делирием, а также между опиоидами (наличие и отсутствие) и делирием.
Методы
Данный систематический обзор и мета-анализ был представлен в соответствии с рекомендациями Preferred Reporting Items for Systematic Reviews and Meta-Analysis [13]. Протокол и поправки были представлены в Международный проспективный регистр систематических обзоров (PROSPERO ID: CRD42022367715) и ранее опубликованы [14].
Определение для факторов воздействия
Подробные определения приведены в онлайн-ресурсе 1. Вкратце, боль классифицировалась как отсутствие клинически значимой боли (цифровая шкала оценки 0-4, поведенческая шкала боли 3-4 или critical care pain observation tool (CPOT) 0-2) или как клинически значимая боль (цифровая шкала оценки ≥ 5, поведенческая шкала боли ≥ 5 или CPOT ≥ 3) [14]. Тяжесть боли определялась в соответствии с оценочным инструментом, использованным в опубликованном исследовании. Опиоиды классифицировались следующим образом: (1) фентанил; (2) морфин; (3) опиоиды, не указанные иначе; и (4) различные опиоиды, включая гидроморфон, метадон, меперидин и петидин. Классификация неопиоидов включала: (1) кетамин; (2) дексмедетомидин; (3) трамадол; (4) ацетаминофен; и (5) нестероидные противовоспалительные средства.
Определения исходов
Делирий определен как присутствующий или отсутствующий; наличие определялось в соответствии с опубликованными исследованиями. Чаще всего для определения делирияиспользовались confusion assessment method in ICU (CAM-ICU) или the intensive care delirium screening checklist (ICDSC). Степень тяжести делирия в данном исследовании указывалась только в том случае, если в исходном исследовании сообщалось об этом результате. Тяжесть определялась в соответствии с оценочным инструментом, использованным в исследовании. Встречаемость делирия определялась как количество всех случаев делирия (числитель) в исследуемой популяции (знаменатель) (подробные определения приведены Online Resource 1 и [14]). Заболеваемость делирием определялась как количество новых случаев делирия (числитель) в исследуемой популяции по отношению к численности исследуемой популяции- человек (знаменатель). Распространенность делирия определялась как количество случаев ранее существовавшего делирия, подсчитанное в исходный период времени исследования (числитель), по отношению к численности исследуемой популяции- человек (знаменатель).
Мы использовали показатель распространенности делирия в связи с неоднородностью исследований, в которых сообщалось о распространенности или заболеваемости делирием.
Стратегия поиска
Поиск проводился по четырем темам: (1) реанимация, (2) делирий, (3) боль и (4) обезболивающие препараты. Стратегия поиска была разработана при содействии медицинского библиотекаря и была рецензирована вторым медицинским библиотекарем с использованием методики Peer Review of Electronic Search Strategies. Поиск проводился в базах данных с момента создания до 15 мая 2023 г., включая: MEDLINE, EMBASE, Cumulative Index to Nursingand Allied Health Literature (CINAHL) и Кокрановский центральный регистр контролируемых исследований (CENTRAL). Авторы провели ручной поиск тезисов пяти крупных конференций по реаниматологии и делирию с января 2020 года по 15 мая 2023 года (подробная информация о конференциях доступна Online Resource 1). Ограничений по языку, дате и стране публикации не было.
Отбор исследований
Для проверки названий и аннотаций использовалась программа Covidence (Covidence systematic review software , Veritas Health Innovation, Мельбурн, Австралия). Программа Endnoteиспользовалась для отслеживания отобранных исследований и исследований для полнотекстового обзора. Скрининг названий (AL, LL, HW), аннотаций (AL, LL, HW) и полнотекстовых (AL, SE, HW) исследований проводился независимо и в двух экземплярах двумя исследователями. На этапе отбора названий и рефератов, если один из рецензентов считал цитату потенциально релевантной, исследование переходило на этап полнотекстового обзора. На этапе полнотекстового обзора разногласия разрешались путем обсуждения или арбитража третьим рецензентом (DJN). Критерии включения и исключения были опубликованы ранее [14]; вкратце, мы включали рандомизированные контролируемые исследования, нерандомизированные квазиэкспериментальные, когортные исследования, исследования «случай-контроль» или их вторичные анализы; пациентов, поступивших в любое ОРИТ; тех, кто мог получить данные о боли или обезболивающих препаратах и о частоте, распространенности или тяжести делирия. Мы исключали неоригинальные исследования; которые сообщали только о делирии при алкогольной абстиненции, делирии при наркотической абстиненции, делирии при тремоне или сообщали о нефармакологических методах в качестве основного метода обезболивания.
Извлечение данных
Данные извлекались независимо и в двух экземплярах с помощью инструмента извлечения данных, созданного в Microsoft Excel для Microsoft 365 MSO Version 2201 (Microsoft, Redmond, USA) (AL, SE, LL, NJ, HW) (подробности опубликованы [14] или в Online Resource 1).
Риск необъективности
Качество включенных исследований оценивалось с помощью Cochrane Collaborative Risk of Bias 2 assessment tool for randomised controlled trials, or Risk of Bias in Non-randomised Studies of Interventions tool for cohort studies [15-17]. Риск необъективности оценивался независимо двумя исследователями, расхождения решались путем обсуждения или третьим исследователем (DJN).
Статистический анализ
Для дихотомических исходов использовалась модель мета-анализа случайных эффектов Hartung-Knapp Sidik-Jonkmann с методом обратной дисперсии для оценки объединенного отношения шансов (ОР) и 95% доверительных интервалов (ДИ) для развития делирия. Выбор этой модели был обусловлен ее повышенной точностью при оценке доверительных интервалов в условиях неоднородности. Мы объединили данные только тех исследований, в которых связь между воздействием и делирием была представлена в виде таблицы 2 × 2, чтобы избежать нарушения статистических предпосылок при объединении точечных оценок, полученных в разных моделях. Для измеренных исходов была проведена модель мета-анализа со случайными эффектами с использованием метода обратной дисперсии для оценки стандартизированной средней разницы и 95%-ного ДИ. Первичным результатом было возникновение делирия, который представлял собой комбинацию распространенного и случайного делирия. В первичном анализе в порядке убывания изучалась связь между: (1) болью (клинически значимой и не клинически значимой) и возникновением делирия; (2) опиоидами и возникновением делирия; (3) неопиоидными обезболивающими препаратами и возникновением делирия. В связи с неоднородностью опиоидов и неопиоидов, использованных в исследованиях, эти классы препаратов анализировались по подтипам, чтобы избежать дополнительного влияния механизма действия, типа и силы связывания с рецепторами. Вторичным результатом была частота делирия. Для оценки выраженности боли мы использовали стандартизированную среднюю разницу, которая представляет собой абсолютную разницу между средним значением боли среди пациентов с делирием и без делирия с учетом вариабельности исследования.
В некоторых исследованиях сообщалось о небольшом количестве событий в группах, подвергшихся и не подвергшихся воздействию. Метод фиксированных эффектов Peto применялся к анализам, в которых в обеих группах произошло пять или менее событий, поскольку он хорошо работает с редкими событиями и не требует коррекции для исследований с нулевым числом событий [18, 19]. Предварительно проведенные анализы представлены в Online Resource 1 (или опубликованы ранее [14]). Статистическая неоднородность оценивалась с помощью статистики I2 [14]. Предвзятость публикаций оценивали с помощью воронкообразных диаграмм и регрессии Egger [20]. Анализ проводился с использованием программы Rstudio.
Анализ чувствительности и анализ подгрупп
Там, где это было возможно, анализ чувствительности проводился с использованием инцидентного делирия в качестве исхода для точного определения связи между воздействием и новыми случаями делирия. Анализ чувствительности был проведен для опиоидов, не указанных в других источниках, и делирия путем исключения исследований (Bose et al. [21] и Kalra et al. [22]), которые в которых были получены большие точечные оценки по методу Peto . Для изучения неоднородности анализа мы провели анализ подгрупп по типу ОРИТ, тяжести заболевания, а также по наличию бреда или болевого синдрома. Для оценки тяжести заболевания мы преобразовали показатель тяжести заболевания в прогнозируемую долю смертности, затем провели дихотомию на прогнозируемую смертность ≥ 50% или < 50% [23-25]. Мы не изучали гетерогенность из-за риска предвзятости, поскольку большинство включенных исследований имели высокий риск предвзятости. Также не удалось изучить гетерогенность по статусу седации, поскольку вариабельность представления данных во включенных исследованиях не позволила провести значимый анализ.
Результаты
Отбор и скрининг исследований
В результате электронного поиска по базам данных и ручного поиска было найдено 8 054 уникальных ссылок, 517 исследований прошли полнотекстовый обзор, и 90 из них были включены в систематический обзор (Fig. 1). Наиболее частой причиной исключения после полнотекстового обзора были данные о боли и делирии, которые не могли быть извлечены в связи друг с другом.

Характеристика включенных исследований
Характеристики включенных исследований представлены в Table 1. Среди 90 включенных исследований (n = 119 230 пациентов) четыре были рандомизированными контролируемыми исследованиями, 48 - проспективными когортными исследованиями и 20 - ретроспективными когортными исследованиями. Исследования проводились преимущественно в США (n = 35, 38,9%), Европе (n = 21, 23,3%) и Азии (n = 15, 16,7%). Исследования были опубликованы в период с 2001 по 2023 год и включали от 12 до 78 364 пациентов. Делирий был выявлен с помощью валидированного инструмента в 86 (95,6%) исследованиях (Table 1). Среди них 66 (73,3%) использовали CAM-ICU и 12 (13,3%) - ICDSC. О выраженности делирия сообщалось в пяти (5,6%) исследованиях. О боли сообщалось в 23 (25,6%) исследованиях; среди них в семи (7,8%) использовался инструмент наблюдения за болью в реанимации, в восьми (8,9%) - цифровая рейтинговая шкала и в пяти (5,6%) - поведенческая шкала боли. Об анальгетиках сообщалось в 89 (98,9%) исследованиях. Полная библиография включенных исследований приведена в Table S1 (Online Resource 2).

Риск необъективности
В Tables S2 и S3 (Online Resource 2) представлены оценки риска необъективности. Для первичного результата «боль и делирий» (n = 16 исследований) 3 исследования были классифицированы как умеренный риск необъективности, 2 - как серьезный риск необъективности и 11 - как критический риск необъективности. Для первичного результата «опиоиды и делирий» (n = 58 исследований) одно исследование было отнесено к категории «некоторые опасения», 12 - к категории «умеренный риск необъективности», 11 - к категории «серьезный риск необъективности» и 34 - к категории «критический риск необъективности».
Первичныq анализ
Боль и делирий
Шестнадцать исследований предоставили данные о боли и делирии. Из-за различий в представлении данных, касающихся боли и делирия, семь исследований (n = 4 848 пациентов) были включены в мета-анализ клинически значимой боли по сравнению с отсутствием клинически значимой боли и возникновением делирия (ранее существовавшие и новые случаи делирия). Наблюдалась тенденция к ассоциации между клинически значимой болью и делирием (ОР 2,49, 95% ДИ 0,98-6,30, p = 0,054, Fig. 2a). Анализ чувствительности среди исследований, в которых сообщалось о новых случаях делирия (инцидентный делирий), выявил связь между клинически значимой болью и инцидентным делирием (ОР 3,70, 95% ДИ 1,73-7,93, p = 0,03, Fig. 2b).

Опиоиды и возникновение делирия
Среди 33 исследований, в которых сообщалось о воздействии фентанила и появления делирия, 12 исследований (n = 3 172 пациента) представили данные в формате 2 × 2, что позволило провести метаанализ. Была выявлена связь между воздействием фентанила и возникновением делирия (ОР 2,49, 95% ДИ 1,45-4,27, р = 0,003, Fig. 3а). Эта связь сохранилась при анализе чувствительности среди исследований, в которых сообщалось о возникновении делирия (ОР 2,21, 95% ДИ 1,69-2,89, p = 0,02, Fig. S1). Аналогичным образом, по результатам пяти исследований (n = 1 000 пациентов), посвященных морфину и делирию, мета-анализ выявил связь между воздействием морфина и возникновением делирия (ОР 2,13, 95% ДИ 1,21-3,75, p = 0,02, рис. 3b). В тех случаях, когда воздействие опиоидов не уточнялось, объединенный анализ 14 исследований (n = 8 943 пациента) выявил ассоциацию между опиоидами и возникновением делирия (ОР 3,01, 95% ДИ 1,23-7,39, p = 0,02, рис. 3c). Однако сила этой ассоциации была уменьшена после исключения двух исследований (Bose et al. [21] и Kalra et al. [22]), которые плохо сходились по методу Peto (ОР 1,98, 95% ДИ 0,89-4,38, p = 0,09, Fig. S2). В трех исследованиях (n = 812 пациентов), в которых изучалась разнородная группа опиоидов (гидроморфон, меперидин, метадон), объединенный анализ не выявил связи с возникновением делирия (ОР 2,62, 95% ДИ 0,51-13,46, p = 0,13, Fig. 3d).

Вторичный анализ
Тяжесть боли и возникновение делирия
Объединенный анализ четырех исследований (n = 4 602 пациента) показал, что умеренная или сильная боль не связана с возникновением делирия (ОР 1,07, 95% ДИ 0,13-8,52, p = 0,92, Fig. 4). Стандартизированная средняя разница - это абсолютная разница (с учетом вариабельности исследования) в баллах боли между пациентами с делирием и без него. Среди трех исследований (n = 1 736 пациентов), в которых приводилась средняя числовая оценка по шкале, объединенный анализ не выявил связи между средней разницей в оценке боли и возникновением делирия (стандартизированная средняя разница 0,09, 95% ДИ -0,50-0,68, p = 0,77, Fig. S3). Среди двух исследований (n = 656 пациентов), в которых сообщалось о средних показателях Critical Care Pain Observation Tool, объединенный анализ показал, что наличие делирия было связано с более высоким баллом боли (стандартизированная средняя разница 0,69, 95% ДИ 0,43-0,95, p < 0,001, Fig. S4).

Неопиоидные обезболивающие препараты и возникновение делирия
В шести исследованиях (n = 1628 пациентов) с адекватными данными о воздействии кетамина и делирии объединенный анализ не выявил связи между кетамином и возникновением делирия (ОР 0,72, 95% ДИ 0,02-22,33, p = 0,82, рис. 3e). Эта связь не изменилась при анализе чувствительности среди исследований, в которых сообщалось о возникновении делирия (Fig.S5). Аналогичным образом, не наблюдалось связи между другими неопиоидными анальгетиками (ацетаминофен, нестероидные противовоспалительные препараты) и возникновением делирия (Fig. 3f, 3g, S6, S7).
Обезболивающие препараты и продолжительность или тяжесть делирия
В двух исследованиях изучались обезболивающие препараты (дексмедетомидин, ацетаминофен) и тяжесть делирия (Table S4). В семи исследованиях изучались обезболивающие препараты (опиоиды, кетамин, ацетаминофен, дексмедетомидин) и продолжительность делирия. Метаанализ не проводился, так как в исследованиях были представлены различные препараты и единицы измерения времени (данные сведены в Table S5 систематического обзора).
Анализ подгрупп, изучающий источники гетерогенности в рамках первичного анализа
Первичный анализ, изучающий воздействие опиоидов и возникновение делирия, был повторен в подгруппах, определенных по: тип ОРИТ, инструмент для лечения делирия и тяжесть заболевания (Online Resource 3). Среди исследований, включавших пациентов с более низкой прогнозируемой смертностью (< 50%), воздействие опиоидов, не указанных в других источниках, было связано с возникновением делирия (ОР 2,34, 95% ДИ 1,85-2,96, p < 0,001, Fig. S8). Анализ подгрупп по фентанилу и делирию показал, что у пациентов, поступивших в ОРИТ смешанного профиля , вероятность возникновения делирия была выше (ОР 2,93, 95% ДИ 1,49-5,75, p = 0,01), в то время как у пациентов, поступивших в специализированные или соматические ОРИТ, она была выше. (Figure S9).
Предвзятость публикаций
По данным воронкообразной диаграммы или регрессии Egger для первичных и вторичных исходов не было обнаружено доказательств предвзятости публикаций (Fig. S10-S23).
Обсуждение
В нашем исследовании обобщены данные 90 исследований, охвативших 119 230 пациентов за 22 года изучения. Это исследование представляет собой всестороннее изучение связи между болью, обезболивающими препаратами и делирием. В соответствии с давними представлениями [1], мы наблюдали тенденцию к ассоциации между клинически значимой болью и уже существующим делирием, а также значительную связь между клинически значимой болью и новым развитием делирия. Мы также отметили, что воздействие морфина на взрослых в критическом состоянии связано с увеличением вероятности возникновения делирия, а фентанила - с увеличением вероятности новых случаев делирия. Воздействие других опиоидов и неопиоидных обезболивающих препаратов не связано с делирием. Объединенные точечные оценки, как правило, имели низкую точность, и лишь немногие исследования имели низкий риск предвзятости, что подчеркивает необходимость получения более надежных данных, оценивающих связь между болью, обезболивающими препаратами и делирием.
Взаимосвязь между болью и делирием является сложной. С биологической точки зрения, боль и делирий потенциально связаны через общие и перекрывающиеся пути [26]. Повышенная реакция на болевые стимулы модулируется через высвобождение хемокинов, цитокинов и глутамата, которые также могут вызывать разрушение гематоэнцефалического барьера [27, 28]. Биомаркеры, связанные с болью и гипералгезией, включают снижение уровня ацетилхолина и повышение уровня провоспалительных цитокинов, таких как интерлейкины-6, -8 и фактор некроза опухоли-α [27, 28]. При делирии "прилипание" лейкоцитов к гематоэнцефалическому барьеру повышает его проницаемость, что приводит к повышению уровня таких медиаторов воспаления, как интерлейкины-6, -8 и фактор некроза опухоли-α [26, 29].
Боль и делирий могут быть связаны между собой повышением уровня провоспалительных цитокинов, снижением уровня ацетилхолина и разрушением гематоэнцефалического барьера [9, 29]. С клинической точки зрения понимание этой взаимосвязи является сложной задачей, поскольку боль очень динамична, и лишь немногие исследования оценивают инцидентный делирий, используют методы, изменяющиеся во времени, или изучают выраженность боли в связи с делирием. Наше исследование предполагает связь между болью и новыми случаями делирия. Однако это противоречит результатам недавних исследований: Duprey et al. установили, что наличие умеренной или сильной боли снижает вероятность развития делирия у взрослых в критическом состоянии (ОР 0,71, 95% ДИ 0,60-0,85, p < 0,01) [11], а Wu et al. обнаружили, что любая степень боли не связана с развитием делирия даже с поправкой на воздействие опиоидов (ОР 0,96, 95% ДИ 0,76-1,21) [30]. И Duprey, и Wu использовали аналитические методы, изменяющиеся во времени.
В отличие от этого, два исследования, включенные в наш мета-анализ, в которых изучались боль и инцидентный делирий, были одноцентровыми проспективными обсервационными когортными исследованиями, в которых использовались модели логистической регрессии прямого отбора, не скорректированные на известные факторы, сдерживающие или изменяющие эффект [31, 32]. Erbay Dalli et al. определили, что оценка по шкале CPOT ≥ 3 ассоциируется с повышенной вероятностью возникновения делирия (ОР 4,70, 95% ДИ 1,05-20,93, p = 0,042) [31]. Среди критически больных пациентов после кардиохирургических операций Kumar et al. выявили, что послеоперационная боль была связана с возникновением делирия (ОР 2,50, 95% ДИ 1,29-4,81, р = 0,0063) [32]. Вариабельность данных о связи между болью и делирием потенциально отражает методологические различия, но оставляет клиницистов в неведении относительно того, как интегрировать лечение боли в широкую стратегию лечения делирия. В дальнейших исследованиях следует использовать строгие методы для анализа изменений во времени, а также изучать тяжесть или траекторию развития боли и делирия, чтобы информировать клиницистов о том, как лучше оптимизировать взаимосвязанное лечение боли и делирия.
Любое исследование взаимосвязи между болью и делирием должно учитывать сложное взаимодействие роли обезболивающих препаратов как потенциальных факторов, сдерживающих или изменяющих эффект. Опиоиды являются краеугольным камнем в лечении критически больных пациентов [1], их используют для анальгезии, а также с учетом их известных побочных эффектов, таких как купирование диспноэ, и в качестве дополнения к седации. Взаимосвязь между опиоидным делирием и его последствиями сложно выяснить из-за динамического дозирования и эффектов, которые могут различаться в зависимости от подтипа опиоида. Опиоиды имеют известные побочные эффекты, включая сонливость и спутанность сознания, которые могут усиливаться и ослабевать в зависимости от пиковых и низких концентраций опиоидов в сыворотке крови. Таким образом, опиоиды могут влиять на инструменты скрининга делирия, которые используют колебания психического статуса, невнимательность, дезориентацию и дезорганизованное мышление в своих параметрах оценки.
Патофизиология опиоидов и делирия может включать изменения дофамина, памяти и циклов сон-бодрствование. В делириозных состояниях высокий и низкий уровни дофамина могут иметь U-образную связь с делирием [29]. Концентрация дофамина повышается в ответ на острую боль. Опиоиды, используемые в качестве лечения, могут еще больше увеличить высвобождение дофамина [10]. Длительное воздействие опиоидов и хроническая боль нарушают сигнализацию дофамина, способствуя развитию делирия [10]. Опиоиды изменяют гиппокампальную синаптическую пластичность и нейрогенез, влияя на аффект и память, что может способствовать развитию делирия [33]. Нарушение цикла сон-бодрствование связано с делирием [26, 29]. Морфин нарушает сон и усиливает бодрствование [34]. Проведенный нами анализ свидетельствует о наличии связи между воздействием фентанила и морфина и возникновением делирия.
Mori et al. сообщили о значительной связи между морфином и распространенным делирием (ОР 2,95, 95% ДИ 1,07-8,12, p = 0,036) [35]. Среди двух исследований, включенных в наш мета-анализ, в которых изучалась экспозиция фентанила и распространенный делирий, Li et al. не обнаружили значимой связи между экспозицией фентанила и делирием (ОР 3,00, 95% ДИ 0,40-22,59, p = 0,29) [36], тогда как Smith et al. сообщили, что опиоиды, в основном фентанил, были связаны с развитием делирия (ОР опиоидов 24, 95% ДИ 16-27, p < 0,001) [37]. Подгрупповой анализ связи фентанила с делирием показал, что у пациентов, поступивших в смешанные ОРИТ, вероятность развития делирия была выше. Присутствие хирургических пациентов в общей популяции ОРИТ может повысить значимость этой взаимосвязи; предыдущие исследования показали, что фентанил повышает вероятность делирия среди хирургических пациентов [12].
В нашем обзоре исследования, в которых изучались опиоиды, отличные от фентанила и морфина (например, гидроморфон, метадон, меперидин), или изучались неопиоидные обезболивающие препараты, не выявили связи с делирием. Возможно, эти сравнения были недостаточно эффективными. Зависимость между дозой и реакцией помогла бы лучше понять связь между обезболивающими препаратами и делирием. Однако лишь немногие исследования изучали дозировку обезболивающих препаратов и делирий, а вариабельность доз (суточная доза или кумулятивная доза или доза, основанная на весе) затрудняет проведение объединенного анализа. Smith et al. сообщили о более высоких дозах фентанила и морфина у тех, у кого развился делирий, по сравнению с теми, у кого его не было [37].
Используя методы изменения во времени, Duprey et al. определили, что вероятность развития делирия возрастала с увеличением дозы синтетических опиоидов и морфина [11]. С клинической точки зрения, относительное постоянство взаимосвязи между фентанилом и морфином и развитием делирия предполагает потенциал для улучшения лечения делирия с помощью стратегий обезболивания, которые направленных на минимизацию или отказ от применения опиоидов, таких как фентанил или морфин. Будущие исследования должны быть направлены на изучение случайного делирия, обеспечение того, чтобы воздействие опиоидов предшествовало развитию делирия, использование методов анализа, изменяющихся во времени, для контроля известных факторов, четко указывающих тип опиоида при воздействии, и сообщение о дозе обезболивающего препарата.
Сильные стороны и ограничения
Данное исследование следует интерпретировать в контексте его сильных и слабых сторон. Мы использовали строгие методы, включая рецензируемую стратегию поиска и широкие критерии включения исследований, которые не ограничивались по языку, размеру выборки, инструментам для лечения делирия или популяциям пациентов ОРИТ. Хотя это внесло клиническую и статистическую неоднородность в наш объединенный анализ, полученная в результате когорта статей представляет собой современный обзор современных научных исследований по этой важной теме. К основным ограничениям данной работы относятся ограниченное количество исследований в рамках более крупного систематического обзора, которые можно было включить в мета-анализ, и небольшое количество включенных исследований, которые имели низкий риск предвзятости. Из-за неоднородности данных о боли, обезболивающих препаратах и делирии объединенный анализ этих взаимосвязей был затруднен, многие исследования были исключены из мета-анализа из-за отсутствия необходимых данных.
С точки зрения определения и для облегчения совместного анализа мы представляли боль и делирий как дихотомии (наличие или отсутствие). Следствием такого решения является потенциальное чрезмерное упрощение этой сложной взаимосвязи за счет предположения о едином эффекте при широком воздействии и/или тяжести исхода. Чтобы решить эту проблему, мы отдельно рассматривали тяжесть боли и делирия. Во многих исследованиях также не выделялся случайный делирий. Поэтому наше определение возникновения делирия может переоценить ассоциацию, поскольку у некоторых пациентов делирий мог быть исходно. Мы рассмотрели эту потенциальную переоценку, проведя анализ чувствительности среди исследований, включавших данные об инцидентах. Что касается возникновения делирия, то многие включенные исследования имели высокий риск предвзятости из-за неадекватного контроля сопутствующих факторов.
Это может преувеличить связь между болью или обезболивающими препаратами и делирием. Среди исследований, включавших данные об инцидентах, одно было с низким риском необъективности, одно - с некоторыми опасениями, а четыре - с серьезным риском необъективности. В исследованиях часто не учитывались сопутствующие факторы или модификаторы эффекта, такие как седация, не учитывались изменяющиеся во времени сопутствующие факторы или множественные подходы к оценки интенсивности боли и/или делирия, а также не всегда обеспечивалась последовательная связь между воздействием и исходом.
Выводы
В соответствии с давними представлениями, в нашем систематическом обзоре и мета-анализе была выявлена связь между болью и развитием делирия. Мы также отметили, что фентанил и морфин связаны с возникновением делирия. Мы не обнаружили связи между другими опиоидами и неопиоидными обезболивающими препаратами и делирием. Многие включенные исследования имели высокий риск необъективности из-за неадекватного контроля сопутствующих факторов. Чтобы глубже понять взаимосвязь между болью, обезболивающими препаратами и делирием, в будущих исследованиях необходимо использовать надежные методы, которые учитывали бы динамическую, изменяющуюся во времени природу потенциально многократно запутанной взаимосвязи. Наблюдаемая связь между болью и делирием в сочетании с устойчивой связью между фентанилом и морфином и развитием делирия позволяет предположить, что в ожидании дальнейших исследований один из компонентов плана лечения делирия должен включать оптимальное обезболивание с помощью стратегии, направленной на минимизацию или отказ от морфина и фентанила.
Дополнительные данные исследования (Supplementary)
References
1. Devlin JW, Skrobik Y, Gйlinas C, Needham DM, Slooter AJC, Pandharipande
PP, Watson PL, Weinhouse GL, Nunnally ME, Rochwerg B, Balas MC, van den Boogaard M, Bosma KJ, Brummel NE, Chanques G, Denehy L, Drouot X, Fraser GL, Harris JE, Joffe AM, Kho ME, Kress JP, Lanphere JA, McKinley S, Neufeld KJ, Pisani MA, Payen J-F, Pun BT, Puntillo KA, Riker RR, Robinson BRH, Shehabi Y, Szumita PM, Winkelman C, Centofanti JE, Price C, Nikayin S, Misak CJ, Flood PD, Kiedrowski K, Alhazzani W (2018) Clinical practice guidelines for the prevention and management of pain, agitation/ sedation, delirium, immobility, and sleep disruption in adult patients in the ICU. Crit Care Med 46:e825–e873
2. Martyn JAJ, Mao J, Bittner EA (2019) Opioid tolerance in critical illness. N
Engl J Med 380:365–378
3. (2013) Diagnostic and statistical manual of mental disorders : DSM-5™.
American Psychiatric Publishing, a division of American Psychiatric Association,
Washington, DC
4. Krewulak KD, Stelfox HT, Leigh JP, Wesley Ely E, Fiest KM (2018) Incidence
and prevalence of delirium subtypes in an adult ICU: A systematic review and meta-analysis. Crit Care Med 46:2029–2035
5. Krewulak KD, Stelfox HT, Ely EW, Fiest KM (2020) Risk factors and outcomes
among delirium subtypes in adult ICUs: a systematic review. J Crit Care 56:257–264
6. Goldberg TE, Chen C, Wang Y, Jung E, Swanson A, Ing C, Garcia PS,Whittington RA, Moitra V (2020) Association of delirium with long-term
cognitive decline: a meta-analysis. JAMA Neurol 77:1373–1381
7. Barr J, Fraser GL, Puntillo K, Ely EW, Gйlinas C, Dasta JF, Davidson JE,
Devlin JW, Kress JP, Joffe AM, Coursin DB, Herr DL, Tung A, Robinson BRH,
Fontaine DK, Ramsay MA, Riker RR, Sessler CN, Pun B, Skrobik Y, Jaeschke R
(2013) Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Crit Care Med 41:263–306
8. Rang HP, Dale MM (2012) Rang and dale’s pharmacology. Churchill Livingstone,Edinburgh
9. Khan BA, Perkins AJ, Campbell NL, Gao S, Farber MO, Wang S, Khan SH, Zarzaur BL, Boustani MA (2019) Pharmacological management of delirium in the intensive care unit: a randomized pragmatic clinical trial. J Am Geriatr Soc 67:1057–1065
10. Taylor AMW, Becker S, Schweinhardt P, Cahill C (2016) Mesolimbic dopamine signaling in acute and chronic pain: implications for motivation,
analgesia, and addiction. Pain 157:1194–1198
11. Duprey MS, Dijkstra-Kersten SMA, Zaal IJ, Briesacher BA, Saczynski JS,
Griffith JL, Devlin JW, Slooter AJC (2021) Opioid use increases the risk of
delirium in critically ill adults independently of pain. Am J Respir Crit Care
Med 204:566–572
12. Pandharipande P, Cotton BA, Shintani A, Thompson J, Pun BT, Morris JA
Jr, Dittus R, Ely EW (2008) Prevalence and risk factors for development of delirium in surgical and trauma intensive care unit patients. J Trauma 65:34–41
13. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD,
Shamseer L, Tetzlaff JM, Akl EA, Brennan SE, Chou R, Glanville J, Grimshaw
JM, Hrуbjartsson A, Lalu MM, Li T, Loder EW, Mayo-Wilson E, McDonald S, McGuinness LA, Stewart LA, Thomas J, Tricco AC, Welch VA, Whiting P, Moher D (2021) The PRISMA 2020 statement: An updated guideline for reporting systematic reviews. BMJ 372:n71–n79
14. Leong AY, Burry L, Fiest KM, Doig CJ, Niven DJ (2024) Does pain optimisation impact delirium outcomes in critically ill patients? A systematic
review and meta-analysis protocol. BMJ Open 14:e078395
15. Sterne JAC, Hernan MA, McAleenan A, Reeves BC, Higgins JPT (2021)
Assessing risk of bias in a non-randomized study. In: Higgins JPT, Thomas J, Chandler J, Cumpston m, Li T, Page MJ, Welch VA (eds) Cochrane Handbook
for Systematic Reviews of Interventions. Cochrane
16. Higgins JPT, Altman DG, Gшtzsche PC, Jьni P, Moher D, Oxman AD, Savović J, Schulz KF, Weeks L, Sterne JAC, (2011) The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. British Medical Journal 343
17. Sterne JAC, Savović J, Page MJ, Elbers RG, Blencowe NS, Boutron I, Cates
CJ, Cheng HY, Corbett MS, Eldridge SM, Emberson JR, Hernбn MA, Hopewell S, Hrуbjartsson A, Junqueira DR, Jьni P, Kirkham JJ, Lasserson T, Li T, McAleenan A, Reeves BC, Shepperd S, Shrier I, Stewart LA, Tilling K, White IR, Whiting PF, Higgins JPT (2019) RoB 2: A revised tool for assessing risk of bias in randomised trials. BMJ 366:l4898. https:// doi. org/ 10. 1136/bmj. l4898
18. Schwarzer G, Carpenter JR, Rucker G (2015) Meta-Analysis with R. In: Editor
(ed) (eds) Book Meta-Analysis with R. Springer International Publishing AG Switzerland, City, pp.
19. Cochrane (2023) Cochrane Handbook for Systematic Reviews of Interventions.
In: Editor (ed) (eds) Book Cochrane Handbook for Systematic Reviews of Interventions. Cochrane, City, pp.
20. Egger M, Smith GD, Minder C (1997) Bias in meta-analysis detected by a
simple, graphical test. BMJ 315:629–634
21. Bose S, Kelly L, Shahn Z, Novack L, Banner-Goodspeed V, Subramaniam B
(2022) Sedative polypharmacy mediates the effect of mechanical ventilation on delirium in critically ill COVID-19 patients: a retrospective cohort study. Acta Anaesthesiol Scand 66:1099–1106
22. Kalra SS, Jaber J, Alzghoul BN, Hyde R, Parikh S, Urbine D, Reddy R (2022)
Pre-existing psychiatric illness is associated with an increased risk of delirium in patients with acute respiratory distress syndrome. J Intensive Care Med 37:647–654
23. Le Gall J-R, Lemeshow S, Saulnier F (1993) A new Simplified Acute Physiology Score (SAPS II) based on a European/North American Multicenter
Study. JAMA 270:2957–2963
24. Vincent JL, Moreno R, Takala J, Willatts S, De Mendonзa A, Bruining H,
Reinhart CK, Suter PM, Thijs LG (1996) The SOFA (Sepsis-related Organ Failure Assessment) score to describe organ dysfunction/failure. On behalf of the Working Group on Sepsis-Related Problems of the European Society of Intensive Care Medicine. Intensive Care Med 22:707–710
25. Knaus WA, Draper EA, Wagner DP, Zimmerman JE (1985) APACHE II: a
severity of disease classification system. Crit Care Med 13:818–829
26. Maldonado JR (2018) Delirium pathophysiology: an updated hypothesis
of the etiology of acute brain failure. Int J Geriatr Psychiatry 33:1428–1457
27. Sampson EL, West E, Fischer T (2020) Pain and delirium: mechanisms,
assessment, and management. European Geriatric Medicine 11:45–52
28. DeVon HA, Piano MR, Rosenfeld AG, Hoppensteadt DA (2014) The association of pain with protein inflammatory biomarkers: a review of the literature. Nurs Res 63:51–62
29. Gunther ML, Morandi A, Ely EW (2008) Pathophysiology of delirium in the
intensive care unit. Crit Care Clin 24:45–65
30. Wu TT, Vernooij LM, Duprey MS, Zaal IJ, Gйlinas C, Devlin JW, Slooter AJC
(2023) Relationship between pain and delirium in critically ill adults. Crit Care Explor 5:e1012
31. Erbay Dalli O, Kelebek Girgin N, Kahveci F (2022) Incidence, characteristics
and risk factors of delirium in the intensive care unit: an observational study. J Clin Nurs 32(1–2):96–105
32. Kumar AK, Jayant A, Arya VK, Magoon R, Sharma R (2017) Delirium after
cardiac surgery: a pilot study from a single tertiary referral center. Ann Card Anaesth 20:76–82
33. Kibaly C, Xu C, Cahill CM, Evans CJ, Law P-Y (2019) Non-nociceptive roles
of opioids in the CNS: opioids’ effects on neurogenesis, learning, memory and affect. Nat Rev Neurosci 20:5–18
34. Eacret D, Manduchi E, Noreck J, Tyner E, Fenik P, Dunn AD, Schug J, Veasey
SC, Blendy JA (2023) Mu-opioid receptor-expressing neurons in the paraventricular thalamus modulate chronic morphine-induced wake alterations. Transl Psychiatry 13:78
35. Mori S, Takeda JRT, Carrara FSA, Cohrs CR, Zanei SSV, Whitaker IY (2016)
Incidence and factors related to delirium in an intensive care unit. Rev Esc Enferm USP 50:587–593
36. Li X, Zhang L, Gong F, Ai Y (2020) Incidence and risk factors for delirium
in older patients following intensive care unit admission: a prospective observational study. J Nurs Res JNR 28:e101
37. Smith RJ, Lachner C, Singh VP, Cartin-Ceba R (2022) Intensive care unit
delirium in patients with severe COVID-19: A prospective observational cohort study. Int J Crit Illn Inj Sci 12:61–69
[DETAIL_PICTURE] =>
[DATE_ACTIVE_FROM] => 07.05.2025 00:01:00
[ACTIVE_FROM] => 07.05.2025 00:01:00
[SHOW_COUNTER] => 353
)
[PROPERTIES] => Array
(
[KEYWORDS] => Array
(
[ID] => 1
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 100
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 102
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 831045
[VALUE] => Боль, анальгезия, делирий, критические состояния, интенсивная терапия, исследование
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Боль, анальгезия, делирий, критические состояния, интенсивная терапия, исследование
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[DESCRIPTION] => Array
(
[ID] => 64
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Описание
[ACTIVE] => Y
[SORT] => 200
[CODE] => DESCRIPTION
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Описание
[~DEFAULT_VALUE] =>
)
[BROWSER_TITLE] => Array
(
[ID] => 9
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Заголовок окна браузера
[ACTIVE] => Y
[SORT] => 300
[CODE] => BROWSER_TITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => content-articles-property-browser_title
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => Y
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 831046
[VALUE] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[~DESCRIPTION] =>
[~NAME] => Заголовок окна браузера
[~DEFAULT_VALUE] =>
)
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 831069
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
)
[vote_count] => Array
(
[ID] => 100
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Количество проголосовавших
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_count
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество проголосовавших
[~DEFAULT_VALUE] =>
)
[vote_sum] => Array
(
[ID] => 101
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Сумма оценок
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_sum
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Сумма оценок
[~DEFAULT_VALUE] =>
)
[rating] => Array
(
[ID] => 102
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Рейтинг
[ACTIVE] => Y
[SORT] => 500
[CODE] => rating
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Рейтинг
[~DEFAULT_VALUE] =>
)
[FAVORITES] => Array
(
[ID] => 148
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Избранное
[ACTIVE] => Y
[SORT] => 500
[CODE] => FAVORITES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Избранное
[~DEFAULT_VALUE] =>
)
[LIKE] => Array
(
[ID] => 153
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Понравилось
[ACTIVE] => Y
[SORT] => 500
[CODE] => LIKE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Понравилось
[~DEFAULT_VALUE] =>
)
[SUBTITLE] => Array
(
[ID] => 93
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Подзаголовок
[ACTIVE] => Y
[SORT] => 501
[CODE] => SUBTITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Подзаголовок
[~DEFAULT_VALUE] =>
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 831053
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
)
[QUOTE] => Array
(
[ID] => 95
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Цитата
[ACTIVE] => Y
[SORT] => 503
[CODE] => QUOTE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Цитата
[~DEFAULT_VALUE] =>
)
[SLIDER] => Array
(
[ID] => 98
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Слайдер
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер
[~DEFAULT_VALUE] =>
)
[SLIDER_DESC] => Array
(
[ID] => 99
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Слайдер описание
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER_DESC
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер описание
[~DEFAULT_VALUE] =>
)
[INFO_SOURCES] => Array
(
[ID] => 96
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Информация и источники
[ACTIVE] => Y
[SORT] => 504
[CODE] => INFO_SOURCES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Информация и источники
[~DEFAULT_VALUE] =>
)
[MATERIALS] => Array
(
[ID] => 97
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Материалы к статье
[ACTIVE] => Y
[SORT] => 505
[CODE] => MATERIALS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Материалы к статье
[~DEFAULT_VALUE] =>
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 831048
[1] => 831049
[2] => 831050
[3] => 831051
[4] => 831052
)
[VALUE] => Array
(
[0] => intensivnayaterapiya
[1] => sepsis
[2] => kriticheskiesostoyaniya
[3] => statia
[4] => issledovanie
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => intensivnayaterapiya
[1] => sepsis
[2] => kriticheskiesostoyaniya
[3] => statia
[4] => issledovanie
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
)
[COMMENTS_COUNT] => Array
(
[ID] => 103
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Количество комментариев
[ACTIVE] => Y
[SORT] => 5010
[CODE] => COMMENTS_COUNT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество комментариев
[~DEFAULT_VALUE] =>
)
[FB2] => Array
(
[ID] => 173
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => FB2
[ACTIVE] => Y
[SORT] => 5020
[CODE] => FB2
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] => fb2
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => FB2
[~DEFAULT_VALUE] =>
)
[ADD_DATES] => Array
(
[ID] => 207
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Дата добавления материалов
[ACTIVE] => Y
[SORT] => 5030
[CODE] => ADD_DATES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => Date
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата добавления материалов
[~DEFAULT_VALUE] =>
)
[LENGHT] =>
[VIDEO_PREVIEW] =>
[VIDEO_FULL] =>
)
[DISPLAY_PROPERTIES] => Array
(
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 831069
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => да
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 831053
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => [8] (info@sepsisforum.ru) Команда Сепсис Форума
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 831048
[1] => 831049
[2] => 831050
[3] => 831051
[4] => 831052
)
[VALUE] => Array
(
[0] => intensivnayaterapiya
[1] => sepsis
[2] => kriticheskiesostoyaniya
[3] => statia
[4] => issledovanie
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => intensivnayaterapiya
[1] => sepsis
[2] => kriticheskiesostoyaniya
[3] => statia
[4] => issledovanie
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => Array
(
[0] => Интенсивная терапия
[1] => Сепсис
[2] => Критические состояния
[3] => Статья
[4] => Исследование
)
)
)
[IBLOCK] => Array
(
[ID] => 2
[~ID] => 2
[TIMESTAMP_X] => 13.08.2025 01:26:24
[~TIMESTAMP_X] => 13.08.2025 01:26:24
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[LID] => s1
[~LID] => s1
[CODE] => articles
[~CODE] => articles
[API_CODE] =>
[~API_CODE] =>
[NAME] => Статьи
[~NAME] => Статьи
[ACTIVE] => Y
[~ACTIVE] => Y
[SORT] => 200
[~SORT] => 200
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[~DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[~SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[CANONICAL_PAGE_URL] =>
[~CANONICAL_PAGE_URL] =>
[PICTURE] =>
[~PICTURE] =>
[DESCRIPTION] => Статьи
[~DESCRIPTION] => Статьи
[DESCRIPTION_TYPE] => html
[~DESCRIPTION_TYPE] => html
[RSS_TTL] => 24
[~RSS_TTL] => 24
[RSS_ACTIVE] => Y
[~RSS_ACTIVE] => Y
[RSS_FILE_ACTIVE] => N
[~RSS_FILE_ACTIVE] => N
[RSS_FILE_LIMIT] =>
[~RSS_FILE_LIMIT] =>
[RSS_FILE_DAYS] =>
[~RSS_FILE_DAYS] =>
[RSS_YANDEX_ACTIVE] => N
[~RSS_YANDEX_ACTIVE] => N
[XML_ID] => content-articles
[~XML_ID] => content-articles
[TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[~TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[INDEX_ELEMENT] => Y
[~INDEX_ELEMENT] => Y
[INDEX_SECTION] => Y
[~INDEX_SECTION] => Y
[WORKFLOW] => N
[~WORKFLOW] => N
[BIZPROC] => N
[~BIZPROC] => N
[SECTION_CHOOSER] => L
[~SECTION_CHOOSER] => L
[LIST_MODE] =>
[~LIST_MODE] =>
[RIGHTS_MODE] => S
[~RIGHTS_MODE] => S
[SECTION_PROPERTY] => Y
[~SECTION_PROPERTY] => Y
[PROPERTY_INDEX] => I
[~PROPERTY_INDEX] => I
[VERSION] => 1
[~VERSION] => 1
[LAST_CONV_ELEMENT] => 0
[~LAST_CONV_ELEMENT] => 0
[SOCNET_GROUP_ID] =>
[~SOCNET_GROUP_ID] =>
[EDIT_FILE_BEFORE] =>
[~EDIT_FILE_BEFORE] =>
[EDIT_FILE_AFTER] =>
[~EDIT_FILE_AFTER] =>
[SECTIONS_NAME] => Разделы статей
[~SECTIONS_NAME] => Разделы статей
[SECTION_NAME] => Раздел статей
[~SECTION_NAME] => Раздел статей
[ELEMENTS_NAME] => Статьи
[~ELEMENTS_NAME] => Статьи
[ELEMENT_NAME] => Статья
[~ELEMENT_NAME] => Статья
[REST_ON] => N
[~REST_ON] => N
[FULLTEXT_INDEX] => N
[~FULLTEXT_INDEX] => N
[EXTERNAL_ID] => content-articles
[~EXTERNAL_ID] => content-articles
[LANG_DIR] => /
[~LANG_DIR] => /
[SERVER_NAME] => sepsisforum.ru
[~SERVER_NAME] => sepsisforum.ru
)
[SECTION] => Array
(
[PATH] => Array
(
)
)
[SECTION_URL] =>
[META_TAGS] => Array
(
[TITLE] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[BROWSER_TITLE] => Связь между болью, анальгезией и делирием у взрослых в критическом состоянии: систематический обзор и метаанализ
[KEYWORDS] => Боль, анальгезия, делирий, критические состояния, интенсивная терапия, исследование
[DESCRIPTION] =>
)
)




