Сепсис в сочетании с острым инфарктом миокарда и кардиогенным шоком: 15-летняя история наблюдений
Critical Care Explorations,
DOI: 10.1097/CCE.0000000000000637
Оригинальное клиническое сообщение
Сепсис в сочетании с острым инфарктом миокарда и кардиогенным шоком: 15-летняя история наблюдений, тренды, менеджмент и исходы.
Перевод оригинальной статьи «Concomitant Sepsis Diagnoses in Acute Myocardial Infarction-Cardiogenic Shock: 15-Year National Temporal Trends, Management, and Outcomes»
Авторы: Jacob C. Jentzer, Anusha G. Bhat, Sri Harsha Patlolla, Shashank S. Sinha, P. Elliott Miller, Patrick R. Lawler, Sean van Diepen, Ashish K. Khanna, David X. Zhao, Saraschandra Vallabhajosyula
Department of Cardiovascular Medicine, Mayo Clinic,Rochester, MN.
Division of Cardiovascular Medicine, Department Medicine, University of Maryland, Baltimore, MD
Department of Cardiovascular Surgery, Mayo Clinic, Rochester, MN.
Inova Heart and Vascular Institute, Inova Fairfax Medical Center, Falls Church, VA.
Division of Cardiovascular Medicine, Department of Medicine, Yale University School of Medicine, New Haven, CT.
Peter Munk Cardiac Centre, University Health Network, Toronto, ON, Canada.
Department of Critical Care and Division of Cardiology, Department of Medicine, University of Alberta, Edmonton, AB, Canada.
Section on Critical Care Medicine, Department of Anesthesiology, Wake Forest University School of Medicine, Winston Salem, NC.
Outcomes Research Consortium, Cleveland, OH.
Section of Cardiovascular Medicine, Department of Medicine, Wake Forest University School of Medicine, Winston Salem, NC.
Key words: acute myocardial infarction; cardiogenic shock; circulatory shock; critical care cardiology; sepsis
Ключевые слова: острый инфаркт миокарда, кардиогенный шок, циркуляторный шок, критические состояния в кардиологии, сепсис
Введение
Кардиогенный шок (КШ) является лидирующей причиной смерти у пациентов с острым инфарктом миокарда (ОИМ), а распространенность КШ имеет тенденцию к увеличению [1—3]. Пациенты, у которых течение ОИМ осложнилось развитием КШ (ОИМ-КШ) имеют очень высокую краткосрочную летальность (до 35—50%), при этом вмешательств, которые бы могли улучшить выживаемость, за последние два десятилетия не появилось [4]. Пациенты с ОИМ-КШ во все время госпитализации находятся под постоянным риском развития осложнений, к которым можно отнести инфекции и органное повреждение [4]. Среди пациентов с КШ можно выделить подгруппу со смешанным кардиогенным-вазодиляторным шоком, у которых риск неблагоприятного исхода повышается многократно [5].
Пациенты с ОИМ-КШ имеют риск развития патологической вазодилятации, что связано с фенотипом ответа на воспаление [6]. Системное воспаление постоянно сопровождает ОИМ-КШ, что связано как с самим ОИМ, который является триггером системного воспаления, так и с ответом на гипоперфузию органов, что обусловлено ОИМ, а также с инфекцией [7]. Исследование SHOCK («SHould we emergently revascularize Occluded Coronaries for Cardiogenic shocK») показало, что примерно у 20% пациентов с ОИМ-КШ развивается инфекция/подозрение на инфекцию [8]. Пациенты с КШ и сопутствующим сепсисом имеют повышенный риск неблагоприятного исхода, чего следует ожидать, учитывая то, что сам по себе сепсис является угрожающим жизни состоянием, способным вызвать полиорганную недостаточность [9, 10]. Но несмотря на все вышесказанное, каких-либо больших исследований, в которых бы изучалась эпидемиология и/или клинические исходы, ассоциированные с сепсисом у пациентов с ОИМ-КШ, до настоящего времени не было.
Принимая во внимание такой пробел в наших знаниях, мы решили оценить временные тренды, менеджмент, стоимость и клинические исходы при сочетании сепсиса и ОИМ-КШ. Мы выдвинули гипотезу, что увеличение распространённости сепсиса при ОИМ-КШ будет сопровождаться более высокой частотой использования интенсивной терапии, механических способов поддержки циркуляции и более высокой частотой развития полиорганной недостаточности.
Материалы и методы
Популяция исследования, переменные и исходы
The National (Nationwide) Inpatient Sample(NIS) — база данных и программное обеспечение, созданное в рамках отраслевого партнерства между федеральным штатом и Агентством медицинских исследований и качества (спонсор) для проекта учета затрат при использовании медицинских услуг (HCUP). HCUPNIS является крупнейшей базой данных о пребывании/оплате в стационаре в Соединенных Штатах и включает данные о выписке примерно 20% стратифицированной выборки больниц США [11].
База данных содержит информацию из всех штатов, участвующих в программе HCUP, и охватывает более 97% населения США. Обезличенная информация о пациенте включает в себя демографические данные, основной плательщик, сопутствующие заболевания, основной диагноз, до 29 вторичных диагнозов и процедурные диагнозы. Утверждение Институционального наблюдательного совета не требовалось из-за не идентифицированного характера общедоступной базы данных. Мы определили наблюдения как «поступления», а не рассматривали их как отдельных пациентов, ограничили детали исследования стационарными переменными, поскольку HCUP-NIS не включает подтвержденную информацию об амбулаторных пациентах, и использовали административные коды, ранее проверенные и использовавшиеся для аналогичных исследований.
Мы использовали данные HCUP-NIS, начиная с января 2000 года по декабрь 2014 года, идентифицируя взрослых (более 18 лет) пациентов с ОИМ (основной диагноз (международная классификация болезней, 9 редакция) [4, 12, 13]. Административные коды ОИМ имели высокую чувствительность (98%), специфичность (91%), ценность положительного прогноза (95%) и отрицательного прогноза (97%). Осложнение основного диагноза в виде КШ идентифицировалось по коду ICD-9-CM 785.51, административные коды КШ имели высокую положительную прогностическую ценность (> 90%) и специфичность (> 95%), но чувствительность была ниже (> 50%) [14, 15]. Несмотря на то, что в литературе существует несколько систематических методов выявления сепсиса, большинство из этих алгоритмов были созданы до интеграции кодов МКБ сепсиса и септического шока. Кроме того, поскольку КШ сам по себе способствует органной дисфункции, использование комбинации сепсиса с органной дисфункцией снизит специфичность нашей когорты. Поэтому мы определяли диагноз сепсиса, используя коды МКБ-9 для тяжелого сепсиса (Дополнительная таблица 1, http:// links.lww.com/CCX/A912) и септического шока (ICD9-CM 785.52). Эти коды применялись в ходе многочисленных предыдущих исследований [16–20] и, как сообщается, имеют чувствительность ~ 50 % и специфичность 99 % [21]. Следует отметить, что идентификацию сепсиса следует экстраполировать как «диагнозы» сепсиса, поскольку изменения в идентификации могут быть связаны с более широким распознаванием сущности болезни. Сопутствующие заболевания были выявлены с использованием индекса сопутствующих заболеваний Чарлсона в модификации Deyo [22]. Информация, связанная с полом, расой, а также сведения о больнице, сопутствующих заболеваниях, кардиальных процедурах и использование других, внесердечных органов, была определена с помощью методологии нашей группы (Дополнительная таблица 2, http://links.lww.com/CCX/A912). ) (4, 12, 13, 23–29). Внесердечная органная недостаточность определялась с использованием нашего определения, а полиорганная недостаточность определялась как поражение более одной системы органов, кроме сердечно-сосудистой недостаточности [4].
Основными клиническими исходами, представляющими интерес, стали временные тенденции в распространенности, характеристиках и госпитальной летальности пациентов с ОИМ-КШ в сочетании с сепсисом. Интересующими вторичными исходами стали временные тенденции в отношении недостаточности одного органа, полиорганной недостаточности, а также использование коронарной ангиографии (КА), чрескожного коронарного вмешательства (ЧКВ), катетера легочной артерии (КЛА), механических методов поддержки органов (ММПО), затрат на госпитализацию, продолжительность пребывания пациента в стационаре, распределение выделений в когортах с сепсисом и без него при ОИМ-КШ.
Статистический анализ
Для статистического анализа использовались полученные в HCUP статистические веса при выписке, что помогло в создании оценок на национальном уровне [11]. Используя веса тренда, полученные с помощью HCUP-NIS, мы повторно взвесили выборки с 2000 по 2011 год, чтобы скорректировать дизайн HCUP-NIS 2012 года [30]. Для сравнения категориальных и непрерывных переменных использовались однофакторный дисперсионный анализ и двусторонний t-критерий, соответственно. После субстратификации по наличию сепсиса и типу ОИМ были нанесены временные тенденции распространенности сепсиса и использования КА, ЧКВ, ММПО, КЛА, острого гемодиализа и инвазивной и не-инвазивной ИВЛ. Мы оценили временные тенденции распространенности одиночной и полиорганной недостаточности с 2000 по 2014 год. Был проведен однофакторный анализ тенденций и исходов, представленный в виде отношения шансов (ОШ) с 95% ДИ. Многопараметрическая логистическая регрессия была выполнена для анализа тенденций во времени (по сравнению с 2000 годом в качестве референса), и ОШ с 95% ДИ были рассчитаны для каждого года с поправкой на возраст, пол, расу, статус дохода, сопутствующие заболевания, основного плательщика, характеристики больницы, острую органную недостаточность, остановку сердца, КА, ЧКВ, аортокоронарное шунтирование, КЛА, ММПО, инвазивная и не-инвазивная механическая вентиляция легких и острый гемодиализ. Для многомерного моделирования был проведен регрессионный анализ с целенаправленным отбором статистически и клинически значимых переменных (либеральный порог p < 0,20 в одномерном анализе). Анализ чувствительности был проведен для госпитализаций с сепсисом по сравнению с септическим шоком и скорректирован с учетом возраста, пола, расы, страховки, местоположения госпиталя, почтового индекса, региона, типа ОИМ, сепсиса, сопутствующих заболеваний, органной недостаточности, острой почечной недостаточности и использования инвазивных методов лечения. кардиологические процедуры. Двустороннее значение p менее 0,05 считалось статистически значимым. Статистический анализ был проведён с помощью SPSS Version 28.0 (IBM Corp, Armonk NY).
Результаты
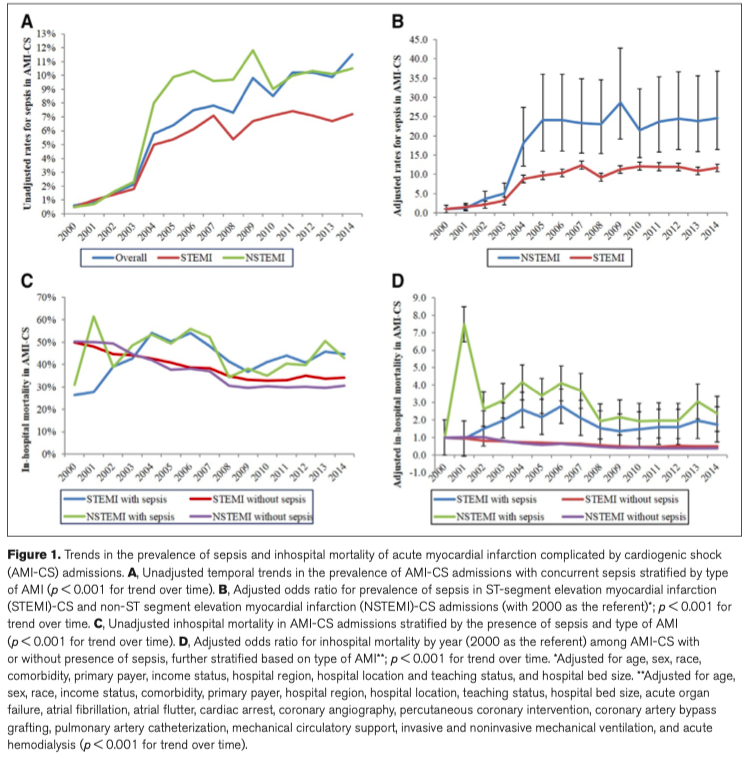
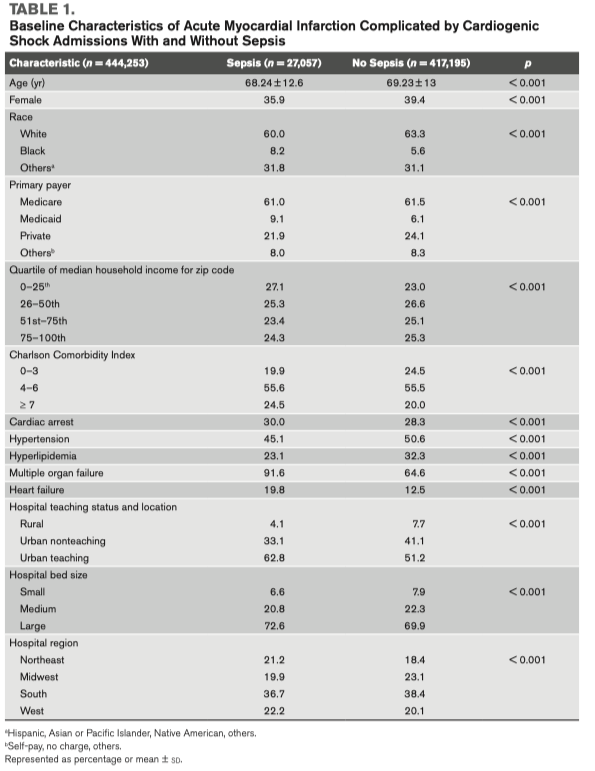
Во время периода исследования между январем 2000 и декабрем 2014 года, нам удалось выявить 444 253 поступления с ОИМ-КШ, из которых в 27 957 (6.1%) развился сепсис, включая 13 066 (2.9%), отмеченных как септический шок. Среди всех ОИМ, поступивших с сепсисом, инфаркт миокарда с подъемом сегмента ST (ST-segment elevation myocardial infarction [STEMI]) диагностировался в 55.7% случаев, а инфаркт миокарда без подъема ST диагностировался в 44.3%. Временные тренды показали устойчивое увеличение распространенности сепсиса, с большей частотой при NSTEMI с кардиогенным шоком (Рис. 1, А и В). Пациенты, поступившие с сепсисом, были моложе, чаще белые мужчины с выраженной коморбидностью (p < 0.001) (Таблица 1).
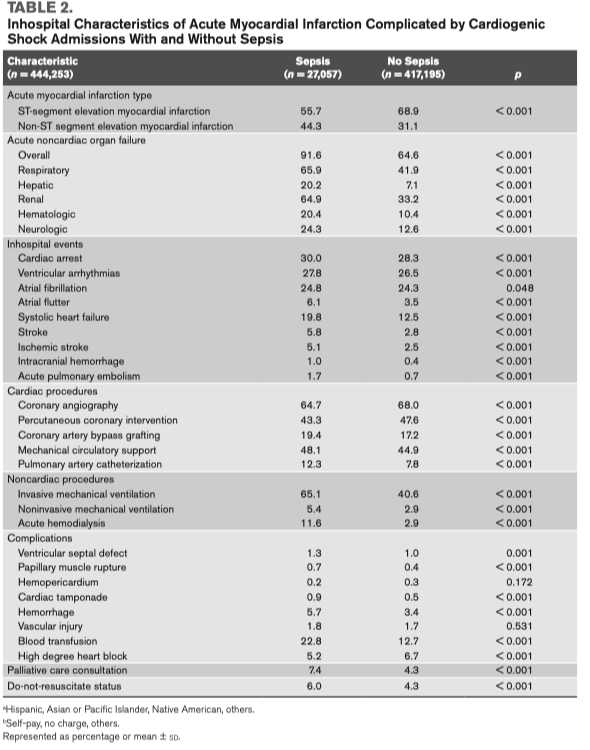
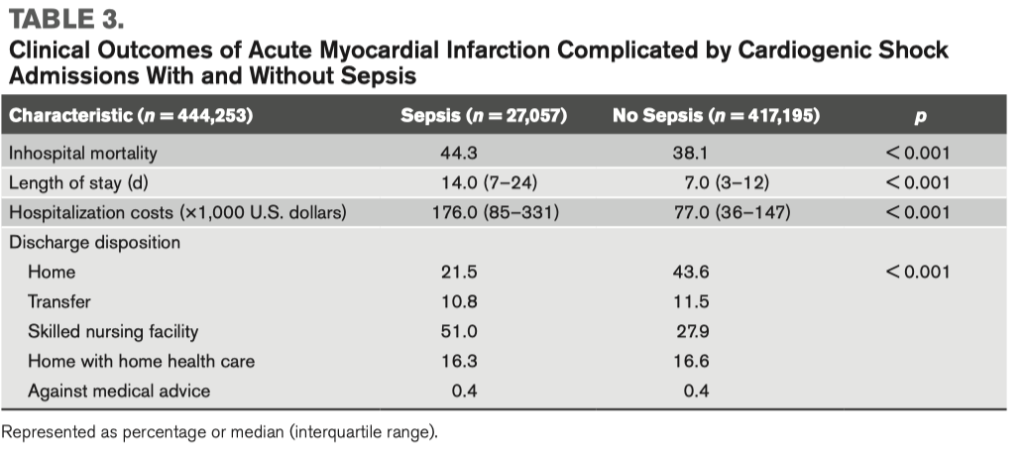
Если сравнивать две когорты пациентов (с сепсисом и без сепсиса), то когорта с сепсисом имела большую частоту развития остановки сердечной деятельности (cardiac arrest), большую частоту развития желудочковых аритмий, систолической сердечной недостаточности, инсультов (в большей части ишемический) и полиорганную недостаточность (Таблица 2). В когорте сепсиса чаще возникали кровотечения, требующие трансфузии компонентов крови (Таблица 2). В то время как когорта пациентов с сепсисом чаще получала не-кардиальные вмешательства и такие вмешательства, как катетеризацию легочной артерии, механические методы органной поддержки, острый гемодиализ, инвазивную и не-инвазивную механическую вентиляцию, в этой же когорте наблюдалось значительно меньшая частота применения коронарной ангиографии и чрескожных коронарных вмешательств (ЧКВ) по сравнению с когортой без сепсиса (p < 0.001) (Таблица 2). Пациенты с сепсисом чаще получали паллиативные вмешательства и здесь чаще встречались требования «Не проводить реанимацию» (do-not resuscitate orders) (Таблица 2). После стратификации на тип ОИМ, использование коронарографии, ЧКВ и ММПО у пациентов STEMI было увеличено при сравнении с пациентами NSTEMI (Рис. 2A–C). Снижение использования катетеризации легочной артерии у пациентов с ОИМ-КШ наблюдается в течение 15 лет (Рис. 2D). Высокий процент поступлений с сепсисом сопровождается развитием полиорганной недостаточности с устойчивым трендом на увеличение за последние 15 лет (Рис. 2D). Исходные и внутрибольничные характеристики пациентов с сепсисом по сравнению с септическим шоком представлены в дополнительной таблице 3 (http://links.lww.com/CCX/ A912). Госпитальная летальность у пациентов с сепсисом по сравнению с пациентами без сепсиса несколько выше (4.3% vs 38.1%; unadjusted OR, 1.29; 95% CI, 1.26–1.32; adjusted OR, 1.21; 95% CI, 1.18–1.25; p < 0.001). Временные тренды показывают увеличение госпитальной летальности среди пациентов с сепсисом в то время, как у пациентов без сепсиса летальность имеет тенденцию к снижению (p < 0.001) (Рис. 1, C и D). Поступившие пациенты с сепсисом имеют более длительное время госпитализации, высокую стоимость госпитализации, меньшую частоту выписки домой и более высокие показатели выписки в учреждения квалифицированного сестринского ухода (p < 0.001) (Таблица 3). В анализе чувствительности (дополнительная таблица 4, http://links.lww.com/CCX/A912) было показано, что кодирование на момент поступления как септический шок имело более высокую госпитальную летальность в подгруппах «возраст», «пол», «раса», «органная недостаточность» и «остановка сердечной деятельности».
Обсуждение
В этом большом исследовании, оценивающем эпидемиологию и клинические исходы при сепсисе в сочетании с ОИМ-КШ, было показано, что сепсис развивается у 6% пациентов, поступивших с ОИМ-КШ, при этом виден устойчивый временной рост распространенности сепсиса, который идет параллельно с увеличением количества инвазивных видов терапии. Пациенты в септической когорте имели более тяжелое состояние, с большей коморбидностью, с большим количеством осложнений во все время госпитализации, большую частоту развития внесердечной органной недостаточности, остановок сердечной деятельности и большую частоту применения механических методов органной поддержки. Несмотря на то, что все это предполагает наличие связи между сепсисом и неблагоприятными исходами ОИМ-КШ, нам удалось определить, что остаточный вмешивающий фактор, как тяжесть заболевания, не влиял на эту ассоциацию. Вызывает интерес то, что среди всех пациентов с ОИМ-КШ, пациенты с сепсисом реже получали такие инвазивные процедуры, как коронарографию и ЧВК, по сравнению с пациентами без сепсиса. Когорта пациентов с сепсисом показала большую госпитальную летальность, стоимость госпитализации, длительность нахождения пациента в стационаре по сравнению с пациентами без сепсиса, даже после корректировки на тяжесть состояния и применение методов интенсивной терапии. Наличие сепсиса было ассоциировано с различиями в менеджменте ОИМ-КШ, о чем свидетельствует меньшее применение процедур, рекомендованных в клинических руководствах, и большему применению паллиативных вмешательств, что тоже могло способствовать увеличению летальности в когорте пациентов с сепсисом. Госпитальная летальность у пациентов с ОИМ-КШ и сепсисом во время периода исследования показала рост тогда, когда летальность у пациентов с ОИМ-КШ без сепсиса показала снижение, что подчеркивает необходимость в раннем выявлении пациентов с сепсисом для улучшения терапии в такой подгруппе высокого риска.
Сепсис был и остается ведущей причиной госпитализаций, органной недостаточности и смерти во все мире [10]. Так что не вызывает удивления, что у пациентов с ОИМ-КШ при развитии у них сепсиса увеличивается риск развития широкого спектра неблагоприятных исходов. Впервые этот феномен был показан при вторичном анализе исследования SHOCK, когда у 18% пациентов с ОИМ-КШ развивается сепсис/подозрение на сепсис (три четверти из них имели положительные микробиологические посевы крови), а также и то, что эти пациенты имеют в два раза более высокий риск смерти [8]. Недавнее одноцентровое исследование из Mayo Clinic также нашло, что пациенты с кардиогенным шоком и сепсисом (19% из всех пациентов с КШ) имели более тяжелое течение заболевания и более высокий риск краткосрочной летальности [9]. В многоцентровом регистре Cardiac Critical Care Trials Network cardiac ICU (CICU) количество пациентов с сочетанным вазодилятационным и кардиогенным шоком оценивается в 20% от всех пациентов с шоком и эти пациенты наиболее тяжелые с большим риском смерти во время госпитализации [5]. Анализ пациентов регистра CICU, сделанный Mayo Clinic, нашел, что распространенность сепсиса увеличивается параллельно тяжести шока, от 6% у пациентов со средним шоком до 37% у пациентов с тяжелым шоком, что подразумевает потенциальную роль сепсиса в утяжелении кардиогенного шока [31]. Последовательный анализ такой же CICU когорты пациентов показал, что большинство пациентов имели критерии синдрома системного воспалительного ответа (ССВО) на момент поступления с увеличением распространённости по мере увеличения тяжести шока и такие пациенты имели большую вероятность смерти [32]. И наоборот, только у 2.4% пациентов с ОИМ без КШ, включенных в исследование «Pexelizumab in Conjunction With Angioplasty», развивались тяжелые инфекционные осложнения во время госпитализации, но при этом у пациентов, у которых течение ОИМ осложнялось инфекцией, вероятность развития неблагоприятных событий на 90-день была в четыре раза выше [33]. Необходимо отметить, что распространенность сепсиса, выявленного в этой национальной репрезентативной когорте, существенно ниже (6% против 18%), чем это было показано в более селективной когорте с КШ. Отражает ли это разницу в популяции или вариабельность в диагностике заболевания или в ведении документации, остается неясным [5, 8, 9]. В дополнение к вышеупомянутым причинам, объяснить многократное увеличение распространенности сепсиса при ОИМ-КШ могут изменения, что произошли с течением времени в распознавании или в документировании сепсиса.
У критически больных пациенты с ОИМ-КШ, которым требуются инвазивные кардио-пульмональные вмешательства, возрастает риск развития инфекций, связанных с оказанием медицинской помощи (ИСМП), что требует более тщательного соблюдения инфекционного контроля [34]. Несомненно, более длительные сроки госпитализации и большее использование инвазивных технологий при интенсивной терапии в подгруппе сепсиса предполагает развитие нозокоминального сепсиса. Распространенность ИСМП у пациентов, госпитализированных с острым сердечно-сосудистым заболеванием, незначительна в отличие от пациентов с КШ (35). Пациенты, у которых все развились ИСМП, имели более высокую госпитальную летальность, большую продолжительность госпитализации и более высокую стоимость лечения, как мы наблюдали у пациентов с ОИМ-КШ с сепсисом.
Уже много лет мы знаем о роли системного воспаления в развитии и прогрессировании КШ и органной недостаточности после ОИМ и вполне вероятно, что одни и те же патофизиологические процессы связывают воспаление при сепсисе с последующим развитием органной и циркуляторной недостаточности. Некроз кардиомиоцитов при ОИМ является триггером множества процессов воспаления, опосредованных иммунной системой, часто приводящим к стерильному системному воспалению, за которым может скрываться сепсис, на что указывает тот факт, что почти четверть пациентов с STEMI на момент поступления отвечают критериям ССВО [36]. Системное повреждение по типу «ишемия-реперфузия», что выявляется после реанимационных мероприятий по причине остановки сердечной деятельности, часто вызывает выраженный воспалительный ответ, что увеличивает риск развития инфекции у таких пациентов [37]. Независимо от причины системное воспаление может приводить к избыточной вазодилятации, что усугубляет гемодинамические нарушения и способствую большему повреждению тканей и органов. Уровни медиаторов воспаления, таких как С-реактивный белок и интерлейкин-6, уже идентифицированы как важные прогностические биомаркеры у пациентов с ОИМ-КШ и с вне-госпитальной остановкой сердечной деятельности и эти биомаркеры коррелируют с тяжестью шока [38—40]. В исследовании SHOCK пациенты с сепсисом имели низкое системное сосудистое сопротивление, а пациентам со смешанным шоком в исследовании «the Mayo Clinic and Cardiac Critical Care Trials Network cohorts» требовались более высокие дозы вазопрессоров [8]. Рассматривается и то обстоятельство, что в условиях вазоплегии и системного воспаления, что характерно для сепсиса, применение механических устройств кардиоподдержки в целях подъема артериального давления и увеличения сердечного выброса, может не иметь предполагаемого эффекта [6, 41]. Здесь мы видим очень большие проблемы, препятствующие стабилизации пациентов с тяжелым шоком в сочетании с сепсисом, что делает очевидным необходимость поиска других стратегий лечения у такой подгруппы пациентов. Несмотря на то, что за последнее десятилетие мы видим снижение частоты применения катетера легочной артерии в нашей когорте пациентов, недавние исследования указывают на то, что инвазивный мониторинг гемодинамики с помощью катетеризации легочной артерии у пациентов с КШ может принести пользу [42, 43].
Несмотря на все усилия разработчиков базы данных HCUP-NIS по минимизации ошибок анализа за счет использования внутренних и внешних мер контроля качества, все-таки база данных HCUP-NIS имеет фундаментальные ограничения, которые, в свою очередь, могут ограничивать дизайн исследований, интерпретацию данных и анализ данных, которые мы приняли во внимание [30]. Здесь есть несколько определенных подходов к идентификации сепсиса с помощью административных кодов, каждый из которых имеет свои важные ограничения. Мы использовали коды МКБ-9, указывающие на сепсис, в ущерб «не явным» кодам сепсиса (к примеру, коды, указывающие на инфекцию и органную дисфункцию), по причине того, что КШ сам по себе может вызвать органную дисфункцию, что может снизить специфичность неявного кодирования сепсиса [10]. По причине того, что все коды МКБ-9 используются при выписке из стационара, мы не могли точно установить, что случилось первым, ОИМ или сепсис. Однако, у всех включенных в исследование пациентов входным диагнозом был ОИМ. Принимая во внимание административную сущность имеющейся базы данных, мы не ставили себе целью разделить ОИМ на типы 1 и 2. Такая информация, как тяжесть шока, источник сепсиса, данные лабораторных и радиографических исследований, какие-либо дополнительные детали медицинского менеджмента, в базе данных NIS-HCUP недоступны. Все это не позволяет сделать окончательный вывод о том, что у всех пациентов с диагнозом сепсис была истинная инфекция, а не стерильная системная воспалительная реакция. В клинической практике септический шок может возникать как часть смешанного шока, но коды МКБ для смешанного шока не утверждены. Кроме того, несмотря на тщательные попытки скорректировать вмешивающиеся факторы с помощью многопараметрического анализа, остается возможность остаточного смешения.
Несмотря на то, что мы изучали данные, полученные за последние 15 лет, в анализ мы включили госпитализации, что произошли до 2014 года. Причина - внесение существенных изменений в определение и лечение сепсиса в связи с введением Третьего международного консенсуса в отношении определений сепсиса и септического шока, и рекомендаций Surviving Sepsis Campaign, но при этом мы считаем, что будущий анализ последних данных будет полезен для определения тенденций [44, 45]. Несколько исследований, опубликованных после 2015 г., выявили ограничения использования кодов МКБ-9 при выписке для идентификации случаев. Увеличение кодирования диагнозов сепсиса, по-видимому, не зависит от увеличения распространенности диагноза сепсиса, распознаваемого по клиническим критериям [46–49]. Поэтому мы не можем определить, были ли наблюдаемые тенденции к более частому диагностированию сепсиса с течением времени обусловлены изменениями в распространенности заболевания, распознавании или кодировании. Таким образом, наши результаты относительно временных тенденций следует интерпретировать с осторожностью. Период нашего исследования включает в себя госпитализации еще до принятия консенсусного определения сепсиса и публикаций рекомендаций Surviving Sepsis Campaign, что могло повысить осведомленность о сепсисе и повлиять на наблюдаемые тенденции в диагностике сепсиса.
Наконец, наши результаты представляют только госпитальные исходы, что не дает возможности сравнения/корреляции с долгосрочными последствиями, учитывая характер базы данных. Это важно потому, что выжившие после госпитализации с сепсисом подвержены повышенному риску последующей смерти и неблагоприятных сердечно-сосудистых событий [50].
Выводы
В заключение, в этом 15-летнем национальном исследовании мы нашли устойчивый рост распространенности сепсиса, осложняющего течение острого инфаркта миокарда с кардиогенным шоком, что ассоциируются с госпитальной летальностью. Пациенты с ОИМ-КШ и сепсисом имеют выраженную коморбидность (сопутствующую патологию), высокую частоту развития полиорганной недостаточности и высокую частоту остановки сердечной деятельности, высокий риск смерти. Более частое использование инвазивных технологий в терапии критических состояний идет параллельно распространённости сепсиса, что поднимает важные вопросы, такие как действительно ли увеличение распространенности сепсиса вызвано большей частотой использования современных инвазивных методов интенсивной терапии или действительно ли увеличение использования инвазивных методов интенсивной терапии подвергает пациент высокому риску развития сепсиса. Требуются новые исследования для понимания причин и патофизиологии сепсиса у пациентов с острым инфарктом миокарда и кардиогенным шоком в целях улучшения мер профилактики и поиска новых стратегий терапии.
Список литературы:
1. Chioncel O, Parissis J, Mebazaa A, et al: Epidemiology, pathophysiology and contemporary management of cardiogenic shock - a position statement from the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2020; 22:1315–1341
2. Omer MA, Tyler JM, Henry TD, et al: Clinical characteristics and outcomes of STEMI patients with cardiogenicshock and cardiac arrest. JACC Cardiovasc Interv 2020; 13:1211–1219
3. Kolte D, Khera S, Aronow WS, et al: Trends in incidence, management, and outcomes of cardiogenic shock complicating ST-elevation myocardial infarction in the United States. J Am Heart Assoc 2014; 3:e000590
4. Vallabhajosyula S, Dunlay SM, Prasad A, et al: Acute noncardiac organ failure in acute myocardial infarction with cardiogenic shock. J Am Coll Cardiol 2019; 73:1781–1791
5. Berg DD, Bohula EA, van Diepen S, et al: Epidemiology of shock in contemporary cardiac intensive care units. Circ Cardiovasc Qual Outcomes 2019; 12:e005618
6. van Diepen S, Katz JN, Albert NM, et al; American Heart Association Council on Clinical Cardiology; Council on Cardiovascular and Stroke Nursing; Council on Quality of Care and Outcomes Research; and Mission: Lifeline: Contemporary management of cardiogenic shock: A scientific statement from the American Heart Association. Circulation 2017; 136:e232–e268
7. Cuinet J, Garbagnati A, Rusca M, et al: Cardiogenic shock elicits acute inflammation, delayed eosinophilia, and depletion of immune cells in most severe cases. Sci Rep 2020; 10:7639
8. Kohsaka S, Menon V, Lowe AM, et al; SHOCK Investigators: Systemic inflammatory response syndrome after acute myocardial infarction complicated by cardiogenic shock. Arch Intern Med 2005; 165:1643–1650
9. Jentzer JC, Ahmed AM, Vallabhajosyula S, et al: Shock in the cardiac intensive care unit: Changes in epidemiology and prognosis over time. Am Heart J 2021; 232:94–104
10. Rudd KE, Johnson SC, Agesa KM, et al: Global, regional, and national sepsis incidence and mortality, 1990-2017: Analysis for the Global Burden of Disease Study. Lancet 2020; 395:200–211
11. HCUP National Inpatient Sample (NIS): Healthcare Cost and Utilization Project (HCUP). Rockville, MD, Agency for Healthcare Research and Quality. Available at: https://www. hcup-us.ahrq.gov/. Accessed January 24, 2022.
12. Vallabhajosyula S, Kumar V, Vallabhajosyula S, et al: Acute myocardial infarction-cardiogenic shock in patients with prior coronary artery bypass grafting: A 16-year national cohort analysis of temporal trends, management and outcomes. Int J Cardiol 2020; 310:9–15
13. Vallabhajosyula S, Patlolla SH, Dunlay SM, et al: Regional variation in the management and outcomes of acute myocardial infarction with cardiogenic shock in the United States. Circ Heart Fail 2020; 13:e006661
14. Lambert L, Blais C, Hamel D, et al: Evaluation of care and surveillance of cardiovascular disease: Can we trust medicoadministrative hospital data? Can J Cardiol 2012; 28:162–168
15. Lauridsen MD, Gammelager H, Schmidt M, et al: Positive predictive value of International Classification of Diseases, 10th revision, diagnosis codes for cardiogenic, hypovolemic, and septic shock in the Danish National Patient Registry. BMC Med Res Methodol 2015; 15:23
16. Kumar G, Kumar N, Taneja A, et al; Milwaukee Initiative in Critical Care Outcomes Research (MICCOR) Group of Investigators: Nationwide trends of severe sepsis in the 21st century (2000-2007). Chest 2011; 140:1223–1231
17. Martin GS, Mannino DM, Eaton S, et al: The epidemiology of sepsis in the United States from 1979 through 2000. N Engl J Med 2003; 348:1546–1554
18. Angus DC, Linde-Zwirble WT, Lidicker J, et al: Epidemiology of severe sepsis in the United States: Analysis of incidence, outcome, and associated costs of care. Crit Care Med 2001; 29:1303–1310
19. Bouza C, Lopez-Cuadrado T, Amate-Blanco JM: Use of explicit ICD9-CM codes to identify adult severe sepsis: Impacts on epidemiological estimates. Crit Care 2016; 20:313
20. Vallabhajosyula S, Deshmukh AJ, Kashani K, et al: Tako-Tsubo cardiomyopathy in severe sepsis: Nationwide trends, predictors, and outcomes. J Am Heart Assoc 2018; 7:e009160
21. Jolley RJ, Sawka KJ, Yergens DW, et al: Validity of administrative data in recording sepsis: A systematic review. Crit Care 2015; 19:139
22. Quan H, Sundararajan V, Halfon P, et al: Coding algorithms for defining comorbidities in ICD-9-CM and ICD-10 administrative data. Med Care 2005; 43:1130–1139
23. Vallabhajosyula S, Dunlay SM, Barsness GW, et al: Hospitallevel disparities in the outcomes of acute myocardial infarction with cardiogenic shock. Am J Cardiol 2019; 124:491–498
24. Vallabhajosyula S, Dunlay SM, Barsness GW, et al: Temporal trends, predictors, and outcomes of acute kidney injury and hemodialysis use in acute myocardial infarction-related cardiogenic shock. PLoS One 2019; 14:e0222894
25. Vallabhajosyula S, Dunlay SM, Kashani K, et al: Temporal trends and outcomes of prolonged invasive mechanical ventilation and tracheostomy use in acute myocardial infarction with cardiogenic shock in the United States. Int J Cardiol 2019; 285:6–10
26. Vallabhajosyula S, Dunlay SM, Prasad A, et al: Cardiogenic shock and cardiac arrest complicating ST-segment elevation myocardial infarction in the United States, 2000-2017. Resuscitation 2020; 155:55–64
27. Vallabhajosyula S, Kashani K, Dunlay SM, et al: Acute respiratory failure and mechanical ventilation in cardiogenic shock complicating acute myocardial infarction in the USA, 20002014. Ann Intensive Care 2019; 9:96
28. Vallabhajosyula S, Prasad A, Bell MR, et al: Extracorporeal membrane oxygenation use in acute myocardial infarction in the United States, 2000 to 2014. Circ Heart Fail 2019; 12:e005929
29. Vallabhajosyula S, Prasad A, Dunlay SM, et al: Utilization of palliative care for cardiogenic shock complicating acute myocardial infarction: A 15-year national perspective on trends, disparities, predictors, and outcomes. J Am Heart Assoc 2019; 8:e011954
30. Khera R, Angraal S, Couch T, et al: Adherence to methodological standards in research using the national inpatient sample. JAMA 2017; 318:2011–2018
31. Jentzer JC, van Diepen S, Barsness GW, et al: Cardiogenic shock classification to predict mortality in the cardiac intensive care unit. J Am Coll Cardiol 2019; 74:2117–2128
32. Jentzer JC, Lawler PR, van Diepen S, et al: Systemic inflammatory response syndrome is associated with increased mortality across the spectrum of shock severity in cardiac intensive care patients. Circ Cardiovasc Qual Outcomes 2020; 13:e006956
33. Truffa AA, Granger CB, White KR, et al: Serious infection after acute myocardial infarction: Incidence, clinical features, and outcomes. JACC Cardiovasc Interv 2012; 5:769–776
34. Fordyce CB, Katz JN, Alviar CL, et al; American Heart Association Council on Clinical Cardiology; Council on Arteriosclerosis, Thrombosis and Vascular Biology; Council on Cardiovascular and Stroke Nursing; Council on Cardiopulmonary, Critical Care, Perioperative and Resuscitation; and Stroke Council: Prevention of complications in the cardiac intensive care unit: A scientific statement from the American Heart Association. Circulation 2020; 142:e379–e406
35. Miller PE, Guha A, Khera R, et al: National trends in healthcare-associated infections for five common cardiovascular conditions. Am J Cardiol 2019; 124:1140–1148
36. van Diepen S, Vavalle JP, Newby LK, et al: The systemic inflammatory response syndrome in patients with ST-segment elevation myocardial infarction. Crit Care Med 2013; 41:2080–2087
37. Jentzer JC, Chonde MD, Dezfulian C: Myocardial dysfunction and shock after cardiac arrest. Biomed Res Int 2015; 2015:314796
38. Ceglarek U, Schellong P, Rosolowski M, et al: The novel cystatin C, lactate, interleukin-6, and N-terminal pro-B-type natriuretic peptide (CLIP)-based mortality risk score in cardiogenic shock after acute myocardial infarction. Eur Heart J 2021; 42:2344–2352
39. Bro-Jeppesen J, Johansson PI, Kjaergaard J, et al: Level of systemic inflammation and endothelial injury is associated with cardiovascular dysfunction and vasopressor support in postcardiac arrest patients. Resuscitation 2017; 121:179–186
40. Bro-Jeppesen J, Kjaergaard J, Wanscher M, et al: Systemic inflammatory response and potential prognostic implications after out-of-hospital cardiac arrest: A substudy of the target temperature management trial. Crit Care Med 2015; 43:1223–1232
41. Rihal CS, Naidu SS, Givertz MM, et al; Society for Cardiovascular Angiography and Interventions (SCAI), Heart Failure Society of America (HFSA), Society of Thoracic Surgeons (STS), American Heart Association (AHA), and American College of Cardiology (ACC): 2015 SCAI/ACC/HFSA/STS clinical expert consensus statement on the use of percutaneous mechanical circulatory support devices in cardiovascular care: Endorsed by the American Heart Association, the Cardiological Society of India, and Sociedad Latino Americana de Cardiología Intervencionista; Affirmation of Value by the Canadian Association of Interventional Cardiology-Association Canadienne de Cardiologie d’intervention. J Am Coll Cardiol 2015; 65:2140–2141
42. Garan AR, Kanwar M, Thayer KL, et al: Complete hemodynamic profiling with pulmonary artery catheters in cardiogenic shock is associated with lower in-hospital mortality. JACC Heart Fail 2020; 8:903–913
43. O’Neill WW, Grines C, Schreiber T, et al: Analysis of outcomes for 15,259 US patients with acute myocardial infarction cardiogenic shock (AMICS) supported with the Impella device. Am Heart J 2018; 202:33–38
44. Singer M, Deutschman CS, Seymour CW, et al: The third international consensus definitions for sepsis and septic shock (Sepsis-3). JAMA 2016; 315:801–810
45. Rhodes A, Evans LE, Alhazzani W, et al: Surviving sepsis campaign: International guidelines for management of sepsis and septic shock: 2016. Intensive Care Med 2017; 43:304–377
46. Rhee C, Dantes R, Epstein L, et al; CDC Prevention Epicenter Program: Incidence and trends of sepsis in US hospitals using clinical vs claims data, 2009-2014. JAMA 2017; 318:1241–1249
47. Rhee C, Kadri S, Huang SS, et al: Objective sepsis surveillance using electronic clinical data. Infect Control Hosp Epidemiol 2016; 37:163–171
48. Rhee C, Murphy MV, Li L, et al; Centers for Disease Control and Prevention Epicenters Program: Comparison of trends in sepsis incidence and coding using administrative claims versus objective clinical data. Clin Infect Dis 2015; 60:88–95
49. Rhee C, Murphy MV, Li L, et al; Centers for Disease Control and Prevention Epicenters Program: Improving documentation and coding for acute organ dysfunction biases estimates of changing sepsis severity and burden: A retrospective study. Crit Care 2015; 19:338
50. Mankowski RT, Yende S, Angus DC: Long-term impact of sepsis on cardiovascular health. Intensive Care Med 2019; 45:78–81
Critical Care Explorations,