Сепсис и септический шок: клиническое руководство, в основу которого положены стратегии управления
CLEVELAND CLINIC JOURNAL OF MEDICINE VOLUME 87 • NUMBER 1 JANUARY 2020
doi:10.3949/ccjm.87a.18143
Сепсис и септический шок: клиническое руководство, в основу которого положены стратегии управления
Перевод оригинальной статьи «Sepsis and septic shock: Guideline-based management»
Авторы: Siddharth Dugar, MD; Chirag Choudhary, MD, MBA; Abhijit Duggal, MD, MPH, MSc, FACP
Ключевые моменты
- Такие инструменты, как критерии синдрома системного воспалительного ответа и быстрая версия шкалы последовательной оценки степени недостаточности органов (qSOFA), могут помочь в ранней диагностике сепсиса и сортировке пациентов.
- Начальный антибиотик должен быть широкого спектра действия, его назначение должно быть основано на локальных моделях чувствительности, антибиотикотерапия должна проводится с ежедневной оценкой возможности её де-эскалации или прекращения антибактериальной терапии.
- Интенсивная инфузионная терапия должна сопровождаться взвешиванием выгод и рисков от дополнительного введения жидкости на основании динамически оцениваемого состояния объема, а при восстановлении - агрессивное удаление жидкости.
- Целевое значение среднего артериального давления при проведении интенсивной терапии составляет 65 мм Hg. Вазопрессор первой линии - норадреналин (при необходимости возможно сочетание с вазопрессином).
- Глюкокортикоиды не рекомендуются к применению, если для восстановления гемодинамической стабильности достаточно инфузионной терапии и вазопрессоров.
Сепсис и особенно септический шок следует признавать неотложным состоянием, в котором решающее значение имеет время, подобно таким состояниям, как острое нарушение мозгового кровообращения и острый инфаркт миокарда. Раннее распознавание и быстрое начало интенсивной терапии имеют решающее значение. Но распознавание сепсиса остается проблемой в то время, как продолжают развиваться новые и эффективные методы управления.
В этой статье рассматриваются рекомендации по диагностике и лечению сепсиса и септического шока, особое внимание здесь уделяется обеспечению максимальной приверженности положениям передовой практики, а также имеющимся противоречиям в определениях, диагностических критериях и в управлении (менеджменте).
Всеобщий и жизне-угрожающий
В США 750 000 пациентов ежегодно страдают от сепсиса, при этом сепсис является основной причиной летальности среди пациентов, находящихся в критическом состоянии, приводя к смерти более 210 000 человек каждый год [1]. Около 15% пациентов, которым установлен диагноз сепсис, страдают от септического шока, который составляет около 10% случаев госпитализации в отделения интенсивной терапии и имеет уровень летальности более 50%.
Частота выявления сепсиса в Соединенных Штатах в период с 2000 по 2008 гг. удвоилась [2], возможно, из-за увеличения числа хронических заболеваний в нашей стареющей популяции наряду с ростом резистентности к антибиотикам и увеличением частоты применения инвазивных процедур, иммунодепрессантов и химиотерапии.
Расходы, связанные с лечением сепсиса в Соединенных Штатах, составляют более 20,3 млрд. долл. США в год.
Развитие определений сепсиса
В 1991 году впервые было дано определение сепсиса, как синдрома системного воспалительного ответа или ССВО (англ. systemic inflammatory response syndrome или SIRS), развивающегося вследствие предполагаемой или подтвержденной инфекции, при этом в клинической картине должны были определяться два и более критерия ССВО [4]:
• Температура тела ниже 36°C или выше 38°C
• Частота сердечных сокращений более 90 ударов в минуту
• Частота дыхания свыше 20 дыханий в минуту, или парциалное артериальной давление СО2 ниже 32 ммHg
• Лейкоцитоз менее 4 × 109 /л или свыше 12 × 109 /L, или палочкоядерный сдвиг свыше 10%.
Тяжелый сепсис определялся, как прогрессирование сепсиса до органной дисфункции, тканевой гипоксии или гипотензии.
Септический шок определялся, как как дисфункция органов и гипотензия, рефракторная к интенсивной инфузионной терапии, что требовало введения вазоактивных препаратов, в сочетании с двумя или более критериями ССВО, перечисленными выше.
В 2001 году определения были обновлены путем добавления клинических симптомов и лабораторных данных.
В 2004 году в клиническом руководстве the Surviving Sepsis Campaign эти определения были одобрены, что привело к разработке модели лечения сепсиса по протоколу SEP-1, внедренном впоследствии во всем мире [6]. Последовав их примеру, центры США по программам Medicare и Medicaid (CMS), определили сепсис, как наличие как минимум 2 критериев ССВО в сочетании с инфекцией; тяжелый сепсис, как сепсис с дисфункцией органов (в том числе увеличение уровня сывороточного лактата свыше 2 ммоль/л);
септический шок как рефракторная у интенсивной инфузионной терапии гипотензия, требующая введения вазопрессоров, или уровень лактата не менее 4 ммоль/л [7].
В 2016 году Комитет «Сепсис-3» выпустил новые определения сепсиса
• Сепсис - опасное для жизни состояние, вызванное нарушениями иммунного ответа на инфекцию, что приводит к развитию дисфункции органов.
• Септический шок - нарушения кровообращения, клеточные и метаболические нарушения у пациентов с сепсисом, клинически проявляющиеся в виде рефрактерной к инфузионной терапии гипотензии, что требует проведения вазопрессорной терапии, с ассоциированной гипоперфузией тканей (уровень сывороточного лактата свыше 2 ммоль/л).
Понятие тяжелого сепсиса из классификации было исключено.
Множество определений вызывает путаницу
В настоящее время в клинической практике используются оба определения, CMS и международного консенсуса, с четкой терминологией, но различными критериями идентификации, включая сюда и артериальное давление, и точки отсечения лактата. CMS в своих определениях сепсиса продолжает рекомендовать критерии ССВО для идентификации сепсиса, в то время как Sepsis-3 для определения сепсиса использует последовательную оценку степени повреждения органов (шкала SOFA) или экспресс-версию шкалы SOFA – qSOFA (описано ниже). Это привело к путанице среди врачей и стало спорным фактором при разработке протоколов оказания медицинской помощи.
Инструменты для идентификации риска
Шкалы SOFA и qSOFA
Шкала SOFA громоздкая
Шкала SOFA - система объективной оценки, предназначенная для определения степени выраженности дисфункции органов, что основана на уровне кислорода (парциальное давление кислорода и фракция вдыхаемого кислорода), на количестве тромбоцитов, показателя шкалы ком Глазго, на уровне билирубина, на уровне креатинина (или темпа диуреза) и на среднем артериальном давлении (или необходимости в применении вазоактивных агентов). Она обычно применяется в клинической и исследовательской практике для мониторинга недостаточности органов (в индивидуальном порядке или при исследованиях) у пациентов, находящихся в критическом состоянии [9]. Но вся эта необходимая для оценки информация весьма обременительна в контексте получения разнообразных параметров и бывает не доступна у постели пациента на момент принятия клинических решений.
Шкала qSOFA легче…
Для создания упрощенной версии шкалы SOFA, именуемой сейчас qSOFA, Singer et al. [8] сравнили шкалу SOFA с критериями ССВО и определили 3 независимых предвестника развития дисфункции органов, связанных с неблагоприятными исходами при сепсисе:
• Частота дыхания не менее 22 вдохов/мин;
• Систолическое артериальное давление 100 мм Hg и ниже;
• Нарушения психического (ментального) статуса - шкала комы Глазго <15 баллов).
Оценка по шкале qSOFA в 2 и более баллов при наличии подозрения на инфекцию или при подтверждённой инфекции была предложена в качестве триггера начала агрессивного лечения, включая сюда частый мониторинг жизненно важных функций и госпитализацию. Преимущество шкалы qSOFA в том, что данные, ее составляющие, легко получить в клинической практике.
…но имеет много ограничений
Несмотря на то, что с помощью шкалы qSOFA можно выявить тяжелую дисфункцию органов и прогнозировать риск смерти при сепсисе, для определения сепсиса необходима тщательная интерпретация. Одна из проблем заключается в том, что шкала gSOFA основана на способности клинициста идентифицировать инфекцию, как причину дисфункции органов, но инфекция может не проявляться на раннем этапе, что для диагностики раннего сепсиса делает шкалу qSOFA менее чувствительной, чем критерии ССВО [10].
Более того, ранее существовавшие хронические заболевания могут влиять на точность измерения при применении шкал qSOFA и SOFA [11]. Помимо этого, шкала qSOFA была одобрена к применению вне отделения интенсивной терапии (ОИТ), а полезность ее применения у пациентов, уже поступивших в ОИТ, ограничена [12].
Исследования показали, что для выявления сепсиса следует использовать критерии ССВО, тогда как шкалу qSOFA следует использовать только в качестве инструмента сортировки.
Антимикробная терапия
[Быстрые] антибиотики широкого спектра действия
Задержка с назначением надлежащей антибактериальной терапии связана со значительным увеличением летальности [14–16]. Соответствующие целям антимикробные препараты следует начинать в течение первого часа после распознавания сепсиса, но только после взятия микробиологических посевов соответствующих образцов при условии, что это существенно не повлияет на время начала антибиотикотерапии [17].
Начинать следует с противомикробных препаратов широкого спектра действия, охватывающих все возможные патогены. Для обеспечения достаточного охвата предпочтительны комбинированные режимы, особенно при септическом шоке. Эмпирический выбор противомикробных препаратов должен учитывать место заражения, предыдущее применение антибиотиков, локальную восприимчивость к патогенам, наличие иммуносупрессии и факторов риска для резистентных микроорганизмов. Для пациентов с высокой вероятностью заражения резистентными патогенами следует рассмотреть комбинацию антимикробных препаратов, что охватила бы грамотрицательные микроорганизмы и метициллин-резистентный золотистый стафилококк (MRSA) [18]. Комбинированное применение двух антибиотиков, направленное на грамотрицательные микроорганизмы, может быть уместным в случаях , когда имеется высокая степень подозрения на инфекцию микроорганизмами с множественной лекарственной устойчивостью, такими как Pseudomonas или Acinetobacter. Если предположить, что причиной сепсиса является внутрибольничный источник инфекции, рекомендуются препараты против MRSA.
Важно соблюдать соответствующие дозировки, так как эффективность зависит и от пикового уровня препарата в крови, и от того, как долго его уровень в крови остается выше минимальной ингибирующей концентрации для патогена. Первоначально вводимая более высокая нагрузочная доза может быть наилучшей стратегией для достижения терапевтического уровня препарата в крови, при этом дальнейшее дозирование основывается на консультации с врачом-инфекционистом или фармакологом.
Рассмотреть возможность антигрибковой терапии
За последние несколько десятилетий произошло на 200% увеличилась заболеваемость сепсисом из-за инфекций, вызываемых грибками [19]. Назначение антифунгальных препаратов следует рассматривать у пациентов из группы риска, которую составляют пациенты, которым поводилось полное парентеральное питание, с недавним лечением антибиотиками широкого спектра действия, с перфорациями полых органов ЖКТ, при состояниях с ослабленным иммунитетом.
Факторы риска грибковой инфекции при септическом шоке должны приводить врача к назначению эхинокандинов или липосомального амфотерицина В. У гемодинамически стабильных пациентов можно назначать азолы [20].
Де-эскалация и ранее прекращение
Антибиотики не безвредны - длительное использование антибиотиков широкого спектра связано с развитием устойчивости к противомикробным препаратам, с развитием инфекции Clostridium difficile и даже со смертью пациента [21].
В целях соблюдения баланса необходима надежная стратегия де-эскалации. Прагматическая стратегия может включать в себя начало антимикробной терапии с противомикробных препаратов широкого спектра действия, особенно в условиях гипотензии, а затем быстрой де-эскалации к противомикробным препаратам с более узким спектром действия, но решение должно быть основано на паттернах локальной чувствительности. Если клиническое течение предполагает, что болезнь на самом деле не вызвана инфекцией, антибиотики следует немедленно прекратить. Было доказано, что экспресс-тест полимеразную цепную реакцию для назальной MRSA, направляющий де-эскалацию, является безопасным и значительно снижает эмпирическое использование ванкомицина и линезолида [22,23]. Возможность де-эскалации антибиотиков необходимо обсуждать ежедневно [17]. Для большинства инфекций может подойти курс антибактериальной терапии длительностью 7-10 дней или даже короче [24,25], хотя может потребоваться и более длительный курс в случаях, когда невозможно обеспечить контроль за источником инфекции, а также у пациентов с ослабленным иммунитетом, при бактериемии, вызванной S. aureus, при эндокардите или при грибковой инфекции.
Интенсивная инфузионная терапия
Сепсис ассоциируется с вазодилятацией, капиллярной утечкой и снижением эффективного объема циркулирующей крови, снижающим венозный возврат. Все это приводит к нарушению перфузии тканей и развитию дисфункции органов. Целью интенсивной инфузионной терапии при сепсисе и септическом шоке является восстановление внутрисосудистого объема, увеличение доставки кислорода к тканям и разрешение дисфункции органов.
Болюс кристаллоидов в дозе 30 мл/кг рекомендуется ввести в течение 3 часов после обнаружения тяжелого сепсиса или септического шока [17]. Но данных, подтверждающих преимущества при соблюдении этой рекомендации, недостаточно, а вот количество доказательств вреда от устойчивого положительного баланса жидкости растет.
Есть рекомендации, в которых предостерегают от слишком большого объёма инфузии, особенно у пациентов с ограниченным кардиореспираторным резервом [26]. Введение чрезмерного количества жидкости может привести к отеку легких, гипоксической дыхательной недостаточности, отеку органов, внутрибрюшной гипертензии, длительному пребыванию в отделении интенсивной терапии и длительному времени искусственной вентиляции легких, и даже к повышенному риску смерти [26,27].
Понимая это, интенсивная инфузионная терапия должна осуществляться следующим образом, в виде последовательных этапов [28]:
• Rescue (Спасение): для коррекции гипоперфузии и шока в течение первых минут или часов требуется введение болюсов инфузионных растворов в объёме от 1 до 2 литров раствора кристаллоида
• Optimization (Оптимизация). На втором этапе для улучшения сердечного выброса и перфузии тканей в целях снижения вреда, необходимо ввести дополнительное количество жидкости [27].
• Stabilization (Стабилизация) - третий этап, обычно через 24-48 часов после начала септического шока, когда следует попытаться достичь нулевого или слегка отрицательного баланса жидкости
• De-escalation (Деэскалация) - четвертый этап, на котором отмечается разрешение шока и восстановление функции органов, и на котором необходимо инициировать агрессивные стратегии удаления жидкости [27].
Оценка объема с помощью динамических показателей
Клиницистам следует отказаться от использования статических показателей для оценки состояния объема. Было обнаружено, что при оценке изменений сердечного выброса во время проведения инфузионой терапии центральное венозное давление, статический показатель, наиболее часто применяемый как цель интенсивной терапии, по сравнению с термодилюцией с использованием катетеров для легочной артерии является точным только в половине случаев [29]. Мета-анализ 2017 года [30] показал, что использование динамической оценки в целенаправленной терапии связано с более низким риском летальности, более коротким пребыванием в ОИТ и меньшей продолжительностью искусственной вентиляции легких.
Динамические показатели используются для оценки влияния дополнительного объема инфузии на сердечный выброс. Применяются два метода - либо внутривенное введение болюса жидкости, либо пассивное поднятие ног. Последний метод возвращает от 200 до 300 мл крови из нижних конечностей в центральный кровоток и выполняется, когда пациента переводят сначала в положение Фовлера (с поднятым головным концом кровати), а затем опускают туловище пациента в горизонтальное положение и пассивно поднимают ноги.
При проведении любого из этих методов изменение сердечного выброса измеряется либо напрямую (например, с помощью термодилюции, эхокардиографии или анализа контура пульса), либо с использованием суррогатов сердечного выброса (например, изменение пульсового давления).
В качестве альтернативы, изменения сердечного выброса могут быть измерены по взаимодействию сердца и легких у пациента, находящегося на искусственной вентиляции легких во время вдоха и выдоха оценивают изменения внутригрудного давления, используя для этого изменение пульсового давления, изменение ударного объема и изменение размера нижней полой вены.
В прогнозировании чувствительности к преднагрузке динамические показатели, упомянутые выше, более точны, чем статические, именно поэтому они и рекомендуются для управления инфузионной терапией [31,32]. Но у них есть и свои ограничения [33]. Несмотря на то, что введение болюса жидкости пациентам, находящимся в критическом состоянии, остается золотым стандартом, не избирательное введение жидкости влечет за собой риск перегрузки жидкостью. Сердечно-легочные взаимодействия будут неточными у пациентов с аритмией, у тех, кто дышит самостоятельно с активным усилием на аппарате ИВЛ и у пациентов после открытых торакальных и абдоминальных операций. Таким образом, их применение будет ограничено у большинства критически больных пациентов.
В отличие от других динамических тестов, пассивный тест с поднятием нижних конечностей является точным у пациентов со спонтанным дыханием, у пациентов с нарушениями сердечного ритма и у тех, ному проводится искусственная вентиляция легких с низким дыхательным объемом [35]. В связи с отличной чувствительностью и специфичностью, для определения ответа к инфузионной терапии рекомендуется пассивный тест с поднятием нижних конечностей.
Лактат как цель интенсивной терапии
Интенсивная терапия, где целью служит уровень сывороточного лактата, может значительно снизить высокий уровень летальности, связанный с повышенными его уровнями (> 4 ммоль/л) [36,37]. Повышение уровня лактата при сепсисе может быть связано с гипоксией тканей, ускоренным гликолизом из-за гиперадренергического состояния, приемом лекарств (адреналина, бета2-агонистов) или печеночной недостаточностью. Измерение уровня лактата - объективный способ оценки реакции на проводимую интенсивную терапию, и этот подход лучше, чем применение других клинических маркеров, и поэтому уровень сывороточного лактат продолжает оставаться неотъемлемой частью определений сепсиса и алгоритма лечения в конической руководстве the Surviving Sepsis Campaign [7,8,17]. Даже если лактат и не является прямым указателем на гипоперфузию тканей, он является основой для оценки гипоперфузии конечных органов.
Интенсивная терапия, где целью служит насыщением кислородом центральной венозной крови (требующая установки центрального венозного катетера) не дает никаких преимуществ перед интенсивной терапией, где целью служит сывороточный лактат [38]. Приборы для оценки состояния микрососудистого русла являются многообещающими инструментами для управления интенсивной терапией, но их применение все еще ограничено клиническими исследованиями.
На сегодня оптимальные конечные цели интенсивной терапии еще неизвестны, но есть оптимальные ключевые переменные для управления интенсивной терапией и включают в себя совокупность результатов физикального исследования плюс периферическую перфузию, клиренс лактата и динамическую чувствительность к преднагрузке [17,39].
Сбалансированные кристаллоиды имеют преимущества перед изотоническими растворами.
Для интенсивной инфузионной терапии сепсиса и септического шока рекомендуются к применению кристаллоидные растворы (изотонический солевой раствор или сбалансированные кристаллоиды). До сих пор обсуждается, что из них лучше, но за последнее десятилетие решения в пользу сбалансированных растворов при интенсивной терапии пациентов, находящихся в критическом состояниии, стали пользоваться популярностью. Все больше данных свидетельствуют о том, что применение сбалансированных кристаллоидов (раствор Рингера-лактат, Plasma-Lyte) связано с более низкой частотой почечного повреждения, меньшей потребностью в заместительной почечной терапии и более низкой летальностью у пациентов в ОИТ. Кроме того, изотонический солевой раствор связан с развитием гиперхлоремии и метаболического ацидоза, а какие состояния снижают почечный кортикальный кровоток [40-42].
Нет доказанной пользы от коллоидов
Основанием для применения коллоидов является повышение внутрисосудистого онкотического давления, снижение капиллярной утечки и, следовательно, уменьшение количества жидкости, необходимой для интенсивной терапии. Но исследования in vivo не смогли показать наличие такого преимущества.
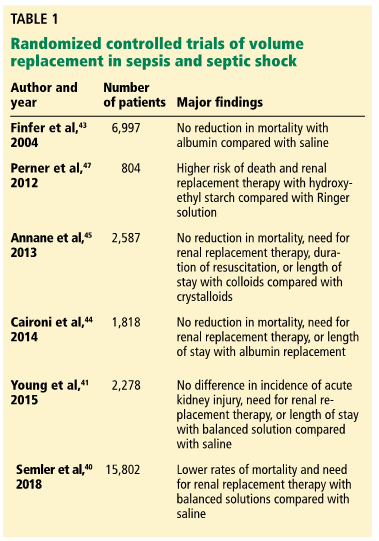
Можно рассмотреть возможность применения при сепсисе альбумина тогда, когда для восстановления внутрисосудистого объема требуется значительный объём инфузии [17]. Однако сравнение кристаллоидов и альбумина, как для интенсивной инфузионной терапии, так и для увеличения уровня сывороточного альбумина у пациентов, находящихся в критических состояниях, не выявило никакой пользы в контексте заболеваемости или летальности [43-45]. При рассмотрении вопроса о применении альбумина в комплексной терапии сепсиса или септического шока клиницисты должны помнить о его недостатках и о его значительной, в 20 – 100 раз больше, чем кристаллоидов, стоимости, при этом дополнительные расходы превышают 30 000 долл. США на каждый случай применения альбумина.
Применение другого коллоида, гидроксиэтилкрахмала (ГЭК), было связано с более высоким уровнем летальности и более высокой частотой развития почечной недостаточности у пациентов с сепсисом и в настоящее время ГЭК не должен применяться при интенсивной инфузионной терапии (Таблица 1) [47].
Ранний контроль источника инфекции
Контроль источника крайне важен при лечении сепсиса и септического шока. Неадекватный контроль источника может привести к ухудшению работы органов и нестабильности гемодинамики, несмотря на соответствующие реанимационные меры [17]. Тщательное обследование и соответствующие лучевые методы исследования должны быть выполнены и определен оптимальный способ контроля источника и оценки рисков, связанных с каждым вмешательством. При необходимости, контроль источника должен быть достигнут в течение 6-12 часов после постановки диагноза, сразу после того, как завершилась начальная стадия интенсивной терапии [48]. Сам по себе контроль источника может варьироваться от удаления инфицированных внутрисосудистых устройств и установки дренажа эмпиемы плевры до чрескожного или хирургического вмешательства в случаях холецистита и пиелонефрита.
Восстановление артериального давления
Персистирующая гипотензия и гипоперфузия тканей после адекватной интенсивной инфузионной терапии вызывается потерей нормального симпатического тонуса сосудов, что приводит к вазодилатации, нейрогормональному дисбалансу, депрессии миокарда, микроциркуляторной дисрегуляции и митохондриальной дисфункции. Вазопрессоры и инотропы восстанавливают доставку кислорода в ткани, повышая артериальное давление и сердечный выброс, соответственно.
Предпочтительной целью интенсивной терапии является среднее артериальное давление (АДср). Рекомендуемое его начальное значение 65 мм Hg. Более высокая цель от 80 до 85 мм Hg может помочь пациентам с хронической гипертензией [49], тогда как более низкая цель может лучше переноситься пациентами с пониженной систолической функцией, пожилыми пациентами и пациентами с терминальной стадией заболевания печени.
Эти рекомендации основаны на нашем понимании ауторегуляции кровотока в сосудистых руслах центральных органов (мозг, сердце, почки). После того, как артериальное давление падает ниже критического порога, тканевая перфузия линейно уменьшается. Этот критический порог может варьироваться в зависимости от систем органов и индивидуумов и, отсюда, целевое значение АДср может быть персонализирована на основе глобальной и региональной перфузии с учетом темпа диуреза, психического статуса или клиренса лактата [50].
Решения по выбору режима дозирования вазопрессоров для достижения целевого значения АДср должны быть приняты с учетом потенциальных побочных эффектов, включая сюда аритмии, сердечно-сосудистые события и ишемию.
Вазопрессор первой линии - Норэпинефрин (Норадреналин)
Было проведено несколько крупных многоцентровых рандомизированных контролируемых исследований для определения наиболее эффективных вазоактивных агентов первой линии и дополнительных вазоагентов при септическом шоке. Норадреналин показал лучшую выживаемость пациентов с меньшим риском развития аритмии по сравнению с дофамином [51-53]. С другой стороны, два систематических обзора не выявили различий в клинических исходах и летальности при применении норадреналина по сравнению с адреналином, вазопрессином, терлипрессином или фенилэфрином [53, 54].
Не имея убедительных доказательств в поддержку других препаратов в качестве терапии первой линии при септическом шоке, для достижения целевого среднего артериального давления норэпинефрин остается предпочтительным вазопрессором и настоятельно рекомендуется к применению в рекомендациях клинического руководства the Surviving Sepsis Campaign, хотя эти рекомендации подтверждаются доказательствами среднего качества [17, 55].
Добавление второго вазопрессора или инотропа
Для достижения целевого значения АДср или для снижения потребности в норэпинефрине можно применять другое симпатомиметическое лекарственное средство, такое как вазопрессин или адреналин. Второй вазопрессор обычно добавляют, когда дозы норэпинефрина превышают 40 или 50 мкг/мин.
Вазопрессин. Септический шок связан с относительным дефицитом вазопрессина. Было показано, что добавление вазопрессина в качестве заместительного гормона оказывает «щадящее действие» в виде снижения дозы норэпинефрина. Рандомизированное контролируемое исследование, в котором сравнивались монотерапия вазопрессином с терапией сочетанием норэпинефрина и вазопрессина, не показала каких-либо преимуществ в плане выживания или снижения частоты развития почечной недостаточности [56,57]. Доказательства, подтверждающие применение вазопрессина в качестве препарата первого ряда и его преимущества над норадреналином остаются ограниченными, но в виде дополнения к норадреналину вазопрессин остается предпочтительным [56,57].
Адреналин рекомендуется к применению в соответствии с клиническими рекомендациями the Surviving Sepsis Campaign в качестве вазопрессора второго ряда. Он обладает мощной альфа- и бета-адренергической активностью, которая увеличивает среднее артериальное давление за счет увеличения сердечного выброса и вазомоторного тонуса. Применение адреналина ограничивает значительный риск развития тахикардии, аритмии и транзиторного лактоацидоза.
Допамин - применение при сепсисе не рекомендуется из-за склонности допамина вызывать тахиаритмию, тем самым резко ухудшать клинические результаты [51,52].
Фенилэфрин является чистым альфа-адренергическим агонистом, который применяется при септическом шоке, хотя и с ограниченными данными о его эффективности и безопасности. Vail et al. [59] в своем многоцентровом когортном исследовании, проведенном во время нехватки норэпинефрина, обнаружили увеличение летальности, связанной с применением фенилэфрина при септическом шоке. Применение фенилэфрина должно быть ограничено септическим шоком, осложненным значительной тахиаритмией, или в качестве дополнения к рефрактерному вазодилататорному шоку до тех пор, пока не появится больше доказательств его пользы.
Ангиотензин II недавно был одобрен в качестве вазопрессора для применения при септическом шоке. Он активирует рецепторы ангиотензина типа 1a и 1b, что увеличивает уровень внутриклеточного кальция в гладких мышцах, что способствует вазоконстрикции. Клинические данные, связанные с его применением, ограничены недавним исследованием, которое показало, что добавление ангиотензина II улучшало артериальное давление у пациентов с рефрактерным вазодилататорным шоком, получающих высокие дозы вазопрессоров [60]. До сих пор нет данных о его безопасности, а его точная роль в алгоритмах лечения рефрактерного шока все еще не определена.
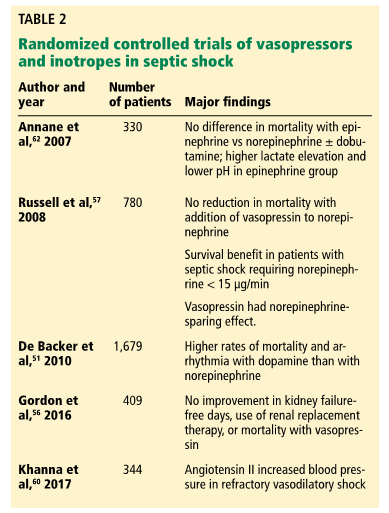
Инотропные агенты могут потребоваться пациентам с недостаточным сердечным выбросом после интенсивной инфузионной терапии из-за вызванной сепсисом кардиомиопатии или комбинированного шока. Данные, которые бы свидетельствовали об оптимальном инотропном действии при септическом шоке, ограничены, но наиболее часто применяются адреналин и добутамин [61,62]. Сравнение норэпинефрина и добутамина с адреналином при септическом шоке не выявило различий в летальности, частоте развития побочных эффектов или продолжительности шока [62]. Изучались милринон и левосимендан (не одобрен в США) с ограниченными данными в поддержку их применения вместо добутамина [63,64]. Реакция на применение инотропов должна контролироваться путем измерения изменений сердечного выброса, насыщения центральной венозной крови кислородом или других показателей перфузии тканей (Таблица 2).
Роль кортикостероидов все еще под вопросом
Кортикостероиды подавляют чрезмерную воспалительную реакцию, наблюдаемую при сепсисе, и помогают справиться с относительной недостаточностью надпочечников, вызванной супрессией надпочечников или резистентностью тканей к глюкокортикоидам [65]. При септическом шоке они играют сосудорасширяющую роль и сокращают продолжительность шока, длительность ИВЛ и время пребывания пациента в ОИТ.
Тем не менее, убедительных доказательств того, что применение кортикостероидов при сепсисе улучшает клинические исходы или выживаемость, нет [66–71], поэтому их применение при сепсисе или тяжелом сепсисе не рекомендуется в случаях, когда для восстановления гемодинамической стабильности достаточно интенсивной инфузионной терапии и вазопрессорной поддержки. Чаще кортикостероиды могут применяться в качестве дополнительной терапии пациентов, которым требуются более высокие дозы вазопрессоров [17,65].
В исследованиях неблагоприятные эффекты от применения кортикостероидов ограничиваются гипергликемией, гипернатриемией и гипертензией без увеличения частоты развития суперинфекций [71]. Ограниченные побочные эффекты, наряду с единообразной демонстрацией более короткой продолжительности шока, продолжительности ИВЛ и продолжительности пребывания в ОИТ, позволяют предположить, что стероиды могут играть свою роль в интенсивной терапии рефрактерного септического шока [66–69].
Если принято решение о применении кортикостероидов при септическом шоке, то современные рекомендации рекомендуют вводить гидрокортизон в дозе 200 мг в сутки внутривенно либо в виде непрерывной инфузии, либо болюсным введением по 50 мг 4 раза/сутки в течение не менее трех дней, дозировки даны на основании систематического обзора, показывающего, что более длительный курс приема низких доз стероидов связан с более низким уровнем летальности [72]. Нет четкого консенсуса относительно того, следует ли постепенно снижать дозы стероидов или целесообразно резкое прекращение их введения, так как в более крупных рандомизированных клинических исследованиях не применялась стратегия постепенного снижения их дозы и не было обнаружено различий в рецидиве шока [66,67]. В большинстве случаев стероиды прекращают вводить после прекращения введения вазопрессоров [65].
Дальнейшие исследования должны быть сосредоточены на правильном выборе времени начала введения глюкокортикоидов после начала шока и сравнении режима с фиксированной продолжительностью с режимом, управляемым по клинической картине.
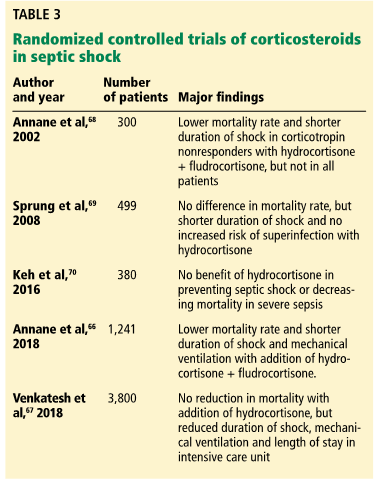
Этомидат в качестве индукционного агента при интубации трахеи ассоциируется с подавлением синтеза кортизола и снижением реакции на экзогенные стероиды. Влияет ли это на результаты, неясно. Тем не менее, клиницисты должны соблюдать особую осторожность при применении этоцидата при септическом шоке (Таблица 3) [73].
Биомаркеры
Биомаркеры помогают в ранней диагностики сепсиса, выявляют пациентов с высоким риском его развития и следят за прогрессированием заболевания, облегчая определение целей интенсивной терапии с большей степенью персонализации.
C-реактивный белок и скорость оседания эритроцитов использовались в прошлом, но с ограниченным успехом [74].
Прокальцитонин помогает на раннем этапе выявлять бактериальные инфекции и направляет де-эскалацию или отмену антибиотиков [75,76]. Управляемая по уровню прокальцитонина де-эскалация антибиотиков сокращает продолжительность воздействия антибиотиков с тенденцией к снижению летальности [77,78].
Galactomannan и beta-D-glucan могут применяться для выявления грибковых инфекций, особенно Aspergillus. Beta-d-glucan более чувствителен к инвазивному аспергиллезу, в то время как galactomannan более специфичен [79].
Цитокины, такие как интерлейкины (например, IL6, IL-8, IL-10), фактор некроза опухоли альфа, белки острой фазы и молекулы рецептора в настоящее время изучаются для определения их полезности при лечении сепсиса.
Ограничения в чувствительности и специфичности отдельных биомаркеров может быть преодолена с помощью комбинаций биомаркеров, что в настоящее время является предметом исследований [80]. На данный момент решение о начале эскалации и де-эскалации проводимой терапии должно основываться на клинической оценке, при этом прокальцитонин или другие биомаркеры применяются в качестве дополнения к другим клиническим факторам [17].
Стандартная терапия против протоколов инициации интенсивной терапии
В 2001 году Rivers et al. [61] сравнили стандартную интенсивную терапию при тяжелом сепсисе или септическом шоке с целенаправленной терапией, использующей протокол, при этом в качестве целей использовались физиологические конечные точки. Они обнаружили значительно более низкий уровень летальности в группе целенаправленной терапии. Этот вывод сильно повлиял развитие целенаправленной стратегии управления, рекомендованную the Surviving Sepsis Campaign в 2004 году.
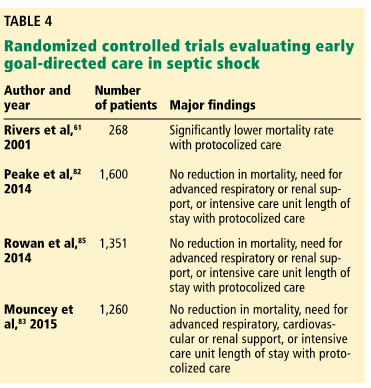
Однако с тех пор терапия на основании протокола была оспорена, а в трех крупных многоцентровых исследованиях было установлено, что при сепсисе стандартная терапия не уступает терапии по протоколу, без различий в летальности или продолжительности пребывания [82–84]. Более того, стандартная терапия ассоциировалась со значительным снижением потребности в центральном сосудистом доступе, переливании крови и во введении добутамина. Мета-анализ, проведенный в в 138 больницах в 7 странах, в котором приняли участие около 4000 пациентов, показал, что стандартная терапия с упором на раннее выявление сепсиса и быстрое проведение соответствующей антимикробной терапии при адекватной инфузионой терапии не только эквивалентна терапии по протоколу, но и является более рентабельной [85]. (Таблица 4).
Применимы ли сейчас критерии «Сепсис-1»?
В январе 2013 года штат Нью-Йорк обязал все больницы штата начать процессы раннего выявления и лечения сепсиса. В октябре 2015 года the National Quality Forum и CMS внедрили эти процессы по всей стране [7]. Полученный показатель качества CMS по критериям SEP-1 стандартизирует раннее управление тяжелым сепсисом и септическим шоком с целью улучшения результатов. Элементы протокола основаны на клиническом руководстве the Surviving Sepsis Campaign и состоят из серии шагов, которые необходимо выполнить в течение 3-х и 6-ти часов после распознавания сепсиса.
Шаги в алгоритме, которые должны быть выполнены в течение 3 часов, включают в себя измерение уровня лактата в сыворотке крови, взятие посевов крови и введение соответствующих антибиотиков, интенсивную инфузионную терапию и вазопрессорную поддержку, если это необходимо. Уровень лактата повторяется в течение 6 часов, необходимо провести статическую и динамическую оценку перфузии, чтобы определить потребность в дополнительной инфузии жидкости или в продолжении вазопрессорной поддержки для улучшения перфузии конечных органов.
Результаты работы больниц по критериям SEP-1 общедоступны на веб-сайте CMS (medicare.gov/hospitalcompare/search.html?) и могут быть использованы для финансовых стимулов, ориентированных на показатели соответствия требованиям SEP-1 [86].
Несмотря на то, что критерии SEP-1 были приняты в качестве показателя качества лечения, некоторые исследователи ставят под сомнение его клиническую значимость, поскольку многие из основных рекомендаций не подтверждаются убедительными доказательствами [86,87]. В трех основных исследованиях было установлено, что уровень летальности при лечении сепсиса на основании протокола был не ниже уровня летальности при проведении стандартной терапии [82–84]. Seymour et al. [28] собрав данные Департамента здравоохранения штата Нью-Йорк по 49 331 пациентам с сепсисом и септическим шоком, обнаружили, что более быстрое завершение 3-х часового алгоритма - особенно назначения антибиотиков, но не завершения инфузионной терапии - ассоциировалось со снижением внутрибольничной летальности. Многоцентровое ретроспективное когортное исследование [88] показало, что несоответствие критериям SEP-1 для любого этапа, кроме введения антибиотиков, не приводит к плохим результатам.
Основная проблема, связанная с введением SEP-1, заключается в том, что будет чрезмерно назначаться как инфузионная терапия, так и антибиотики широкого спектра действия, поскольку системы здравоохранения будут пытаться выполнить все предписанные CMS меры качества лечения. Но неизбирательное использование таких методов лечения может не только нанести вред пациенту, но и создать чрезмерную нагрузку на ресурсы здравоохранения [89].
Призыв к совершенствованию клинического руководства
Сепсис является многофакторным заболеванием, а его лечение остается сложным. Необходимы упрощенные клинические рекомендации и показатели качества лечения, основанные на достоверных данных. Электронные системы медицинской документации обещают помочь в раннем и точном обнаружении сепсиса и могут сыграть важную роль [90,91]. Еще одним подходом к лечению сепсиса являются чек-листы (контрольные списки), которые позволяют лицам, осуществляющим лечение пациентов, применить свою клиническую проницательность. Успех инициатив по оптимальной терапии требует постоянных и совместных попыток улучшения качества лечения по различным специальностям в медицине, сестринском деле и в административной работе [92].


