Array
(
[NAME] => Пять новых реалий в интенсивной терапии у онкологических больных
[~NAME] => Пять новых реалий в интенсивной терапии у онкологических больных
[PREVIEW_PICTURE] => Array
(
[ID] => 5216
[TIMESTAMP_X] => 11.11.2024 15:10:27
[MODULE_ID] => iblock
[HEIGHT] => 3744
[WIDTH] => 5616
[FILE_SIZE] => 10408858
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4
[FILE_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[ORIGINAL_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 6fe7e2c05db92a6ccf46d467ca55498f
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4/medical-banner-with-doctor-holding-tablet.jpg
[UNSAFE_SRC] => /upload/iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4/medical-banner-with-doctor-holding-tablet.jpg
[SAFE_SRC] => /upload/iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4/medical-banner-with-doctor-holding-tablet.jpg
[ALT] => Пять новых реалий в интенсивной терапии у онкологических больных
[TITLE] => Пять новых реалий в интенсивной терапии у онкологических больных
)
[~PREVIEW_PICTURE] => 5216
[DETAIL_TEXT] =>
Guillaume Dumas, Stephen M. Pastores and Laveena Munshi Five new realities in criticalcare for patients with cancer
Пять новых реалий в интенсивной терапии у онкологических больных
Intensive Care Med 2023 doi.org/10.1007/s00134-023-06988-y
Опасные для жизни осложнения возникают у 5–10% больных раком, требующих госпитализации в отделение интенсивной терапии (ОИТ). Несколько факторов, таких как осложнения, связанные с самим заболеванием или индуцированные химиотерапией, делают эту популяцию уникальной. В эту эпоху быстрых изменений в онкологии понимание особенностей таких пациентов имеет решающее значение для определения клинического подхода. В этой статье мы выделяем пять новых реалий в лечении рака для реаниматологов.
Серьезное заболевание на запущенной стадии рака больше не означает конец жизни
Исторически госпитализация в ОИТ пациентов с распространенным раком (метастатическим солидным раком, гематологическими злокачественными новообразованиями высокой степени злокачественности) была связана с неблагоприятными исходами [1, 2]. Это было обусловлено (1) плохим функциональным статусом, (2) осторожным долгосрочным прогнозом или (3) критическим заболеванием из-за прогрессирования неизлечимого рака. Однако сейчас подход стал более сложным, поскольку был достигнут значительный прогресс в диагностике, классификации и лечении рака. Это позволило удвоить продолжительность жизни многих онкологических больных. Ранее неизлечимые виды злокачественных опухолей, такие как меланома или рефрактерная лимфома, теперь подвержены эффективной продлевающей жизнь терапии, приводящую к устойчивому контролю над раком. Реаниматологи должны учитывать эти новые реалии, чтобы адаптировать тактику в отношении данных пациентов.
При рассмотрении показаний для госпитализации в ОИТ есть несколько факторов, уникальных для пациентов с раком. (1) Прогноз в ОИТ в основном определяется диагнозом пациента, обусловившим развитие критического состояния и количеством пораженных органов, а не характеристиками рака. Если причина критического состояния быстро обратима (например, желудочно-кишечное кровотечение и катетер-ассоциированная инфекция кровотока) и отсутствуют обычные неблагоприятные прогностические признаки (например, выраженная старческая астения «хрупкость»), следует рассмотреть вопрос о госпитализации в ОИТ. Это решение должно учитывать ценности, предпочтения и ожидания пациента в отношении госпитализации, чтобы гарантировать, что мы оказываем целенаправленную помощь. (2) И наоборот, существуют специфические связанные с раком состояния, которые имеют очень плохой прогноз (например, легочно-лимфангитный карциноматоз e-Table-1; Supplemental appendix ).
Подобно состоянию «хрупкости», когда эти состояния присутствуют, независимо от причины критического состояния, выживаемость после лечения в ОИТ может быть мало вероятной, и следует рассмотреть паллиативный подход. (3) Наконец, при критических состояниях, связанных с более интенсивной поддержкой органов (например, инвазивная вентиляция легких) на поздних стадиях рака, крайне важно понимать прогноз рака у пациента, существуют ли поддерживающие жизнь методы лечения рака и влияние, которое критическое заболевание может оказать на конкретного пациента. Ограниченное по времени испытание в ОИТ (section-4) может быть рассмотрено в случаях, когда существует вероятность выживания в и возвращения к лечению рака после пребывания в ОИТ.
Новые методы лечения рака меняют результаты лечения пациентов, создавая новые болезни
Таргетная терапия произвела революцию в онкологии и все чаще используется в качестве терапии первой линии при некоторых видах рака. Интенсивисты должны знать о механизмах действия препаратов и токсичности (Fig. 1). В зависимости от класса лекарств нередки случаи тяжелой токсичности, включая пневмонит и нейротоксичность [1]. При некоторых видах терапии в рамках курса лечения можно ожидать развитие критического состояния, например тяжелого синдрома высвобождения цитокинов после инфузии химерных антигенных рецепторов-Т-клеток (CAR-T) (15–23%). Большинство этих проявлений токсичности можно смягчить введением кортикостероидов/иммунодепрессантов [1].
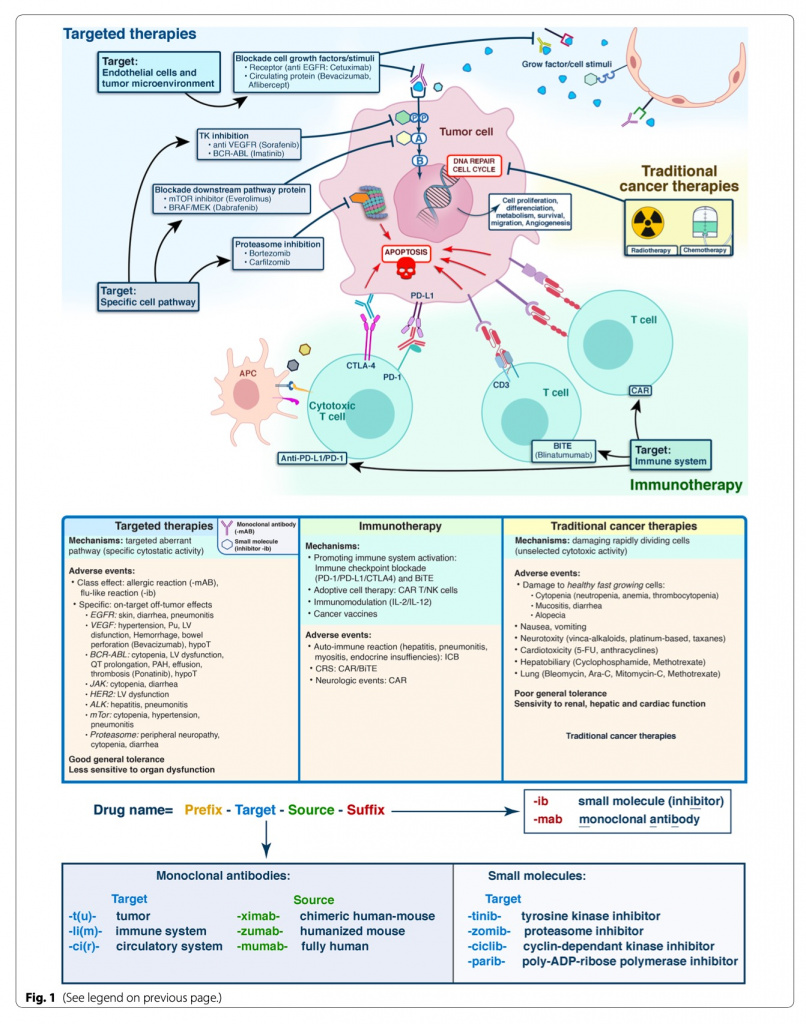
Важно отметить, что такие осложнения не обязательно являются противопоказанием к повторному назначению препарата или альтернативных классов. В отличие от традиционной химиотерапии, некоторые новые методы лечения могут быть предложены при органных дисфункциях, а некоторые показали быстрый регресс опухоли даже у пациентов в критическом состоянии. Более того, воздействуя на специфический путь, участвующий в патофизиологии рака, новые методы лечения продемонстрировали лучшую переносимость по сравнению с химиотерапией. Интенсивисты должны быть осведомлены об атипичных паттернах ответа, таких как псевдопрогрессия рака (определяемая как начальное увеличение объема опухоли в ответ на лечение), которая может привести к транзиторным локальным и (или) регионарным осложнениям и не должна быть ошибочно принята за неэффективность лечения [3].
Наконец, хотя количество новых методов лечения увеличивается, а траектории пациентов становятся более сложными (сочетание методов лечения одновременно/через некоторое время), вполне вероятно, что новые связанные с препаратами заболевания будут проявляться как критические состояния, и ОИТ могут использоваться для постановке диагноза или сыграть роль в разработке стратегии лечения.
Нам нужно по-новому взглянуть на острую дыхательную недостаточность
С 1990-х годов смертность от острой дыхательной недостаточности (ОДН) резко снизилась. Однако инвазивная вентиляция продолжает ассоциироваться с высокой смертностью (50–60%) при сохраняющемся разрыве у больных с раком при отсутствии онкологического заболевания [4, 5]. Существует несколько возможностей для дальнейших исследований (1) более глубокое понимание механизмов ОДН при раке необходимо для разработки терапевтических целей, (2) неопределенная ОДН остается высокой, и необходимы стратегии для улучшения диагностических возможностей (инфекционные по сравнению с неинфекционными), (3) идентификация субфенотипов необходима для продвижения поддерживающей терапии и заложения основы для таргетной терапии ОДН.
В рамках ОДН были идентифицированы субфенотипы (например, гипо/гипервоспалительные). Эти субфенотипы, вероятно, по-разному реагируют на лечение. В то время как сообщество по изучению ОДН продвигает эту исследовательскую программу вперед, важно, чтобы пациенты с ослабленным иммунитетом/раком были включены в этот анализ. Исторически сложилось так, что исследования ОДН грубо разделяли анализы на «иммунокомпрометированные» и «неиммунокомпрометированные»; однако идентификация субфенотипа, вероятно, является более сложной. Идентификация субфенотипа может быть важным следующим шагом для информирования терапевтических целей при ОДН.
Цели лечения и ограниченное по времени испытание
Эффективная коммуникация между ОИТ и онкологии необходима для обеспечения надлежащей эскалации и ограничения. Вероятно, существуют большие различия в клинической практике в зависимости от географических районов, убеждений врачей и подтипов рака. Учитывая отсутствие надежных показателей тяжести заболевания для прогнозирования исходов онкологических больных, решение о госпитализации в ОРИТ должно приниматься в индивидуальном порядке. Это решение должно учитывать ценности/предпочтения пациентов, прогноз критического состояния и ожидаемый долгосрочный исход рака (с правом на продолжение лечения рака и без него).
Решение о госпитализации в ОИТ часто бывает простым для пациента, получающего радикальное лечение. Однако в литературе отсутствует ясность в отношении политики госпитализации в эпоху новых противораковых препаратов для пациентов с распространенным раком. Новые методы лечения, такие как инфузия CAR-T-клеток, предполагают высокий риск развития критического состояния, и госпитализация в ОИТ может считаться частью проведения специфического лечения. С другой стороны, среди пациентов, получавших другие таргетные методы лечения, существуют неопределенности в отношении динамики состояния пациентов и того, как госпитализация в ОИТ может повлиять на их право на лечение в будущем. Учитывая это, в начале 2000-х годов было предложено «ICU time-limited trial» (TLT) [6] для интеграции таких неопределенностей в процессе принятия решений.
Эта политика госпитализации может быть определена как соглашение между всеми заинтересованными сторонами (т. е. пациентом, семьей, онкологом и реаниматологом) о типах расширенной органной поддержки в течение ограниченного периода времени для оценки вероятности выздоровления. Чтобы это было успешным, необходимо тесное сотрудничество между отделениями интенсивной терапии и онкологии, чтобы наилучшим образом информировать о полезности пребывания в ОИТ. В настоящее время оптимальное количество дней TLT плохо определено (в основном колеблется от 5 до 7 дней для солидных опухолей, но, возможно, до 14 дней для гематологических злокачественных новообразований) [7]. Количество отказавших органов может изменить продолжительность. Следует также добиваться внедрения высококачественной паллиативной помощи в ОИТ. Необходимы дальнейшие исследования, чтобы определить TLT для различных подтипов рака и показаний для госпитализации в ОИТ.
Пришло время выйти за рамки ОИТ
Смертность в ОИТ снизилась с 80–90% в исторических отчетах до 30–50% [5, 8]. Однако этот обнадеживающий прогресс обычно уравновешивается более разочаровывающими сообщениями о долгосрочной выживаемости (> 3 месяцев) в диапазоне от 25 до 55% с частым и стойким снижением качества жизни после выписки из ОИТ [1, 3, 9,10]. На сегодняшний день лишь несколько исследований посвящены долгосрочной выживаемости после выписки из ОИТ у онкологических больных [2, 8, 11–13]. Мы должны сместить наше внимание на определение влияния критического заболевания на лечение рака и долгосрочный прогноз рака после лечения в ОИТ в дополнение к исходам, ориентированным на пациента, таким как функциональные, когнитивные и симптоматические нарушения после пребывания в ОИТ.
Этот сдвиг согласуется с усилиями интенсивистов по характеристике бремени ПИТ-синдрома. Существует сложное взаимодействие между интенсивной терапией и онкологией, которое нельзя экстраполировать на пациентов, не страдающих раком. Дополнительные соображения включают право на поддерживающее жизнь или излечивающее лечение рака после выздоровления от критического заболевания. Крайне важно, чтобы мы понимали (до госпитализации в ОИТ): (1) доступные методы лечения рака, (2) применялись ли они, и (3) как выздоровление от критического заболевания влияет на возможность продолжения лечения от рака.
Нам необходимо оценить детерминанты возвращения к лечению после ОИТ (функциональное состояние, прогрессирование заболевания, персистирующая органная дисфункция и предпочтения пациента), чтобы обеспечить принятие решения врачом и пациентом. Это необходимо для обоснования будущих исследований потенциальных методов лечения для оптимизации этих факторов в будущем.
Ссылка на документ с дополнительными данными исследования (Supplementary)
References
1. Joseph A, Simonaggio A, Stoclin A et al (2020) Immune‑related adverse events: a retrospectivelook into the future of oncology in the intensive care unit. Ann Intensive Care 10:143. https://doi.org/10.1186/ s13613‑020‑00761‑w
2. Ehooman F, Biard L, Lemiale V et al (2019) Long‑term health‑related quality of life of criticallyill patients with haematological malignancies: a prospective observational multicenter study. Ann Intensive Care 9:2. https://doi.org/10.1186/s13613‑018‑0478‑3
3. Chiou VL, Burotto M (2015) Pseudoprogression and immune‑related response in solid tumors. J Clin Oncol 33:3541–3543. https://doi.org/10. 1200/JCO.2015.61.6870
4. Cortegiani A, Madotto F, Gregoretti C et al (2018) Immunocompromised patients with acuterespiratory distress syndrome: secondary analysis of the LUNG SAFE database. Crit Care 22:157
5. Azoulay E, Pickkers P, Soares M et al (2017) Acute hypoxemic respiratory failure inimmunocompromised patients: the Efraim multinational prospective cohort study. Intensive Care Med 43:1808–1819. https://doi. org/10.1007/s00134‑017‑4947‑1
6. Vink EE, Azoulay E, Caplan A et al (2018) Time‑limited trial of intensive care treatment: an overview of current literature. Intensive Care Med 44:1369–1377.https://doi.org/10.1007/s00134‑018‑5339‑x
7. Shrime MG, Ferket BS, Scott DJ et al (2016) Time‑limited trials of intensive care for critically ill patients with cancer: how long is long enough? JAMA Oncol 2:76–83.https://doi.org/10.1001/jamaoncol.2015.3336
8. Borcoman E, Dupont A, Mariotte E et al (2020) One‑year survival in patients with solid tumoursdischarged alive from the intensive care unit after unplanned admission: a retrospective study. J Crit Care 57:36–41. https://doi.org/10.1016/j.jcrc.2020.01.027
9. Ferreyro BL, Scales DC, Wunsch H et al (2021) Critical illness in patients with hematologicmalignancy: a population‑based cohort study. Intensive Care Med 47:1104–1114. https://doi.org/10.1007/ s00134‑021‑06502‑2
10. Darmon M, Bourmaud A, Georges Q et al (2019) Changes in critically ill cancer patients’ short‑term outcome over the last decades: results of systematic review with meta‑analysis onindividual data. Intensive Care Med 45:977–987. https://doi.org/10.1007/s00134‑019‑05653‑7
11. Bernal T, Pardavila EV, Bonastre J et al (2013) Survival of hematological patients after discharge from the intensive care unit: a prospective obser‑ vational study. Crit Care.https://doi.org/10.1186/cc13172
12. Vigneron C, Charpentier J, Wislez M et al (2021) Short‑term and long‑term outcomes ofpatients with lung cancer and life‑threatening complications. Chest 160:1560–1564.https://doi.org/10.1016/j.chest.2021.04.056
13. Soares M, Salluh JIF, Ferreira CG et al (2005) Impact of two different comorbidity measures onthe 6‑month mortality of critically ill cancer patients. Intensive Care Med 31:408–415.https://doi.org/10.1007/ s00134‑005‑2554‑z
Источник фотоиллюстрации - www.freepik.com
[~DETAIL_TEXT] =>
Guillaume Dumas, Stephen M. Pastores and Laveena Munshi Five new realities in criticalcare for patients with cancer
Пять новых реалий в интенсивной терапии у онкологических больных
Intensive Care Med 2023 doi.org/10.1007/s00134-023-06988-y
Опасные для жизни осложнения возникают у 5–10% больных раком, требующих госпитализации в отделение интенсивной терапии (ОИТ). Несколько факторов, таких как осложнения, связанные с самим заболеванием или индуцированные химиотерапией, делают эту популяцию уникальной. В эту эпоху быстрых изменений в онкологии понимание особенностей таких пациентов имеет решающее значение для определения клинического подхода. В этой статье мы выделяем пять новых реалий в лечении рака для реаниматологов.
Серьезное заболевание на запущенной стадии рака больше не означает конец жизни
Исторически госпитализация в ОИТ пациентов с распространенным раком (метастатическим солидным раком, гематологическими злокачественными новообразованиями высокой степени злокачественности) была связана с неблагоприятными исходами [1, 2]. Это было обусловлено (1) плохим функциональным статусом, (2) осторожным долгосрочным прогнозом или (3) критическим заболеванием из-за прогрессирования неизлечимого рака. Однако сейчас подход стал более сложным, поскольку был достигнут значительный прогресс в диагностике, классификации и лечении рака. Это позволило удвоить продолжительность жизни многих онкологических больных. Ранее неизлечимые виды злокачественных опухолей, такие как меланома или рефрактерная лимфома, теперь подвержены эффективной продлевающей жизнь терапии, приводящую к устойчивому контролю над раком. Реаниматологи должны учитывать эти новые реалии, чтобы адаптировать тактику в отношении данных пациентов.
При рассмотрении показаний для госпитализации в ОИТ есть несколько факторов, уникальных для пациентов с раком. (1) Прогноз в ОИТ в основном определяется диагнозом пациента, обусловившим развитие критического состояния и количеством пораженных органов, а не характеристиками рака. Если причина критического состояния быстро обратима (например, желудочно-кишечное кровотечение и катетер-ассоциированная инфекция кровотока) и отсутствуют обычные неблагоприятные прогностические признаки (например, выраженная старческая астения «хрупкость»), следует рассмотреть вопрос о госпитализации в ОИТ. Это решение должно учитывать ценности, предпочтения и ожидания пациента в отношении госпитализации, чтобы гарантировать, что мы оказываем целенаправленную помощь. (2) И наоборот, существуют специфические связанные с раком состояния, которые имеют очень плохой прогноз (например, легочно-лимфангитный карциноматоз e-Table-1; Supplemental appendix ).
Подобно состоянию «хрупкости», когда эти состояния присутствуют, независимо от причины критического состояния, выживаемость после лечения в ОИТ может быть мало вероятной, и следует рассмотреть паллиативный подход. (3) Наконец, при критических состояниях, связанных с более интенсивной поддержкой органов (например, инвазивная вентиляция легких) на поздних стадиях рака, крайне важно понимать прогноз рака у пациента, существуют ли поддерживающие жизнь методы лечения рака и влияние, которое критическое заболевание может оказать на конкретного пациента. Ограниченное по времени испытание в ОИТ (section-4) может быть рассмотрено в случаях, когда существует вероятность выживания в и возвращения к лечению рака после пребывания в ОИТ.
Новые методы лечения рака меняют результаты лечения пациентов, создавая новые болезни
Таргетная терапия произвела революцию в онкологии и все чаще используется в качестве терапии первой линии при некоторых видах рака. Интенсивисты должны знать о механизмах действия препаратов и токсичности (Fig. 1). В зависимости от класса лекарств нередки случаи тяжелой токсичности, включая пневмонит и нейротоксичность [1]. При некоторых видах терапии в рамках курса лечения можно ожидать развитие критического состояния, например тяжелого синдрома высвобождения цитокинов после инфузии химерных антигенных рецепторов-Т-клеток (CAR-T) (15–23%). Большинство этих проявлений токсичности можно смягчить введением кортикостероидов/иммунодепрессантов [1].

Важно отметить, что такие осложнения не обязательно являются противопоказанием к повторному назначению препарата или альтернативных классов. В отличие от традиционной химиотерапии, некоторые новые методы лечения могут быть предложены при органных дисфункциях, а некоторые показали быстрый регресс опухоли даже у пациентов в критическом состоянии. Более того, воздействуя на специфический путь, участвующий в патофизиологии рака, новые методы лечения продемонстрировали лучшую переносимость по сравнению с химиотерапией. Интенсивисты должны быть осведомлены об атипичных паттернах ответа, таких как псевдопрогрессия рака (определяемая как начальное увеличение объема опухоли в ответ на лечение), которая может привести к транзиторным локальным и (или) регионарным осложнениям и не должна быть ошибочно принята за неэффективность лечения [3].
Наконец, хотя количество новых методов лечения увеличивается, а траектории пациентов становятся более сложными (сочетание методов лечения одновременно/через некоторое время), вполне вероятно, что новые связанные с препаратами заболевания будут проявляться как критические состояния, и ОИТ могут использоваться для постановке диагноза или сыграть роль в разработке стратегии лечения.
Нам нужно по-новому взглянуть на острую дыхательную недостаточность
С 1990-х годов смертность от острой дыхательной недостаточности (ОДН) резко снизилась. Однако инвазивная вентиляция продолжает ассоциироваться с высокой смертностью (50–60%) при сохраняющемся разрыве у больных с раком при отсутствии онкологического заболевания [4, 5]. Существует несколько возможностей для дальнейших исследований (1) более глубокое понимание механизмов ОДН при раке необходимо для разработки терапевтических целей, (2) неопределенная ОДН остается высокой, и необходимы стратегии для улучшения диагностических возможностей (инфекционные по сравнению с неинфекционными), (3) идентификация субфенотипов необходима для продвижения поддерживающей терапии и заложения основы для таргетной терапии ОДН.
В рамках ОДН были идентифицированы субфенотипы (например, гипо/гипервоспалительные). Эти субфенотипы, вероятно, по-разному реагируют на лечение. В то время как сообщество по изучению ОДН продвигает эту исследовательскую программу вперед, важно, чтобы пациенты с ослабленным иммунитетом/раком были включены в этот анализ. Исторически сложилось так, что исследования ОДН грубо разделяли анализы на «иммунокомпрометированные» и «неиммунокомпрометированные»; однако идентификация субфенотипа, вероятно, является более сложной. Идентификация субфенотипа может быть важным следующим шагом для информирования терапевтических целей при ОДН.
Цели лечения и ограниченное по времени испытание
Эффективная коммуникация между ОИТ и онкологии необходима для обеспечения надлежащей эскалации и ограничения. Вероятно, существуют большие различия в клинической практике в зависимости от географических районов, убеждений врачей и подтипов рака. Учитывая отсутствие надежных показателей тяжести заболевания для прогнозирования исходов онкологических больных, решение о госпитализации в ОРИТ должно приниматься в индивидуальном порядке. Это решение должно учитывать ценности/предпочтения пациентов, прогноз критического состояния и ожидаемый долгосрочный исход рака (с правом на продолжение лечения рака и без него).
Решение о госпитализации в ОИТ часто бывает простым для пациента, получающего радикальное лечение. Однако в литературе отсутствует ясность в отношении политики госпитализации в эпоху новых противораковых препаратов для пациентов с распространенным раком. Новые методы лечения, такие как инфузия CAR-T-клеток, предполагают высокий риск развития критического состояния, и госпитализация в ОИТ может считаться частью проведения специфического лечения. С другой стороны, среди пациентов, получавших другие таргетные методы лечения, существуют неопределенности в отношении динамики состояния пациентов и того, как госпитализация в ОИТ может повлиять на их право на лечение в будущем. Учитывая это, в начале 2000-х годов было предложено «ICU time-limited trial» (TLT) [6] для интеграции таких неопределенностей в процессе принятия решений.
Эта политика госпитализации может быть определена как соглашение между всеми заинтересованными сторонами (т. е. пациентом, семьей, онкологом и реаниматологом) о типах расширенной органной поддержки в течение ограниченного периода времени для оценки вероятности выздоровления. Чтобы это было успешным, необходимо тесное сотрудничество между отделениями интенсивной терапии и онкологии, чтобы наилучшим образом информировать о полезности пребывания в ОИТ. В настоящее время оптимальное количество дней TLT плохо определено (в основном колеблется от 5 до 7 дней для солидных опухолей, но, возможно, до 14 дней для гематологических злокачественных новообразований) [7]. Количество отказавших органов может изменить продолжительность. Следует также добиваться внедрения высококачественной паллиативной помощи в ОИТ. Необходимы дальнейшие исследования, чтобы определить TLT для различных подтипов рака и показаний для госпитализации в ОИТ.
Пришло время выйти за рамки ОИТ
Смертность в ОИТ снизилась с 80–90% в исторических отчетах до 30–50% [5, 8]. Однако этот обнадеживающий прогресс обычно уравновешивается более разочаровывающими сообщениями о долгосрочной выживаемости (> 3 месяцев) в диапазоне от 25 до 55% с частым и стойким снижением качества жизни после выписки из ОИТ [1, 3, 9,10]. На сегодняшний день лишь несколько исследований посвящены долгосрочной выживаемости после выписки из ОИТ у онкологических больных [2, 8, 11–13]. Мы должны сместить наше внимание на определение влияния критического заболевания на лечение рака и долгосрочный прогноз рака после лечения в ОИТ в дополнение к исходам, ориентированным на пациента, таким как функциональные, когнитивные и симптоматические нарушения после пребывания в ОИТ.
Этот сдвиг согласуется с усилиями интенсивистов по характеристике бремени ПИТ-синдрома. Существует сложное взаимодействие между интенсивной терапией и онкологией, которое нельзя экстраполировать на пациентов, не страдающих раком. Дополнительные соображения включают право на поддерживающее жизнь или излечивающее лечение рака после выздоровления от критического заболевания. Крайне важно, чтобы мы понимали (до госпитализации в ОИТ): (1) доступные методы лечения рака, (2) применялись ли они, и (3) как выздоровление от критического заболевания влияет на возможность продолжения лечения от рака.
Нам необходимо оценить детерминанты возвращения к лечению после ОИТ (функциональное состояние, прогрессирование заболевания, персистирующая органная дисфункция и предпочтения пациента), чтобы обеспечить принятие решения врачом и пациентом. Это необходимо для обоснования будущих исследований потенциальных методов лечения для оптимизации этих факторов в будущем.
Ссылка на документ с дополнительными данными исследования (Supplementary)
References
1. Joseph A, Simonaggio A, Stoclin A et al (2020) Immune‑related adverse events: a retrospectivelook into the future of oncology in the intensive care unit. Ann Intensive Care 10:143. https://doi.org/10.1186/ s13613‑020‑00761‑w
2. Ehooman F, Biard L, Lemiale V et al (2019) Long‑term health‑related quality of life of criticallyill patients with haematological malignancies: a prospective observational multicenter study. Ann Intensive Care 9:2. https://doi.org/10.1186/s13613‑018‑0478‑3
3. Chiou VL, Burotto M (2015) Pseudoprogression and immune‑related response in solid tumors. J Clin Oncol 33:3541–3543. https://doi.org/10. 1200/JCO.2015.61.6870
4. Cortegiani A, Madotto F, Gregoretti C et al (2018) Immunocompromised patients with acuterespiratory distress syndrome: secondary analysis of the LUNG SAFE database. Crit Care 22:157
5. Azoulay E, Pickkers P, Soares M et al (2017) Acute hypoxemic respiratory failure inimmunocompromised patients: the Efraim multinational prospective cohort study. Intensive Care Med 43:1808–1819. https://doi. org/10.1007/s00134‑017‑4947‑1
6. Vink EE, Azoulay E, Caplan A et al (2018) Time‑limited trial of intensive care treatment: an overview of current literature. Intensive Care Med 44:1369–1377.https://doi.org/10.1007/s00134‑018‑5339‑x
7. Shrime MG, Ferket BS, Scott DJ et al (2016) Time‑limited trials of intensive care for critically ill patients with cancer: how long is long enough? JAMA Oncol 2:76–83.https://doi.org/10.1001/jamaoncol.2015.3336
8. Borcoman E, Dupont A, Mariotte E et al (2020) One‑year survival in patients with solid tumoursdischarged alive from the intensive care unit after unplanned admission: a retrospective study. J Crit Care 57:36–41. https://doi.org/10.1016/j.jcrc.2020.01.027
9. Ferreyro BL, Scales DC, Wunsch H et al (2021) Critical illness in patients with hematologicmalignancy: a population‑based cohort study. Intensive Care Med 47:1104–1114. https://doi.org/10.1007/ s00134‑021‑06502‑2
10. Darmon M, Bourmaud A, Georges Q et al (2019) Changes in critically ill cancer patients’ short‑term outcome over the last decades: results of systematic review with meta‑analysis onindividual data. Intensive Care Med 45:977–987. https://doi.org/10.1007/s00134‑019‑05653‑7
11. Bernal T, Pardavila EV, Bonastre J et al (2013) Survival of hematological patients after discharge from the intensive care unit: a prospective obser‑ vational study. Crit Care.https://doi.org/10.1186/cc13172
12. Vigneron C, Charpentier J, Wislez M et al (2021) Short‑term and long‑term outcomes ofpatients with lung cancer and life‑threatening complications. Chest 160:1560–1564.https://doi.org/10.1016/j.chest.2021.04.056
13. Soares M, Salluh JIF, Ferreira CG et al (2005) Impact of two different comorbidity measures onthe 6‑month mortality of critically ill cancer patients. Intensive Care Med 31:408–415.https://doi.org/10.1007/ s00134‑005‑2554‑z
Источник фотоиллюстрации - www.freepik.com
[DETAIL_PICTURE] => Array
(
[ID] => 5217
[TIMESTAMP_X] => 11.11.2024 15:10:27
[MODULE_ID] => iblock
[HEIGHT] => 1078
[WIDTH] => 1616
[FILE_SIZE] => 191928
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn
[FILE_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[ORIGINAL_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 7017c35438bd3f7099a0eae004b3a6cc
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn/medical-banner-with-doctor-holding-tablet.jpg
[UNSAFE_SRC] => /upload/iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn/medical-banner-with-doctor-holding-tablet.jpg
[SAFE_SRC] => /upload/iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn/medical-banner-with-doctor-holding-tablet.jpg
[ALT] => Пять новых реалий в интенсивной терапии у онкологических больных
[TITLE] => Пять новых реалий в интенсивной терапии у онкологических больных
)
[~DETAIL_PICTURE] => 5217
[DATE_ACTIVE_FROM] => 30.05.2023
[~DATE_ACTIVE_FROM] => 30.05.2023
[ACTIVE_FROM_X] => 2023-05-30 00:00:00
[~ACTIVE_FROM_X] => 2023-05-30 00:00:00
[ACTIVE_FROM] => 30.05.2023
[~ACTIVE_FROM] => 30.05.2023
[SHOW_COUNTER] => 879
[~SHOW_COUNTER] => 879
[ID] => 8348
[~ID] => 8348
[IBLOCK_ID] => 2
[~IBLOCK_ID] => 2
[IBLOCK_SECTION_ID] =>
[~IBLOCK_SECTION_ID] =>
[DETAIL_TEXT_TYPE] => html
[~DETAIL_TEXT_TYPE] => html
[PREVIEW_TEXT] =>
[~PREVIEW_TEXT] =>
[PREVIEW_TEXT_TYPE] => text
[~PREVIEW_TEXT_TYPE] => text
[TIMESTAMP_X] => 11.11.2024 15:10:27
[~TIMESTAMP_X] => 11.11.2024 15:10:27
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/pyat-novykh-realiy-v-intensivnoy-terapii-u-onkologicheskikh-bolnykh-/
[~DETAIL_PAGE_URL] => /library/articles/pyat-novykh-realiy-v-intensivnoy-terapii-u-onkologicheskikh-bolnykh-/
[LANG_DIR] => /
[~LANG_DIR] => /
[CODE] => pyat-novykh-realiy-v-intensivnoy-terapii-u-onkologicheskikh-bolnykh-
[~CODE] => pyat-novykh-realiy-v-intensivnoy-terapii-u-onkologicheskikh-bolnykh-
[EXTERNAL_ID] => 8348
[~EXTERNAL_ID] => 8348
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[IBLOCK_CODE] => articles
[~IBLOCK_CODE] => articles
[IBLOCK_EXTERNAL_ID] => content-articles
[~IBLOCK_EXTERNAL_ID] => content-articles
[LID] => s1
[~LID] => s1
[NAV_RESULT] =>
[NAV_CACHED_DATA] =>
[DISPLAY_ACTIVE_FROM] => 30 мая 2023
[IPROPERTY_VALUES] => Array
(
)
[FIELDS] => Array
(
[NAME] => Пять новых реалий в интенсивной терапии у онкологических больных
[PREVIEW_PICTURE] => Array
(
[ID] => 5216
[TIMESTAMP_X] => 11.11.2024 15:10:27
[MODULE_ID] => iblock
[HEIGHT] => 3744
[WIDTH] => 5616
[FILE_SIZE] => 10408858
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4
[FILE_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[ORIGINAL_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 6fe7e2c05db92a6ccf46d467ca55498f
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4/medical-banner-with-doctor-holding-tablet.jpg
[UNSAFE_SRC] => /upload/iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4/medical-banner-with-doctor-holding-tablet.jpg
[SAFE_SRC] => /upload/iblock/119/afxlfcd5xbhf1j702vgegnpcpqjei8j4/medical-banner-with-doctor-holding-tablet.jpg
[ALT] => Пять новых реалий в интенсивной терапии у онкологических больных
[TITLE] => Пять новых реалий в интенсивной терапии у онкологических больных
)
[DETAIL_TEXT] =>
Guillaume Dumas, Stephen M. Pastores and Laveena Munshi Five new realities in criticalcare for patients with cancer
Пять новых реалий в интенсивной терапии у онкологических больных
Intensive Care Med 2023 doi.org/10.1007/s00134-023-06988-y
Опасные для жизни осложнения возникают у 5–10% больных раком, требующих госпитализации в отделение интенсивной терапии (ОИТ). Несколько факторов, таких как осложнения, связанные с самим заболеванием или индуцированные химиотерапией, делают эту популяцию уникальной. В эту эпоху быстрых изменений в онкологии понимание особенностей таких пациентов имеет решающее значение для определения клинического подхода. В этой статье мы выделяем пять новых реалий в лечении рака для реаниматологов.
Серьезное заболевание на запущенной стадии рака больше не означает конец жизни
Исторически госпитализация в ОИТ пациентов с распространенным раком (метастатическим солидным раком, гематологическими злокачественными новообразованиями высокой степени злокачественности) была связана с неблагоприятными исходами [1, 2]. Это было обусловлено (1) плохим функциональным статусом, (2) осторожным долгосрочным прогнозом или (3) критическим заболеванием из-за прогрессирования неизлечимого рака. Однако сейчас подход стал более сложным, поскольку был достигнут значительный прогресс в диагностике, классификации и лечении рака. Это позволило удвоить продолжительность жизни многих онкологических больных. Ранее неизлечимые виды злокачественных опухолей, такие как меланома или рефрактерная лимфома, теперь подвержены эффективной продлевающей жизнь терапии, приводящую к устойчивому контролю над раком. Реаниматологи должны учитывать эти новые реалии, чтобы адаптировать тактику в отношении данных пациентов.
При рассмотрении показаний для госпитализации в ОИТ есть несколько факторов, уникальных для пациентов с раком. (1) Прогноз в ОИТ в основном определяется диагнозом пациента, обусловившим развитие критического состояния и количеством пораженных органов, а не характеристиками рака. Если причина критического состояния быстро обратима (например, желудочно-кишечное кровотечение и катетер-ассоциированная инфекция кровотока) и отсутствуют обычные неблагоприятные прогностические признаки (например, выраженная старческая астения «хрупкость»), следует рассмотреть вопрос о госпитализации в ОИТ. Это решение должно учитывать ценности, предпочтения и ожидания пациента в отношении госпитализации, чтобы гарантировать, что мы оказываем целенаправленную помощь. (2) И наоборот, существуют специфические связанные с раком состояния, которые имеют очень плохой прогноз (например, легочно-лимфангитный карциноматоз e-Table-1; Supplemental appendix ).
Подобно состоянию «хрупкости», когда эти состояния присутствуют, независимо от причины критического состояния, выживаемость после лечения в ОИТ может быть мало вероятной, и следует рассмотреть паллиативный подход. (3) Наконец, при критических состояниях, связанных с более интенсивной поддержкой органов (например, инвазивная вентиляция легких) на поздних стадиях рака, крайне важно понимать прогноз рака у пациента, существуют ли поддерживающие жизнь методы лечения рака и влияние, которое критическое заболевание может оказать на конкретного пациента. Ограниченное по времени испытание в ОИТ (section-4) может быть рассмотрено в случаях, когда существует вероятность выживания в и возвращения к лечению рака после пребывания в ОИТ.
Новые методы лечения рака меняют результаты лечения пациентов, создавая новые болезни
Таргетная терапия произвела революцию в онкологии и все чаще используется в качестве терапии первой линии при некоторых видах рака. Интенсивисты должны знать о механизмах действия препаратов и токсичности (Fig. 1). В зависимости от класса лекарств нередки случаи тяжелой токсичности, включая пневмонит и нейротоксичность [1]. При некоторых видах терапии в рамках курса лечения можно ожидать развитие критического состояния, например тяжелого синдрома высвобождения цитокинов после инфузии химерных антигенных рецепторов-Т-клеток (CAR-T) (15–23%). Большинство этих проявлений токсичности можно смягчить введением кортикостероидов/иммунодепрессантов [1].

Важно отметить, что такие осложнения не обязательно являются противопоказанием к повторному назначению препарата или альтернативных классов. В отличие от традиционной химиотерапии, некоторые новые методы лечения могут быть предложены при органных дисфункциях, а некоторые показали быстрый регресс опухоли даже у пациентов в критическом состоянии. Более того, воздействуя на специфический путь, участвующий в патофизиологии рака, новые методы лечения продемонстрировали лучшую переносимость по сравнению с химиотерапией. Интенсивисты должны быть осведомлены об атипичных паттернах ответа, таких как псевдопрогрессия рака (определяемая как начальное увеличение объема опухоли в ответ на лечение), которая может привести к транзиторным локальным и (или) регионарным осложнениям и не должна быть ошибочно принята за неэффективность лечения [3].
Наконец, хотя количество новых методов лечения увеличивается, а траектории пациентов становятся более сложными (сочетание методов лечения одновременно/через некоторое время), вполне вероятно, что новые связанные с препаратами заболевания будут проявляться как критические состояния, и ОИТ могут использоваться для постановке диагноза или сыграть роль в разработке стратегии лечения.
Нам нужно по-новому взглянуть на острую дыхательную недостаточность
С 1990-х годов смертность от острой дыхательной недостаточности (ОДН) резко снизилась. Однако инвазивная вентиляция продолжает ассоциироваться с высокой смертностью (50–60%) при сохраняющемся разрыве у больных с раком при отсутствии онкологического заболевания [4, 5]. Существует несколько возможностей для дальнейших исследований (1) более глубокое понимание механизмов ОДН при раке необходимо для разработки терапевтических целей, (2) неопределенная ОДН остается высокой, и необходимы стратегии для улучшения диагностических возможностей (инфекционные по сравнению с неинфекционными), (3) идентификация субфенотипов необходима для продвижения поддерживающей терапии и заложения основы для таргетной терапии ОДН.
В рамках ОДН были идентифицированы субфенотипы (например, гипо/гипервоспалительные). Эти субфенотипы, вероятно, по-разному реагируют на лечение. В то время как сообщество по изучению ОДН продвигает эту исследовательскую программу вперед, важно, чтобы пациенты с ослабленным иммунитетом/раком были включены в этот анализ. Исторически сложилось так, что исследования ОДН грубо разделяли анализы на «иммунокомпрометированные» и «неиммунокомпрометированные»; однако идентификация субфенотипа, вероятно, является более сложной. Идентификация субфенотипа может быть важным следующим шагом для информирования терапевтических целей при ОДН.
Цели лечения и ограниченное по времени испытание
Эффективная коммуникация между ОИТ и онкологии необходима для обеспечения надлежащей эскалации и ограничения. Вероятно, существуют большие различия в клинической практике в зависимости от географических районов, убеждений врачей и подтипов рака. Учитывая отсутствие надежных показателей тяжести заболевания для прогнозирования исходов онкологических больных, решение о госпитализации в ОРИТ должно приниматься в индивидуальном порядке. Это решение должно учитывать ценности/предпочтения пациентов, прогноз критического состояния и ожидаемый долгосрочный исход рака (с правом на продолжение лечения рака и без него).
Решение о госпитализации в ОИТ часто бывает простым для пациента, получающего радикальное лечение. Однако в литературе отсутствует ясность в отношении политики госпитализации в эпоху новых противораковых препаратов для пациентов с распространенным раком. Новые методы лечения, такие как инфузия CAR-T-клеток, предполагают высокий риск развития критического состояния, и госпитализация в ОИТ может считаться частью проведения специфического лечения. С другой стороны, среди пациентов, получавших другие таргетные методы лечения, существуют неопределенности в отношении динамики состояния пациентов и того, как госпитализация в ОИТ может повлиять на их право на лечение в будущем. Учитывая это, в начале 2000-х годов было предложено «ICU time-limited trial» (TLT) [6] для интеграции таких неопределенностей в процессе принятия решений.
Эта политика госпитализации может быть определена как соглашение между всеми заинтересованными сторонами (т. е. пациентом, семьей, онкологом и реаниматологом) о типах расширенной органной поддержки в течение ограниченного периода времени для оценки вероятности выздоровления. Чтобы это было успешным, необходимо тесное сотрудничество между отделениями интенсивной терапии и онкологии, чтобы наилучшим образом информировать о полезности пребывания в ОИТ. В настоящее время оптимальное количество дней TLT плохо определено (в основном колеблется от 5 до 7 дней для солидных опухолей, но, возможно, до 14 дней для гематологических злокачественных новообразований) [7]. Количество отказавших органов может изменить продолжительность. Следует также добиваться внедрения высококачественной паллиативной помощи в ОИТ. Необходимы дальнейшие исследования, чтобы определить TLT для различных подтипов рака и показаний для госпитализации в ОИТ.
Пришло время выйти за рамки ОИТ
Смертность в ОИТ снизилась с 80–90% в исторических отчетах до 30–50% [5, 8]. Однако этот обнадеживающий прогресс обычно уравновешивается более разочаровывающими сообщениями о долгосрочной выживаемости (> 3 месяцев) в диапазоне от 25 до 55% с частым и стойким снижением качества жизни после выписки из ОИТ [1, 3, 9,10]. На сегодняшний день лишь несколько исследований посвящены долгосрочной выживаемости после выписки из ОИТ у онкологических больных [2, 8, 11–13]. Мы должны сместить наше внимание на определение влияния критического заболевания на лечение рака и долгосрочный прогноз рака после лечения в ОИТ в дополнение к исходам, ориентированным на пациента, таким как функциональные, когнитивные и симптоматические нарушения после пребывания в ОИТ.
Этот сдвиг согласуется с усилиями интенсивистов по характеристике бремени ПИТ-синдрома. Существует сложное взаимодействие между интенсивной терапией и онкологией, которое нельзя экстраполировать на пациентов, не страдающих раком. Дополнительные соображения включают право на поддерживающее жизнь или излечивающее лечение рака после выздоровления от критического заболевания. Крайне важно, чтобы мы понимали (до госпитализации в ОИТ): (1) доступные методы лечения рака, (2) применялись ли они, и (3) как выздоровление от критического заболевания влияет на возможность продолжения лечения от рака.
Нам необходимо оценить детерминанты возвращения к лечению после ОИТ (функциональное состояние, прогрессирование заболевания, персистирующая органная дисфункция и предпочтения пациента), чтобы обеспечить принятие решения врачом и пациентом. Это необходимо для обоснования будущих исследований потенциальных методов лечения для оптимизации этих факторов в будущем.
Ссылка на документ с дополнительными данными исследования (Supplementary)
References
1. Joseph A, Simonaggio A, Stoclin A et al (2020) Immune‑related adverse events: a retrospectivelook into the future of oncology in the intensive care unit. Ann Intensive Care 10:143. https://doi.org/10.1186/ s13613‑020‑00761‑w
2. Ehooman F, Biard L, Lemiale V et al (2019) Long‑term health‑related quality of life of criticallyill patients with haematological malignancies: a prospective observational multicenter study. Ann Intensive Care 9:2. https://doi.org/10.1186/s13613‑018‑0478‑3
3. Chiou VL, Burotto M (2015) Pseudoprogression and immune‑related response in solid tumors. J Clin Oncol 33:3541–3543. https://doi.org/10. 1200/JCO.2015.61.6870
4. Cortegiani A, Madotto F, Gregoretti C et al (2018) Immunocompromised patients with acuterespiratory distress syndrome: secondary analysis of the LUNG SAFE database. Crit Care 22:157
5. Azoulay E, Pickkers P, Soares M et al (2017) Acute hypoxemic respiratory failure inimmunocompromised patients: the Efraim multinational prospective cohort study. Intensive Care Med 43:1808–1819. https://doi. org/10.1007/s00134‑017‑4947‑1
6. Vink EE, Azoulay E, Caplan A et al (2018) Time‑limited trial of intensive care treatment: an overview of current literature. Intensive Care Med 44:1369–1377.https://doi.org/10.1007/s00134‑018‑5339‑x
7. Shrime MG, Ferket BS, Scott DJ et al (2016) Time‑limited trials of intensive care for critically ill patients with cancer: how long is long enough? JAMA Oncol 2:76–83.https://doi.org/10.1001/jamaoncol.2015.3336
8. Borcoman E, Dupont A, Mariotte E et al (2020) One‑year survival in patients with solid tumoursdischarged alive from the intensive care unit after unplanned admission: a retrospective study. J Crit Care 57:36–41. https://doi.org/10.1016/j.jcrc.2020.01.027
9. Ferreyro BL, Scales DC, Wunsch H et al (2021) Critical illness in patients with hematologicmalignancy: a population‑based cohort study. Intensive Care Med 47:1104–1114. https://doi.org/10.1007/ s00134‑021‑06502‑2
10. Darmon M, Bourmaud A, Georges Q et al (2019) Changes in critically ill cancer patients’ short‑term outcome over the last decades: results of systematic review with meta‑analysis onindividual data. Intensive Care Med 45:977–987. https://doi.org/10.1007/s00134‑019‑05653‑7
11. Bernal T, Pardavila EV, Bonastre J et al (2013) Survival of hematological patients after discharge from the intensive care unit: a prospective obser‑ vational study. Crit Care.https://doi.org/10.1186/cc13172
12. Vigneron C, Charpentier J, Wislez M et al (2021) Short‑term and long‑term outcomes ofpatients with lung cancer and life‑threatening complications. Chest 160:1560–1564.https://doi.org/10.1016/j.chest.2021.04.056
13. Soares M, Salluh JIF, Ferreira CG et al (2005) Impact of two different comorbidity measures onthe 6‑month mortality of critically ill cancer patients. Intensive Care Med 31:408–415.https://doi.org/10.1007/ s00134‑005‑2554‑z
Источник фотоиллюстрации - www.freepik.com
[DETAIL_PICTURE] => Array
(
[ID] => 5217
[TIMESTAMP_X] => 11.11.2024 15:10:27
[MODULE_ID] => iblock
[HEIGHT] => 1078
[WIDTH] => 1616
[FILE_SIZE] => 191928
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn
[FILE_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[ORIGINAL_NAME] => medical-banner-with-doctor-holding-tablet.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 7017c35438bd3f7099a0eae004b3a6cc
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn/medical-banner-with-doctor-holding-tablet.jpg
[UNSAFE_SRC] => /upload/iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn/medical-banner-with-doctor-holding-tablet.jpg
[SAFE_SRC] => /upload/iblock/745/r0n8ffefob0qn40ozccq8guoqwu7kpvn/medical-banner-with-doctor-holding-tablet.jpg
[ALT] => Пять новых реалий в интенсивной терапии у онкологических больных
[TITLE] => Пять новых реалий в интенсивной терапии у онкологических больных
)
[DATE_ACTIVE_FROM] => 30.05.2023
[ACTIVE_FROM] => 30.05.2023
[SHOW_COUNTER] => 879
)
[PROPERTIES] => Array
(
[KEYWORDS] => Array
(
[ID] => 1
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 100
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 102
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 828610
[VALUE] => интенсивная терапия, онкология
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => интенсивная терапия, онкология
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[DESCRIPTION] => Array
(
[ID] => 64
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Описание
[ACTIVE] => Y
[SORT] => 200
[CODE] => DESCRIPTION
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 828612
[VALUE] => Пять новых реалий в интенсивной терапии у онкологических больных
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Пять новых реалий в интенсивной терапии у онкологических больных
[~DESCRIPTION] =>
[~NAME] => Описание
[~DEFAULT_VALUE] =>
)
[BROWSER_TITLE] => Array
(
[ID] => 9
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Заголовок окна браузера
[ACTIVE] => Y
[SORT] => 300
[CODE] => BROWSER_TITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => content-articles-property-browser_title
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => Y
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 828611
[VALUE] => Пять новых реалий в интенсивной терапии у онкологических больных
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Пять новых реалий в интенсивной терапии у онкологических больных
[~DESCRIPTION] =>
[~NAME] => Заголовок окна браузера
[~DEFAULT_VALUE] =>
)
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 830452
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
)
[vote_count] => Array
(
[ID] => 100
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Количество проголосовавших
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_count
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество проголосовавших
[~DEFAULT_VALUE] =>
)
[vote_sum] => Array
(
[ID] => 101
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Сумма оценок
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_sum
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Сумма оценок
[~DEFAULT_VALUE] =>
)
[rating] => Array
(
[ID] => 102
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Рейтинг
[ACTIVE] => Y
[SORT] => 500
[CODE] => rating
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Рейтинг
[~DEFAULT_VALUE] =>
)
[FAVORITES] => Array
(
[ID] => 148
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Избранное
[ACTIVE] => Y
[SORT] => 500
[CODE] => FAVORITES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Избранное
[~DEFAULT_VALUE] =>
)
[LIKE] => Array
(
[ID] => 153
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Понравилось
[ACTIVE] => Y
[SORT] => 500
[CODE] => LIKE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Понравилось
[~DEFAULT_VALUE] =>
)
[SUBTITLE] => Array
(
[ID] => 93
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Подзаголовок
[ACTIVE] => Y
[SORT] => 501
[CODE] => SUBTITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Подзаголовок
[~DEFAULT_VALUE] =>
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828616
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
)
[QUOTE] => Array
(
[ID] => 95
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Цитата
[ACTIVE] => Y
[SORT] => 503
[CODE] => QUOTE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Цитата
[~DEFAULT_VALUE] =>
)
[SLIDER] => Array
(
[ID] => 98
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Слайдер
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер
[~DEFAULT_VALUE] =>
)
[SLIDER_DESC] => Array
(
[ID] => 99
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Слайдер описание
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER_DESC
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер описание
[~DEFAULT_VALUE] =>
)
[INFO_SOURCES] => Array
(
[ID] => 96
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Информация и источники
[ACTIVE] => Y
[SORT] => 504
[CODE] => INFO_SOURCES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Информация и источники
[~DEFAULT_VALUE] =>
)
[MATERIALS] => Array
(
[ID] => 97
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Материалы к статье
[ACTIVE] => Y
[SORT] => 505
[CODE] => MATERIALS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Материалы к статье
[~DEFAULT_VALUE] =>
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828614
[1] => 828615
[2] => 828680
[3] => 828682
)
[VALUE] => Array
(
[0] => statia
[1] => Infekcionnyj kontrol'
[2] => onkologiya
[3] => intensivnayaterapiya
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => statia
[1] => Infekcionnyj kontrol'
[2] => onkologiya
[3] => intensivnayaterapiya
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
)
[COMMENTS_COUNT] => Array
(
[ID] => 103
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Количество комментариев
[ACTIVE] => Y
[SORT] => 5010
[CODE] => COMMENTS_COUNT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество комментариев
[~DEFAULT_VALUE] =>
)
[FB2] => Array
(
[ID] => 173
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => FB2
[ACTIVE] => Y
[SORT] => 5020
[CODE] => FB2
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] => fb2
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => FB2
[~DEFAULT_VALUE] =>
)
[ADD_DATES] => Array
(
[ID] => 207
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Дата добавления материалов
[ACTIVE] => Y
[SORT] => 5030
[CODE] => ADD_DATES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => Date
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата добавления материалов
[~DEFAULT_VALUE] =>
)
[LENGHT] =>
[VIDEO_PREVIEW] =>
[VIDEO_FULL] =>
)
[DISPLAY_PROPERTIES] => Array
(
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 830452
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => да
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828616
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => [8] (info@sepsisforum.ru) Команда Сепсис Форума
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828614
[1] => 828615
[2] => 828680
[3] => 828682
)
[VALUE] => Array
(
[0] => statia
[1] => Infekcionnyj kontrol'
[2] => onkologiya
[3] => intensivnayaterapiya
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => statia
[1] => Infekcionnyj kontrol'
[2] => onkologiya
[3] => intensivnayaterapiya
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => Array
(
[0] => Статья
[1] => Инфекционный контроль
[2] => Онкология
[3] => Интенсивная терапия
)
)
)
[IBLOCK] => Array
(
[ID] => 2
[~ID] => 2
[TIMESTAMP_X] => 03.07.2025 10:45:52
[~TIMESTAMP_X] => 03.07.2025 10:45:52
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[LID] => s1
[~LID] => s1
[CODE] => articles
[~CODE] => articles
[API_CODE] =>
[~API_CODE] =>
[NAME] => Статьи
[~NAME] => Статьи
[ACTIVE] => Y
[~ACTIVE] => Y
[SORT] => 200
[~SORT] => 200
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[~DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[~SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[CANONICAL_PAGE_URL] =>
[~CANONICAL_PAGE_URL] =>
[PICTURE] =>
[~PICTURE] =>
[DESCRIPTION] => Статьи
[~DESCRIPTION] => Статьи
[DESCRIPTION_TYPE] => html
[~DESCRIPTION_TYPE] => html
[RSS_TTL] => 24
[~RSS_TTL] => 24
[RSS_ACTIVE] => Y
[~RSS_ACTIVE] => Y
[RSS_FILE_ACTIVE] => N
[~RSS_FILE_ACTIVE] => N
[RSS_FILE_LIMIT] =>
[~RSS_FILE_LIMIT] =>
[RSS_FILE_DAYS] =>
[~RSS_FILE_DAYS] =>
[RSS_YANDEX_ACTIVE] => N
[~RSS_YANDEX_ACTIVE] => N
[XML_ID] => content-articles
[~XML_ID] => content-articles
[TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[~TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[INDEX_ELEMENT] => Y
[~INDEX_ELEMENT] => Y
[INDEX_SECTION] => Y
[~INDEX_SECTION] => Y
[WORKFLOW] => N
[~WORKFLOW] => N
[BIZPROC] => N
[~BIZPROC] => N
[SECTION_CHOOSER] => L
[~SECTION_CHOOSER] => L
[LIST_MODE] =>
[~LIST_MODE] =>
[RIGHTS_MODE] => S
[~RIGHTS_MODE] => S
[SECTION_PROPERTY] => Y
[~SECTION_PROPERTY] => Y
[PROPERTY_INDEX] => I
[~PROPERTY_INDEX] => I
[VERSION] => 1
[~VERSION] => 1
[LAST_CONV_ELEMENT] => 0
[~LAST_CONV_ELEMENT] => 0
[SOCNET_GROUP_ID] =>
[~SOCNET_GROUP_ID] =>
[EDIT_FILE_BEFORE] =>
[~EDIT_FILE_BEFORE] =>
[EDIT_FILE_AFTER] =>
[~EDIT_FILE_AFTER] =>
[SECTIONS_NAME] => Разделы статей
[~SECTIONS_NAME] => Разделы статей
[SECTION_NAME] => Раздел статей
[~SECTION_NAME] => Раздел статей
[ELEMENTS_NAME] => Статьи
[~ELEMENTS_NAME] => Статьи
[ELEMENT_NAME] => Статья
[~ELEMENT_NAME] => Статья
[REST_ON] => N
[~REST_ON] => N
[FULLTEXT_INDEX] => N
[~FULLTEXT_INDEX] => N
[EXTERNAL_ID] => content-articles
[~EXTERNAL_ID] => content-articles
[LANG_DIR] => /
[~LANG_DIR] => /
[SERVER_NAME] => sepsisforum.ru
[~SERVER_NAME] => sepsisforum.ru
)
[SECTION] => Array
(
[PATH] => Array
(
)
)
[SECTION_URL] =>
[META_TAGS] => Array
(
[TITLE] => Пять новых реалий в интенсивной терапии у онкологических больных
[BROWSER_TITLE] => Пять новых реалий в интенсивной терапии у онкологических больных
[KEYWORDS] => интенсивная терапия, онкология
[DESCRIPTION] => Пять новых реалий в интенсивной терапии у онкологических больных
)
)
Пять новых реалий в интенсивной терапии у онкологических больных
Guillaume Dumas, Stephen M. Pastores and Laveena Munshi Five new realities in criticalcare for patients with cancer
Пять новых реалий в интенсивной терапии у онкологических больных
Intensive Care Med 2023 doi.org/10.1007/s00134-023-06988-y
Опасные для жизни осложнения возникают у 5–10% больных раком, требующих госпитализации в отделение интенсивной терапии (ОИТ). Несколько факторов, таких как осложнения, связанные с самим заболеванием или индуцированные химиотерапией, делают эту популяцию уникальной. В эту эпоху быстрых изменений в онкологии понимание особенностей таких пациентов имеет решающее значение для определения клинического подхода. В этой статье мы выделяем пять новых реалий в лечении рака для реаниматологов.
Серьезное заболевание на запущенной стадии рака больше не означает конец жизни
Исторически госпитализация в ОИТ пациентов с распространенным раком (метастатическим солидным раком, гематологическими злокачественными новообразованиями высокой степени злокачественности) была связана с неблагоприятными исходами [1, 2]. Это было обусловлено (1) плохим функциональным статусом, (2) осторожным долгосрочным прогнозом или (3) критическим заболеванием из-за прогрессирования неизлечимого рака. Однако сейчас подход стал более сложным, поскольку был достигнут значительный прогресс в диагностике, классификации и лечении рака. Это позволило удвоить продолжительность жизни многих онкологических больных. Ранее неизлечимые виды злокачественных опухолей, такие как меланома или рефрактерная лимфома, теперь подвержены эффективной продлевающей жизнь терапии, приводящую к устойчивому контролю над раком. Реаниматологи должны учитывать эти новые реалии, чтобы адаптировать тактику в отношении данных пациентов.
При рассмотрении показаний для госпитализации в ОИТ есть несколько факторов, уникальных для пациентов с раком. (1) Прогноз в ОИТ в основном определяется диагнозом пациента, обусловившим развитие критического состояния и количеством пораженных органов, а не характеристиками рака. Если причина критического состояния быстро обратима (например, желудочно-кишечное кровотечение и катетер-ассоциированная инфекция кровотока) и отсутствуют обычные неблагоприятные прогностические признаки (например, выраженная старческая астения «хрупкость»), следует рассмотреть вопрос о госпитализации в ОИТ. Это решение должно учитывать ценности, предпочтения и ожидания пациента в отношении госпитализации, чтобы гарантировать, что мы оказываем целенаправленную помощь. (2) И наоборот, существуют специфические связанные с раком состояния, которые имеют очень плохой прогноз (например, легочно-лимфангитный карциноматоз e-Table-1; Supplemental appendix ).
Подобно состоянию «хрупкости», когда эти состояния присутствуют, независимо от причины критического состояния, выживаемость после лечения в ОИТ может быть мало вероятной, и следует рассмотреть паллиативный подход. (3) Наконец, при критических состояниях, связанных с более интенсивной поддержкой органов (например, инвазивная вентиляция легких) на поздних стадиях рака, крайне важно понимать прогноз рака у пациента, существуют ли поддерживающие жизнь методы лечения рака и влияние, которое критическое заболевание может оказать на конкретного пациента. Ограниченное по времени испытание в ОИТ (section-4) может быть рассмотрено в случаях, когда существует вероятность выживания в и возвращения к лечению рака после пребывания в ОИТ.
Новые методы лечения рака меняют результаты лечения пациентов, создавая новые болезни
Таргетная терапия произвела революцию в онкологии и все чаще используется в качестве терапии первой линии при некоторых видах рака. Интенсивисты должны знать о механизмах действия препаратов и токсичности (Fig. 1). В зависимости от класса лекарств нередки случаи тяжелой токсичности, включая пневмонит и нейротоксичность [1]. При некоторых видах терапии в рамках курса лечения можно ожидать развитие критического состояния, например тяжелого синдрома высвобождения цитокинов после инфузии химерных антигенных рецепторов-Т-клеток (CAR-T) (15–23%). Большинство этих проявлений токсичности можно смягчить введением кортикостероидов/иммунодепрессантов [1].

Важно отметить, что такие осложнения не обязательно являются противопоказанием к повторному назначению препарата или альтернативных классов. В отличие от традиционной химиотерапии, некоторые новые методы лечения могут быть предложены при органных дисфункциях, а некоторые показали быстрый регресс опухоли даже у пациентов в критическом состоянии. Более того, воздействуя на специфический путь, участвующий в патофизиологии рака, новые методы лечения продемонстрировали лучшую переносимость по сравнению с химиотерапией. Интенсивисты должны быть осведомлены об атипичных паттернах ответа, таких как псевдопрогрессия рака (определяемая как начальное увеличение объема опухоли в ответ на лечение), которая может привести к транзиторным локальным и (или) регионарным осложнениям и не должна быть ошибочно принята за неэффективность лечения [3].
Наконец, хотя количество новых методов лечения увеличивается, а траектории пациентов становятся более сложными (сочетание методов лечения одновременно/через некоторое время), вполне вероятно, что новые связанные с препаратами заболевания будут проявляться как критические состояния, и ОИТ могут использоваться для постановке диагноза или сыграть роль в разработке стратегии лечения.
Нам нужно по-новому взглянуть на острую дыхательную недостаточность
С 1990-х годов смертность от острой дыхательной недостаточности (ОДН) резко снизилась. Однако инвазивная вентиляция продолжает ассоциироваться с высокой смертностью (50–60%) при сохраняющемся разрыве у больных с раком при отсутствии онкологического заболевания [4, 5]. Существует несколько возможностей для дальнейших исследований (1) более глубокое понимание механизмов ОДН при раке необходимо для разработки терапевтических целей, (2) неопределенная ОДН остается высокой, и необходимы стратегии для улучшения диагностических возможностей (инфекционные по сравнению с неинфекционными), (3) идентификация субфенотипов необходима для продвижения поддерживающей терапии и заложения основы для таргетной терапии ОДН.
В рамках ОДН были идентифицированы субфенотипы (например, гипо/гипервоспалительные). Эти субфенотипы, вероятно, по-разному реагируют на лечение. В то время как сообщество по изучению ОДН продвигает эту исследовательскую программу вперед, важно, чтобы пациенты с ослабленным иммунитетом/раком были включены в этот анализ. Исторически сложилось так, что исследования ОДН грубо разделяли анализы на «иммунокомпрометированные» и «неиммунокомпрометированные»; однако идентификация субфенотипа, вероятно, является более сложной. Идентификация субфенотипа может быть важным следующим шагом для информирования терапевтических целей при ОДН.
Цели лечения и ограниченное по времени испытание
Эффективная коммуникация между ОИТ и онкологии необходима для обеспечения надлежащей эскалации и ограничения. Вероятно, существуют большие различия в клинической практике в зависимости от географических районов, убеждений врачей и подтипов рака. Учитывая отсутствие надежных показателей тяжести заболевания для прогнозирования исходов онкологических больных, решение о госпитализации в ОРИТ должно приниматься в индивидуальном порядке. Это решение должно учитывать ценности/предпочтения пациентов, прогноз критического состояния и ожидаемый долгосрочный исход рака (с правом на продолжение лечения рака и без него).
Решение о госпитализации в ОИТ часто бывает простым для пациента, получающего радикальное лечение. Однако в литературе отсутствует ясность в отношении политики госпитализации в эпоху новых противораковых препаратов для пациентов с распространенным раком. Новые методы лечения, такие как инфузия CAR-T-клеток, предполагают высокий риск развития критического состояния, и госпитализация в ОИТ может считаться частью проведения специфического лечения. С другой стороны, среди пациентов, получавших другие таргетные методы лечения, существуют неопределенности в отношении динамики состояния пациентов и того, как госпитализация в ОИТ может повлиять на их право на лечение в будущем. Учитывая это, в начале 2000-х годов было предложено «ICU time-limited trial» (TLT) [6] для интеграции таких неопределенностей в процессе принятия решений.
Эта политика госпитализации может быть определена как соглашение между всеми заинтересованными сторонами (т. е. пациентом, семьей, онкологом и реаниматологом) о типах расширенной органной поддержки в течение ограниченного периода времени для оценки вероятности выздоровления. Чтобы это было успешным, необходимо тесное сотрудничество между отделениями интенсивной терапии и онкологии, чтобы наилучшим образом информировать о полезности пребывания в ОИТ. В настоящее время оптимальное количество дней TLT плохо определено (в основном колеблется от 5 до 7 дней для солидных опухолей, но, возможно, до 14 дней для гематологических злокачественных новообразований) [7]. Количество отказавших органов может изменить продолжительность. Следует также добиваться внедрения высококачественной паллиативной помощи в ОИТ. Необходимы дальнейшие исследования, чтобы определить TLT для различных подтипов рака и показаний для госпитализации в ОИТ.
Пришло время выйти за рамки ОИТ
Смертность в ОИТ снизилась с 80–90% в исторических отчетах до 30–50% [5, 8]. Однако этот обнадеживающий прогресс обычно уравновешивается более разочаровывающими сообщениями о долгосрочной выживаемости (> 3 месяцев) в диапазоне от 25 до 55% с частым и стойким снижением качества жизни после выписки из ОИТ [1, 3, 9,10]. На сегодняшний день лишь несколько исследований посвящены долгосрочной выживаемости после выписки из ОИТ у онкологических больных [2, 8, 11–13]. Мы должны сместить наше внимание на определение влияния критического заболевания на лечение рака и долгосрочный прогноз рака после лечения в ОИТ в дополнение к исходам, ориентированным на пациента, таким как функциональные, когнитивные и симптоматические нарушения после пребывания в ОИТ.
Этот сдвиг согласуется с усилиями интенсивистов по характеристике бремени ПИТ-синдрома. Существует сложное взаимодействие между интенсивной терапией и онкологией, которое нельзя экстраполировать на пациентов, не страдающих раком. Дополнительные соображения включают право на поддерживающее жизнь или излечивающее лечение рака после выздоровления от критического заболевания. Крайне важно, чтобы мы понимали (до госпитализации в ОИТ): (1) доступные методы лечения рака, (2) применялись ли они, и (3) как выздоровление от критического заболевания влияет на возможность продолжения лечения от рака.
Нам необходимо оценить детерминанты возвращения к лечению после ОИТ (функциональное состояние, прогрессирование заболевания, персистирующая органная дисфункция и предпочтения пациента), чтобы обеспечить принятие решения врачом и пациентом. Это необходимо для обоснования будущих исследований потенциальных методов лечения для оптимизации этих факторов в будущем.
Ссылка на документ с дополнительными данными исследования (Supplementary)
References
1. Joseph A, Simonaggio A, Stoclin A et al (2020) Immune‑related adverse events: a retrospectivelook into the future of oncology in the intensive care unit. Ann Intensive Care 10:143. https://doi.org/10.1186/ s13613‑020‑00761‑w
2. Ehooman F, Biard L, Lemiale V et al (2019) Long‑term health‑related quality of life of criticallyill patients with haematological malignancies: a prospective observational multicenter study. Ann Intensive Care 9:2. https://doi.org/10.1186/s13613‑018‑0478‑3
3. Chiou VL, Burotto M (2015) Pseudoprogression and immune‑related response in solid tumors. J Clin Oncol 33:3541–3543. https://doi.org/10. 1200/JCO.2015.61.6870
4. Cortegiani A, Madotto F, Gregoretti C et al (2018) Immunocompromised patients with acuterespiratory distress syndrome: secondary analysis of the LUNG SAFE database. Crit Care 22:157
5. Azoulay E, Pickkers P, Soares M et al (2017) Acute hypoxemic respiratory failure inimmunocompromised patients: the Efraim multinational prospective cohort study. Intensive Care Med 43:1808–1819. https://doi. org/10.1007/s00134‑017‑4947‑1
6. Vink EE, Azoulay E, Caplan A et al (2018) Time‑limited trial of intensive care treatment: an overview of current literature. Intensive Care Med 44:1369–1377.https://doi.org/10.1007/s00134‑018‑5339‑x
7. Shrime MG, Ferket BS, Scott DJ et al (2016) Time‑limited trials of intensive care for critically ill patients with cancer: how long is long enough? JAMA Oncol 2:76–83.https://doi.org/10.1001/jamaoncol.2015.3336
8. Borcoman E, Dupont A, Mariotte E et al (2020) One‑year survival in patients with solid tumoursdischarged alive from the intensive care unit after unplanned admission: a retrospective study. J Crit Care 57:36–41. https://doi.org/10.1016/j.jcrc.2020.01.027
9. Ferreyro BL, Scales DC, Wunsch H et al (2021) Critical illness in patients with hematologicmalignancy: a population‑based cohort study. Intensive Care Med 47:1104–1114. https://doi.org/10.1007/ s00134‑021‑06502‑2
10. Darmon M, Bourmaud A, Georges Q et al (2019) Changes in critically ill cancer patients’ short‑term outcome over the last decades: results of systematic review with meta‑analysis onindividual data. Intensive Care Med 45:977–987. https://doi.org/10.1007/s00134‑019‑05653‑7
11. Bernal T, Pardavila EV, Bonastre J et al (2013) Survival of hematological patients after discharge from the intensive care unit: a prospective obser‑ vational study. Crit Care.https://doi.org/10.1186/cc13172
12. Vigneron C, Charpentier J, Wislez M et al (2021) Short‑term and long‑term outcomes ofpatients with lung cancer and life‑threatening complications. Chest 160:1560–1564.https://doi.org/10.1016/j.chest.2021.04.056
13. Soares M, Salluh JIF, Ferreira CG et al (2005) Impact of two different comorbidity measures onthe 6‑month mortality of critically ill cancer patients. Intensive Care Med 31:408–415.https://doi.org/10.1007/ s00134‑005‑2554‑z
Источник фотоиллюстрации - www.freepik.com