Array
(
[NAME] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[~NAME] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[PREVIEW_PICTURE] => Array
(
[ID] => 5108
[TIMESTAMP_X] => 11.11.2024 15:24:54
[MODULE_ID] => iblock
[HEIGHT] => 720
[WIDTH] => 900
[FILE_SIZE] => 136557
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk
[FILE_NAME] => red-blood-cells.jpg
[ORIGINAL_NAME] => red-blood-cells.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 04509b0cec63a27995ce0eca5eaa2ef0
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk/red-blood-cells.jpg
[UNSAFE_SRC] => /upload/iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk/red-blood-cells.jpg
[SAFE_SRC] => /upload/iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk/red-blood-cells.jpg
[ALT] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[TITLE] => Призыв к персонализации коррекции гемодинамики при септическом шоке
)
[~PREVIEW_PICTURE] => 5108
[DETAIL_TEXT] => DeBacker D. et al. A plea for personalization of the hemodynamic management of septic shock Призыв кперсонализации коррекции гемодинамики при септическом шоке Critical Care (2022)26:372doi.org/10.1186/s13054-022-04255-y
Абстракт
Несмотря на то, что руководства содержат отличные рекомендации специалистов по ведению пациентов с септическим шоком, они оставляют место для персонализации в зависимости от состояния пациентов. Мониторинг гемодинамики зависит от фазы развития: спасение, оптимизация, стабилизация и деэскалация. На начальном этапе во время спасательной фазы мониторинг для определения этиологии и тяжести шока должен включать измерение артериального давления и лактата вместе с клиническим обследованием, особенно определением пятнистости кожи и времени наполнения капилляров. Низкое диастолическое давление может мотивировать к использованию вазопрессоров.
На этой стадии эхокардиография может быть полезна для выявления выраженной сердечной дисфункции. На этапе оптимизации следует проводить эхокардиографический мониторинг, с оценкой тканевой перфузии путем измерения центральной или смешанной венозной сатурации кислородом, измерения лактата и вено-артериального градиента углекислого газа. Транспульмональная термомодуляция и катетеризация легочной артерии должны рассматриваться у наиболее тяжелых пациентов. Инфузионная терапия также зависит от фаз шока. В то время как предусмотрена либеральная стратегия инфузионной терапии во время фазы реанимации, следует оценить реакцию на инфузионную терапию во время фазы оптимизации. Во время стабилизации инфузия жидкости должна быть сведена к минимуму. На этапе деэскалации может быть обеспечено безопасное удаление жидкости за счет сохранения тканевой перфузии. В качестве вазопрессорной терапии первой линии рекомендуется норэпинефрин, в то время как у некоторых пациентов предпочтение отдается вазопрессину.
Остаются важные вопросы относительно оптимального выбора вазопрессоров, комбинированной терапии и наиболее эффективной и безопасной эскалации. Ренин сыворотки и соотношение ангиотензина I/II могут выявить пациентов, которые получают наибольшую пользу от ангиотензина II.Оптимальная терапевтическая стратегия при шоке, требующем высоких доз вазопрессоров, ограничена. Во всех случаях вазопрессорная терапия должна быть индивидуализирована и основана на клинической оценке и измерениях кровотока, чтобы избежать чрезмерной вазоконстрикции. Инотропы следует рассматривать у пациентов со сниженной сердечной сократимостью, связанной с нарушением тканевой перфузии. Исходя из фармакологических свойств, мы предлагаем в качестве первого теста ограниченную дозу добутамина, добавить эноксимон или милринон во вторую линию и заменить или добавить левосимендан, если нет эффекта. Что касается дополнительной терапии, то хотя гидрокортизон в настоящее время рекомендуется пациентам, получающим высокие дозы вазопрессоров, в будущем пациентов, отвечающих на кортикостероиды, можно будет идентифицировать с помощью анализа выбранных цитокинов или специфических транскриптомныхэ ндотипов.
Несмотря на то, что для лечения шока применяются некоторые общие правила, следует учитывать индивидуальный подход для мониторинга и поддержки гемодинамики.
Ключевые слова: артериальное давление, сердечный выброс, тканевая перфузия, жидкости, вазопрессорные средства, инотропные средства.
Шок — опасное для жизни состояние, характеризующееся неадекватной доставкой кислорода к тканям [1]. Септический шок является одной из наиболее частых причин шока в отделении интенсивной терапии(ОИТ) [2]. Рекомендации Surviving Sepsis Campaign (SSC) представляют собой отличное руководство по ведению пациентов с сепсисом [3], но по ряду причин здесь есть место для персонализации [4]. Во-первых, хотя эти рекомендации подтверждаются доказательствами, они основаны главным образом на рандомизированных контролируемых исследованиях (РКИ), в которых изучалась реакция больших групп пациентов на вмешательство. Эти исследования, как правило, негативны, т. е. не выявляют различий в смертности. Важно осознавать, что индивидуальные особенности пациента могут влиять на реакцию или переносимость данного вмешательства. Во-вторых, многие области реанимации до сих пор являются предметом дискуссий и остаются пробелы в исследованиях [5].
Следовательно, руководящие принципы часто не содержат сильных и точных рекомендаций в конкретных областях. В-третьих, существуют разные этапы лечения шока [2], каждый из которых требует своего подхода. Таким образом, может быть оправдано индивидуализация терапевтических подходов в зависимости от состояния пациента. В этом экспертном заключении мы обсуждаем различные варианты персонализации гемодинамического мониторинга и ведения пациентов на разных стадиях септического шока. Общий принцип персонализированного лечения шока заключается в измерении, интерпретации, применении терапии, оценке ее эффектов и реагировании, в отличие от применения стандартных мер.
Персонализация мониторинга
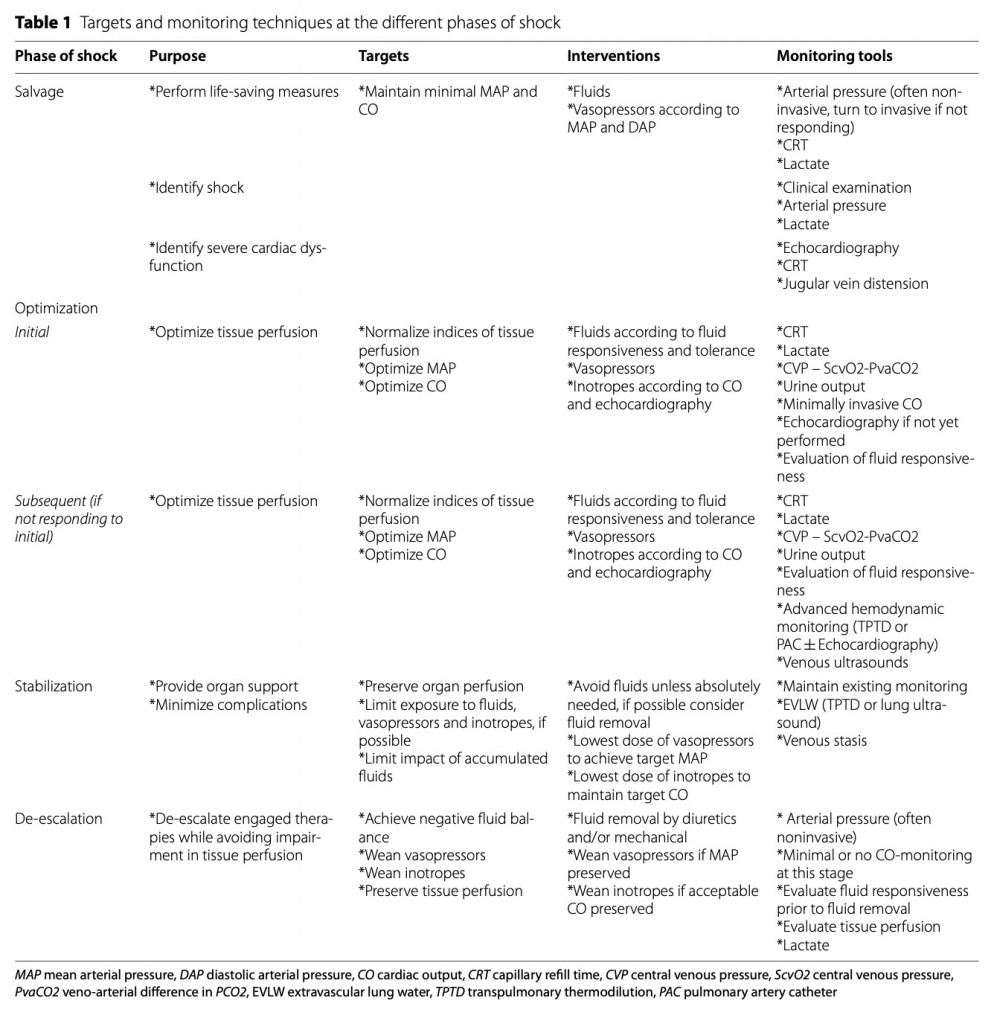
Персонализация гемодинамического мониторинга подразумевает рассмотрение различных фаз SOSD(спасение, оптимизация, стабилизация и деэскалация). На каждом этапе доступные методы и цели различаются (Fig.1and Table1).
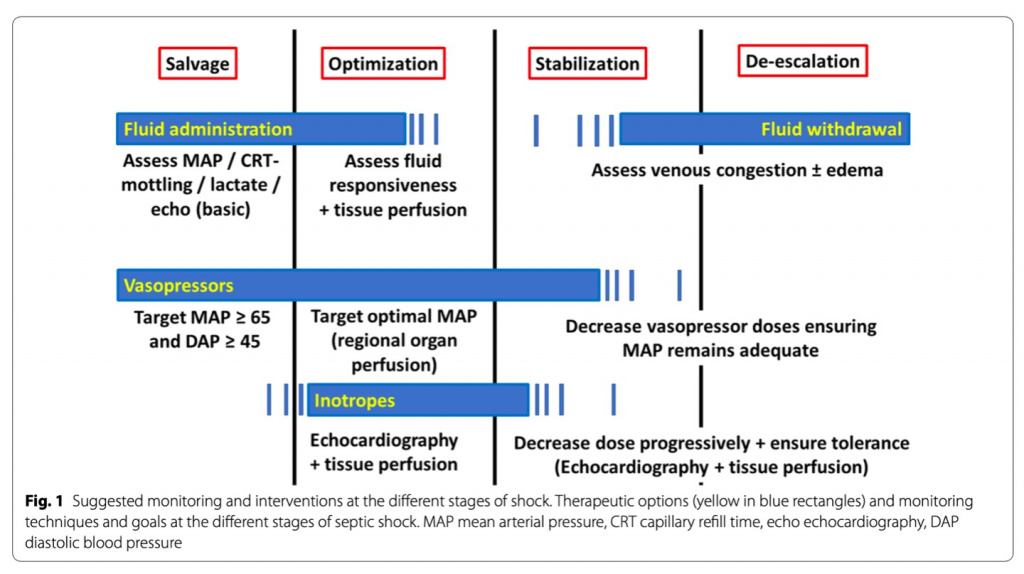
Время распознавания шока: фаза спасения
Во время распознавания и идентификации шока первоначальное лечение направлено на обеспечение уровня перфузии тканей, совместимого с жизнью. В этой фазе гемодинамический мониторинг часто является очень простым, а терапевтические возможности ограничены жидкостями и вазопрессорами.
Какую информацию можно получить из базового гемодинамического мониторинга при проведении реанимационных мероприятий?
Клиническая оценка имеет решающее значение для выявления гипоперфузии тканей. Измерение артериального давления, пятнистость кожи и время наполнения капилляров (CRT) информируют о ходе реанимации. Изменения показателей CRT и пятнистости могут использоваться для базового мониторинга, поскольку они коррелируют с исходом [6, 7] и быстро реагируют на проводимую терапию. Однако они плохо коррелируют с сердечным выбросом (СВ), не позволяют идентифицировать источник тканевой гипоперфузии и определить необходимые мероприятия [8].
Если есть кардиологический анамнез или если пациент не реагирует на жидкости, для уточнения оценки гемодинамики полезно быстрое эхокардиографическое исследование [1]. Эхокардиография у постели больного является единственным методом, который позволяет быстро оценить СВ наряду с идентификацией причины низкого СВ. В недавнем РКИ использование эхокардиографии группой быстрого реагирования было связано с улучшением выживаемости [9].
Во время фазы спасения инотропы могут быть показаны, когда соответствующий кардиогенный компонент (связанный с септической кардиомиопатией или сопутствующими заболеваниями пациента) способствует шоковому процессу [1, 10]. Это можно определить только с помощью эхокардиографии, и инотропы следует рассматривать, когда СВ низкий из-за серьезного нарушения сократительной способности сердца. При тяжелом кардиогенном шоке эхокардиография может также быстро выявить пациентов, не отвечающих на первоначальную терапию, и для которых может быть рассмотрена механическая поддержка сердца [11].
Базовый клинический мониторинг играет роль в выявлении пациентов, которые могут реагировать на жидкости, и оценке их реакции [12]. В частности, время наполнения капилляров можно использовать для оценки перфузионной реакции тканей и определения необходимости дальнейшего введения жидкостей [13].
Динамические тесты, такие как реакция пульсового давления или время наполнения капилляров на пассивное поднятие ноги, могут использоваться для прогнозирования реакции на жидкость [14, 15]. Однако эти тесты трудно проводить на этапе спасения, когда одновременно применяется множество вмешательств. Прогнозирование реакции на инфузию и оценка эффектов инфузии должны быть предприняты как можно скорее, особенно у пациентов с плохой функцией сердца.
Измерение уровня лактата в крови полезно для выявления нарушений тканевой перфузии. Кроме того, когда установлен центральный венозный катетер, центральная венозная сатурация O2 (ScvO2) и градиент парциального давления углекислого газа (pCO2) между центральной венозной и артериальной кровью (Pv-aCO2) могут быть полезны для оценки эффективности проводимых мероприятий.
Как определить пациентов, у которых немедленная вазопрессорная терапия приносит пользу, не дожидаясь результатов инфузионной терапии?
В то время как некоторые пациенты могут реагировать только на инфузионную терапию, другим требуется вазопрессорная поддержка. Руководящие принципы SSC рекомендуют поддерживать среднее артериальное давление (САД) ≥ 65 мм рт. ст., но не указывают сроки или не дают указаний по приоритетности жидкости по сравнению с вазопрессорами. Некоторым пациентам с тяжелой гипотензией может потребоваться раннее начало введения вазопрессоров, т. е. не дожидаясь эффекта жидкости, для ускорения восстановления артериального давления. Действительно, отсрочка коррекции гипотензии связана с плохим исходом [16]. Более того, норадреналин может способствовать увеличению преднагрузки на сердце [17], что может снизить потребность в жидкости. В обсервационном исследовании с использованием сопоставления склонности раннее начало норадреналина было связано с менее положительным балансом жидкости и более низкой 28-дневной смертностью [18].
Решение о раннем назначении вазопрессоров наряду с инфузионной терапией кажется логичным в случаях выраженной гипотензии, хотя точного порога САД дать нельзя. Диастолическое давление (ДАД) также может влиять на принятие решения.. При сепсисе низкое ДАД часто отражает выраженную вазодилатацию и связано с повышенной смертностью [19]. Поэтому представляется логичным начинать назначение вазопрессоров при очень низком ДАД, например, < 45 мм рт.ст. У пациентов с тахикардией высокие значения индекса диастолического шока (ИДШ): соотношение между ДАД и ЧСС, связаны с более высоким риском смерти у больных с септическим шоком [19]. Следует ли использовать ИДШ> 2 для начала введения вазопрессоров, остается неизвестным.
Фаза оптимизации: инструменты и цели
На этом этапе целью реанимационных мероприятий является оптимизация тканевой перфузии за счет оптимизации перфузионного давления и СВ. В идеале это также должно включать оптимизацию регионарного распределения кровотока и микроциркуляторной перфузии. Хотя изменения в распределении регионарного кровотока [20] и микрососудистой перфузии [21] часты при шоке и могут быть отделены от системного кровообращения, в клинической практике их нелегко контролировать.
Наиболее частые показатели тканевой гипоперфузии, используемые у постели больного, включают артериальное давление, диурез, кожную перфузию, время наполнения капилляров, ScvO2, Pv-aCO2 и концентрацию лактата. Важно отметить, что даже если на исходном уровне существует некоторая корреляция между различными индексами, некоторые переменные нормализуются быстрее, чем другие [22]. ScvO2, по-видимому, нормализуется быстрее всего, за ним следуют CRT и Pv-aCO2, которые обычно нормализуются в течение 6–8 часов, в то время как лактат и подъязычная микроциркуляция могут нормализоваться более, чем через 24 часа [13]. Кажется логичным объединить несколько переменных и прекратить реанимационные мероприятия, когда большинство из них нормализуются, не прибегая к нормализации переменных, таких как концентрации лактата [23]. При обнаружении тканевой гипоперфузии следует оценить реакцию на инфузионную терапию, а в некоторых случаях следует рассмотреть возможность применения передовых гемодинамических методов для оценки сердечно-сосудистой функции.
Время наполнения капилляров (CRT)
CRT является маркером гипоперфузии кожи, динамически реагирующей на вазоактивные вещества. В какой степени время наполнения капилляров отражает центральную перфузию остается неизвестной. В то время как одно исследование пришло к выводу, что CRTотражает центральное кровообращение [24], другие исследования предполагают некоторую диссоциацию [22, 25]. Измерения CRT показывают значительную изменчивость между наблюдателями [26], но это можно свести к минимуму с помощью стандартизации метода [13]. По сравнению с реанимацией, нацеленной на лактат при раннем септическом шоке реанимация под контролем CRT, как правило, лучше [13, 27]. Среди факторов, способствующих этим различиям, более частые оценки кровообращения в группе CRT. Достижение значения CRT< 3 с является ценным ориентиром эффективных мероприятий, в то время как медленное снижение уровня лактата само по себе может привести к дополнительному введению жидкости, даже если перфузия тканей могла нормализоваться на момент оценки.
Среднее артериальное давление
Определение целевого системного артериального давления, необходимого для достижения адекватной тканевой перфузии, остается сложной задачей. В принципе, органный кровоток зависит от перфузионного давления (т. е. разницы между давлением притока и оттока) и сопротивления. Однако сохранения системного артериального давления недостаточно для обеспечения адекватности микроциркуляторного русла. Важно отметить, что перфузионное давление различается в зависимости от сосудистого русла (Table2), и эти уровни также могут повреждаться при сепсисе.

Большинство органов обладают эндогенной способностью сохранять микроциркуляцию в определенном диапазоне перфузионных давлений. Например, сердце и мозг могут поддерживать постоянный кровоток, несмотря на большие изменения перфузионного давления. В случае, если давление падает ниже органоспецифической зоны ауторегуляции, органный кровоток становится зависимым от давления притока, поэтому основное внимание уделяется устранению гипотонии в фазу спасения.
Неоднородность пациентов, различная органоспецифическая регуляция микроциркуляции, вариабельная плотность рецепторов и влияние фармакологических взаимодействий затрудняют единый подход к лечению септического шока [28]. Руководство SSC рекомендует начальное целевое среднее артериальное давление 65 мм рт. ст. [3], но не содержит рекомендаций для более поздних стадий. Данные наблюдений показывают, что органная дисфункция иногда может начаться уже при падении СрАД ниже 75–80 мм рт. ст. [16], но для достижения более высоких целевых значений СрАД часто требуются более высокие дозы вазопрессоров, которые могут быть связаны с большим количеством побочных эффектов.
Исследования, рандомизирующие пациентов с сепсисом в группы с целевым значением СрАД ~ 65 мм рт. ст. или даже меньше по сравнению с от~ 75 и до ~ 85 мм рт. ст., не показали различий в смертности [29, 30]. Положительное влияние более высокого среднего артериального давления на функцию почек у ранее страдающих артериальной гипертензией пациентов можно наблюдать [29], но оно не является систематическим [30]. Различия в влиянии более высоких целевых значений СрАД на функцию почек можно частично объяснить высокой вариабельностью реакции почечного кровотока на увеличение СрАД [31].
Несостоятельность подхода «один размер подходит всем» была также продемонстрирована у пациентов с артериальной гипотензией. Анализ 3542 пациентов в критическом состоянии с шоком показал, что пациенты с естественно низким АД (систолическое АД < 100 мм рт. ст.) лечились дольше и с более высокими дозами норадреналина и имели более длительное пребывание в ОИТ и более высокую смертность [32]. Соответственно, в то время как начальное целевое среднее артериальное давление 65 мм рт. ст. представляется разумным подходом для многих пациентов, идеальное среднее артериальное давление должно быть индивидуальным. Подтверждение эффективности выбранного индивидуального целевого СрАД заключается в оценке изменений показателей перфузии, таких как диурез, уровень сознания и кожная перфузия. Если наблюдаются положительные эффекты, можно использовать это новое целевое значение СрАД, если оно неэффективно или непереносимо, то следует установить начальное значение СрАД.
Центральное венозное давление (ЦВД)
ЦВД представляет собой сложную переменную, отражающую преднагрузку и функцию правого желудочка [33]. Несмотря на то, что его способность точно предсказывать реакцию на инфузионную терапию сомнительна, оно по-прежнему предоставляет важную информацию о волемическом статусе и резерве правого желудочка и должно измеряться при шоке [34]. ЦВД может быть важным ранним индикатором недостаточности правого желудочка. Устойчивое повышение ЦВД > 12 мм рт. ст. связано с нарушением функции почек и кишечника, даже когда перфузионное давление в органах остается постоянным, что свидетельствует о том, что венозный застой играет роль в органной дисфункции. Для ЦВД не должно быть целевого значения, так как идеальное ЦВД — это самое низкое ЦВД, связанное с гемодинамической стабильностью.
Сердечный выброс (СВ)
CВ является ключевым фактором перфузии тканей. Однако не существует фиксированного значения оптимального СВ при шоке, и СВ следует оптимизировать в соответствии с индексами тканевой перфузии, перечисленными ниже, и функцией органов. Важно отметить, что микрососудистые изменения могут сохраняться даже после коррекции низкого СВ, что ухудшает тканевую перфузию [21, 35]. При гиперкинетическом шоке стойкие нарушения перфузии связаны с изменениями регионарной перфузии и/или изменениями микроваскулярной перфузии. Эти микрососудистые изменения могут быть нечувствительны к увеличению СВ, поэтому следует использовать другие стратегии для улучшения микроциркуляции. Соответственно, CВ следует рассматривать как средство улучшения тканевой перфузии, а не как мишень.
Смешанное венозное (SvO2) и центральное венозное (ScvO2) насыщение кислородом
Хотя ScvO2 или SvO2 даже не упоминаются в новых рекомендациях SSC [3], они являются очень важными физиологическими переменными, которые необходимо понимать и измерять. Они отражают баланс между фактическим потреблением кислорода и доставкой кислорода тканям. Соответственно, низкий уровень ScvO2указывает на нарушение или неадекватную доставку O2, что объясняется неадекватным СО, если гемоглобин и сатурация артериальной крови O2 находятся в пределах нормы. Ожидается, что при сепсисе SvO2 и ScvO2 будут нормальными или повышенными даже при нарушении тканевой перфузии [21]. В то время как определение конкретных значений SvO2 или ScvO2 у всех пациентов было затруднено [36], обнаружение низкого SvO2 или ScvO2 может выявить пациентов, которым должны помочь дальнейшие реанимационные мероприятия. Это может заключаться в увеличении СО с помощью инфузионной терапии или инотропного агента, а иногда и гемоглобина путем переливания крови у пациентов с анемией. У пациентов с высоким ScvO2 следует тщательно проверять другие показатели нарушения перфузии.
Разница венозной и артериальной концентрации углекислого газа (Pv-aCO2)
Pv-aCO2 зависит от общего производства углекислого газа (CO2), CO и перфузии микрососудов, а также от сложной взаимосвязи между парциальным давлением CO2 и содержанием CO2 в крови. Согласно модифицированному уравнению Фика, Pv-aCO2 находится в обратной зависимости от CO (криволинейная зависимость). При стабильных условиях как потребления кислорода (VO2), так и продукции CO2 (VCO2) Pv-aCO2 прогрессивно увеличивается в ответ на снижение CO из-за застояCO2 в микрососудах. Прогрессирующее увеличение Pv-aCO2 отражает снижение микроциркуляторной перфузии на ранних стадиях септического шока [37]. Таким образом, высокое значение Pv-aCO2 может идентифицировать пациентов с сепсисом, которые неадекватно реанимированы [38]. ЗначениеPv-aCO2 [39] и изменение Pv-aCO2 в ответ на терапию связаны с исходом [40]. Измерение Pv-aCO2 может быть особенно полезным у пациентов с нормальными значениями лактата или ScvO2 для выявления пациентов с риском неблагоприятного исхода, несмотря на очевидную адекватную реанимацию [40–42]. Тем не менее, трудно рекомендовать конкретное целевое значение Pv-aCO2 на основе наблюдательных испытаний. Отношение Pv-aCO2 к артериовенозной разнице содержания кислорода является оценкой дыхательного коэффициента и, как таковая, может быть прямым показателем анаэробного метаболизма с более быстрыми изменениями, чем у лактата [42, 43].
Концентрация лактата в крови
Уровни лактата имеют сильное прогностическое значение и поэтому могут использоваться для скрининга. Оценка серийных уровней лактата полезна, так как они обычно снижаются у пациентов, которым становится лучше, и часто остаются повышенными или даже увеличиваются, когда септический шок плохо контролируется. Стратегии реанимации, направленные на снижение уровня лактата, были связаны со снижением госпитальной летальности [44]. Таким образом, кажется логичным направить реанимационную стратегию на снижение уровня лактата [3].Однако повышенный уровень лактата также может быть вызван другими причинами, помимо тканевой гипоксии (например, воспалением, снижением клиренса лактата и т. д.). У больных с шоком гиперлактатемия в первые несколько часов после поступления преимущественно гипоксического происхождения, тогда как не гипоксические причины преобладают на более поздних стадиях [45]. Снижение уровня лактата также требует времени, поэтому изолированная гиперлактатемия может сохраняться после нормализации других показателей тканевой гипоперфузии [22]. Следовательно, погоня за нормализацией лактата может быть нецелесообразной [23]. У пациентов с нормализованным временем наполнения капилляров реанимация под контролем лактата была связана с повышенной смертностью [46]. Соответственно, мониторинг уровня лактата в крови играет роль в оценке эффективности реанимационных процедур в сочетании с другими показателями тканевой гипоперфузии.
Эхокардиография
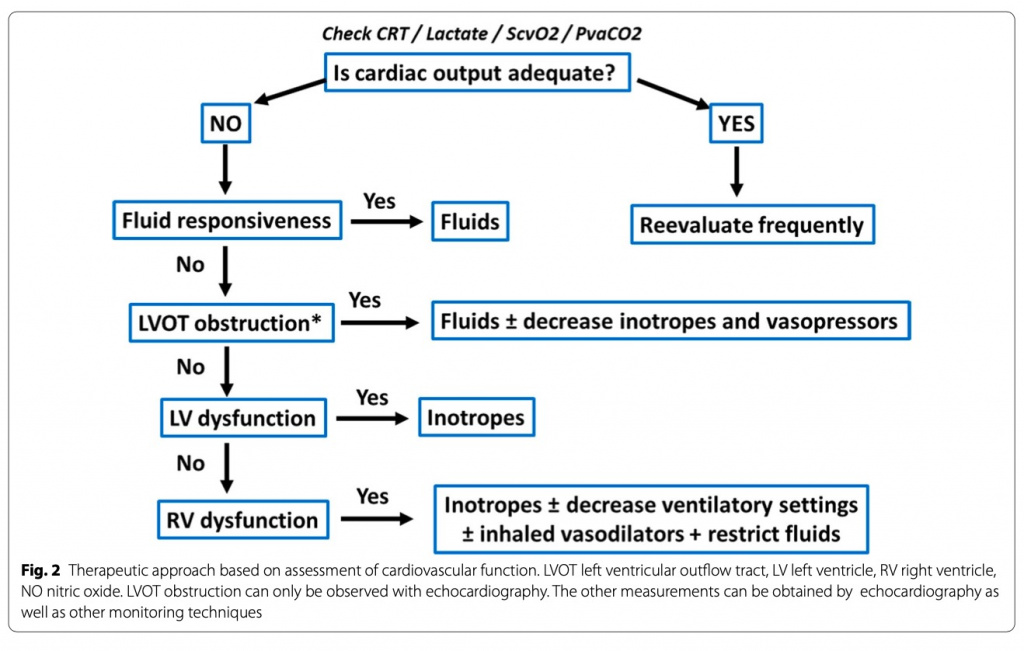
Следует рассмотреть вопрос о проведении эхокардиографии, поскольку первоначальные реанимационные процедуры могли повлиять на функцию левого и правого желудочков: дисфункция левого желудочка может возникнуть из-за увеличения постнагрузки после коррекции тяжелой гипотензии; динамическая обструкция могла быть вызвана инотропными или вазопрессорными агентами; и, наконец, правожелудочковая дисфункция может быть связана с искусственной вентиляцией легких. Кроме того, сепсис-индуцированная кардиопатия может нарушать функцию левого и правого желудочков. Эхокардиографию можно использовать для оценки объемного статуса [34].При сепсисе различные фенотипы можно идентифицировать по комбинации эхокардиографических показателей [47]. Это позволяет точно настроить терапевтические вмешательства (Fig. 2). Важно измерять ударный объем (УО), поскольку инотропные препараты показаны только в том случае, если нарушение сердечной функции связано с низким или неадекватным УО и нарушением тканевой перфузии. Кроме того, особое внимание должно быть сосредоточено на правом желудочке, так как дисфункция правого желудочка может потребовать специального лечения.
Расширенный мониторинг
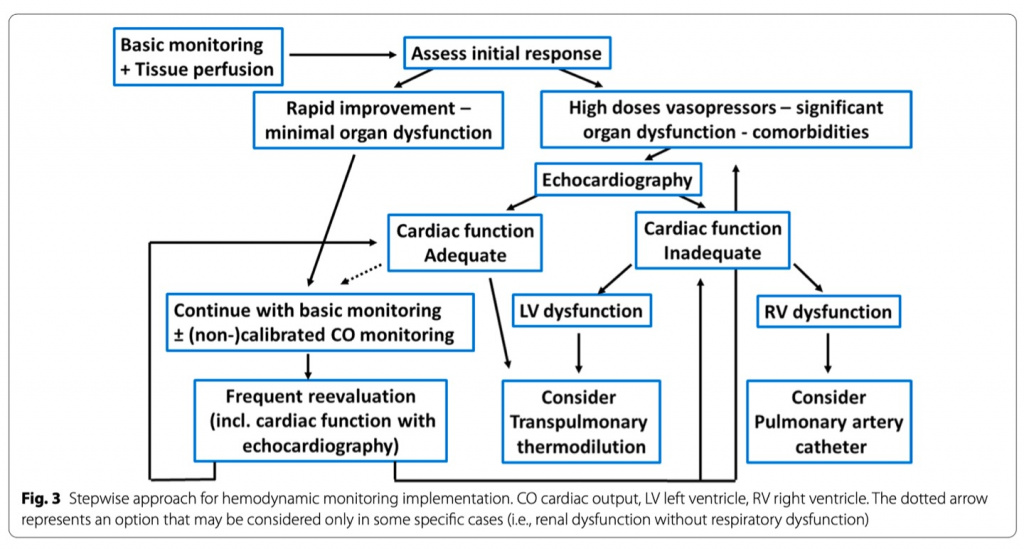
Для надежного измерения СВ можно использовать различные инструменты, но выбор метода должен основываться на представляющих интерес переменных, в зависимости от состояния пациента (Fig. 3). У пациентов без сопутствующих заболеваний и с минимальной органной дисфункцией можно использовать некалиброванные устройства с внутренней калибровкой доя для мониторинга CВ [48], но более сложные пациенты (с сопутствующими заболеваниями, сопутствующей органной дисфункцией) выиграют от использования транспульмональной термодилюции [49] или, в конечном итоге, катетеризации легочную артерии в сочетании с эхокардиографией по мере необходимости [50].
Транспульмональная термодилюция (TPTD) сочетает в себе калиброванное измерение CВ, пошаговое и точное определение УО, что полезно для прогнозирования реакции на инфузию, показателей статической объемной преднагрузки, индексов сердечной функции, внесосудистой жидкости в легких (EVLW) и сосудистой проницаемости. Эта всесторонняя гемодинамическая оценка особенно полезна при управлении инфузионной терапией, поскольку она обеспечивает динамическую оценку реакции на инфузионную терапию в сочетании с оценкой рисков, связанных с объемом введенной жидкости [34].
Благодаря комбинированным измерениям СВ, легочного давления и SvO2 использование катетера легочной артерии (КЛА), обеспечивает оценку адекватности СВ и его детерминант. Несмотря на то, что КЛА не позволяет предсказать реакцию на введение жидкости, он отлично подходит для оценки эффективности и толерантности к инфузионной терапии во время введения жидкости. Одновременное измерение ЦВД и давления в легочной артерии делает КЛА идеальным для мониторинга пациентов с дисфункцией правых отделов сердца. В конце концов, выбор метода мониторинга должен основываться на состоянии пациента, местном опыте и доступности, а также ожидаемом ответе на терапию. Предлагается поэтапный подход к пациенту с септическим шоком (Fig.3).
Стабилизация и деэскалация: подходы и показатели толерантности
Во время стабилизации и деэскалации подходы и цели должны быть адаптированы. На этих этапах цель гемодинамической поддержки меняется с оптимизации перфузии тканей на предотвращение осложнений при обеспечении поддержки органов. Он включает эвакуацию скопившейся жидкости и отказ от вазоактивной поддержки при сохранении тканевой перфузии.
В фазе стабилизации распространены сердечная дисфункция и объемная перегрузка и часто продолжают использовать уже внедренные методы поддержки гемодинамики. УЗИ легких и оценка печеночного, почечного и портального венозного кровотока с помощью ультразвука могут выявить признаки венозного застоя, которые могут указывать на необходимость удаления жидкости и/или введения инотропов [34]. Комбинация визуализации легких/вен с эхокардиографией особенно полезна для дифференциальной диагностики между перегрузкой объемом и сердечной дисфункцией.
Частым осложнением является развитие дисфункции правого желудочка, которая может развиться у 20% пациентов с острым респираторным дистресс-синдромом (ОРДС), подвергающихся легочно-защитным стратегиям вентиляции [51]. Соответственно, повторение эхокардиографии через регулярные промежутки времени может быть полезным, особенно при повышении ЦВД. Ведение таких пациентов является сложной задачей и может включать изменение параметров вентиляции и введение инотропных препаратов. Выбор терапии для данного пациента основан на комплексном анализе последствий дисфункции правого желудочка на тканевую перфузию, венозный застой и постоянную потребность в определенных параметрах вентиляции.
На этапе деэскалации ситуация еще более сложная. Пациенты обычно находятся под минимальным наблюдением, а показатели толерантности четко не определены. Должны ли мы по-прежнему ориентироваться на те же значения, что и на этапе оптимизации? Вероятно, нет, но остается неизвестным, как определить допустимый уровень нарушений. Логично не возвращаться к шоку (поэтому термин «де-раенимация» неуместен). Тем не менее, некоторая степень снижения артериального давления и кровотока может быть допустима при условии сохранения оксигенации тканей и их функции. Очевидно, что деэскалация должна быть остановлена до возникновения гипоперфузии. Например, было показано, что чрезмерное удаление жидкости с помощью ультрафильтрации связано с повышенной смертностью [52]. Мониторинг может помочь ограничить или предотвратить неблагоприятные события во время деэскалации. Тестирование реакции на преднагрузку перед удалением жидкости может выявить пациентов, для которых это будет вредно [53]. Кроме того, измерение кожной перфузии во время удаления жидкости может выявить пациентов, у которых она будет плохо переноситься, до появления гипоперфузии и новой гиперлактатемии [54]. Для деэскалации вазопрессоров оценка динамической эластичности артерий, отношение изменений пульсового давления к визменениям УО может помочь в прогнозировании гипотензии и выявлении кандидатов на снижение дозы вазопрессоров [55].
Персонализация жизнеспасающей терапии
Персонализированные подходы к инфузии, использованию вазопрессоров и инотропов должны быть адаптирована к оценке состояния тканевой перфузии и сердечно-сосудистой системы с учетом ответа на терапию.
Индивидуальное подходы к инфузионной терапии
При септическом шоке крайне важно обеспечить инфузионную терапию. Во время фазы спасения жидкости можно вводить в больших количествах, так как польза в значительной степени перевешивает риски. При оптимизации ситуация сложнее. Доля пациентов, отвечающих на введение жидкости, прогрессивно снижается [13], а вероятность нежелательных явлений возрастает. Стратегии по формуле, будь то «сухие» или «влажные», явно не подходят [56], и предпочтение отдается персонализированным стратегиям.
Персонализированный способ введения жидкости включает несколько этапов. Во-первых, должно быть четкое указание на необходимость введения жидкости, т. е. нарушение перфузии, которое, как ожидается, будет корректироваться в ответ на введение жидкости. Во-вторых, следует прогнозировать реакцию пациента на жидкости. Прогноз реакции на инфузию лучше достигается с помощью динамических тестов [57], а не статических измерений преднагрузки. В-третьих, следует тщательно оценить реакцию на введение жидкости [34]. Во время фазы стабилизации следует свести к минимуму введение жидкости [58]. В фазе деэскалации необходимо обеспечить безопасный вывод жидкости с помощью диуретиков или ультрафильтрации при минимальном мониторинге. Во-первых, идентификация пациента, потенциально получающего пользу от удаления жидкости, имеет решающее значение. Пациенты с признаками легочного или системного венозного застоя являются идеальными кандидатами [34]. Измерение внесосудистой жидкости легких (EVLW) с помощью TPTD или ультразвука) может использоваться для начала удаления жидкости и оценки его эффективности. Как и для многих других переменных, цель EVLW должна быть индивидуальной. Как указывалось выше, кажется логичным не отменять инфузионную терапию у пациентов, реагирующих на инфузию, поскольку это может поставить под угрозу состояние их гемодинамики [53]. Во-вторых, следует проверить показатели непереносимости удаления жидкости. Действительно, индивидуальную скорость наполнения капилляров трудно оценить в клинической практике, а высокая скорость удаления жидкости недопустима.
В то время как рекомендации предлагают сбалансированные кристаллоиды [3], при выборе между альбумином и кристаллоидами, а также между 0,9% физиологическим раствором и сбалансированными кристаллоидами (на основе уровней хлоридов) следует учитывать индивидуальные факторы, такие как уровни хлоридов и альбумина, а также наличие отека. Во время стабилизации и деэскалации следует также попытаться свести к минимуму «нереанимационные жидкости» и натриевую нагрузку [58].
Персонализированное использование вазопрессоров
Вазопрессоры начинают, титруют и отменяют в соответствии с СрАД, показателями перфузии и функции органов, как указано выше. Они различаются по своей фармакологии, влиянию на капиллярную перфузию, функции органов и профилям безопасности (Table3).
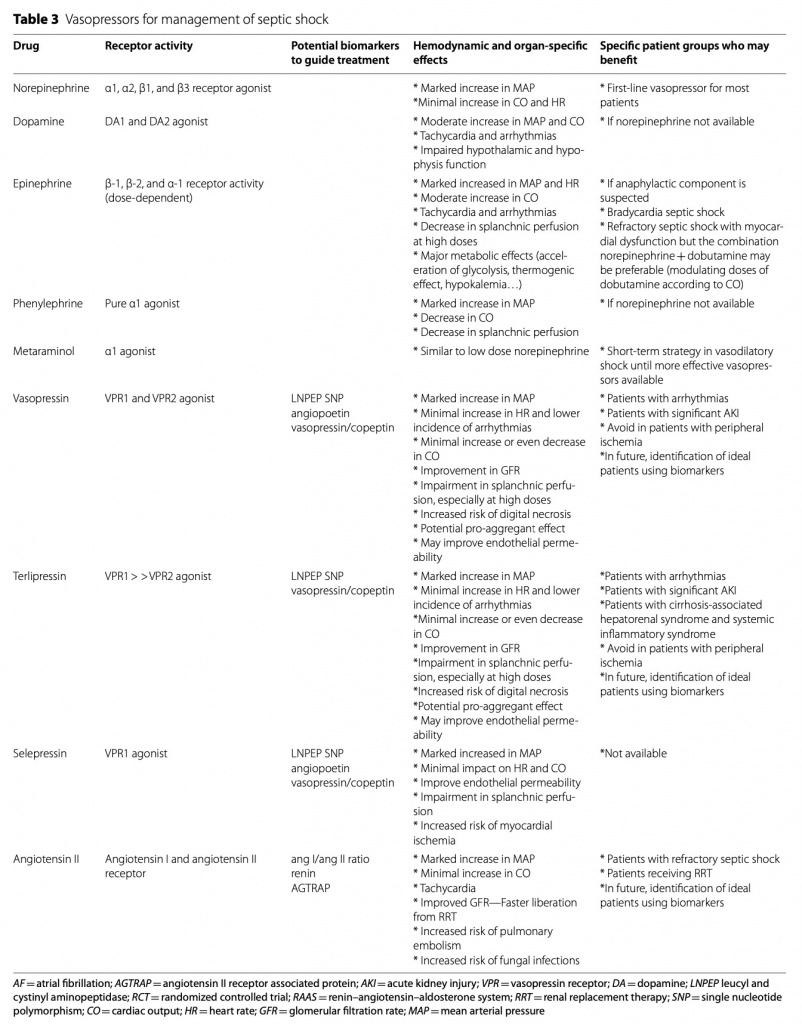
Норэпинефрин рекомендуется в качестве вазопрессора первой линии при септическом шоке на основании данных большого количества РКИ, сравнивающих норадреналин и дофамин, и нескольких мета-анализов [59, 60]. Кроме того, дефицит норадреналина и его замена другими вазопрессорами были связаны с повышенной смертностью [61]. В целом эти данные подтверждают, что норадреналин является вазопрессором первой линии. Вазопрессин изучался в качестве основного агента и в комбинации с норадреналином [62–64]. В то время как не было никакой разницы в смертности, вазопрессин был связан с меньшим количеством аритмий, меньшей потребностью в заместительной почечной терапии (ЗПТ), но более высокой частотой ишемии внутренних органов и пальцев [65]. Об аналогичном эффекте сообщалось при применении терлипрессина [66, 67], но прямого сравнения с вазопрессином не проводилось. Применение селепрессина у пациентов с септическим шоком без оценки кровотока не продемонстрировало положительного влияния на исход [68], несмотря на благоприятный профиль в доклинических исследованиях [69].
Ангиотензин II появился как новый вазопрессор в лечении вазодилататорного шока. Он эффективен для повышении артериального давления и обладает катехоламин-сберегающим эффектом по сравнению с плацебо [70]. Апостериорный анализ пациентов, получавших ЗПТ, показал улучшение выживаемости и более раннее прекращение ЗПТ у пациентов, которые были рандомизированы в группу ангиотензина II [71]. Остаются важные вопросы, касающиеся оптимального выбора вазопрессоров, роли комбинированной терапии и наиболее эффективного и безопасного метода эскалации в различных когортах пациентов [72]. Необходимы дополнительные методы информирования клиницистов о наиболее эффективных вазопрессорах в конкретных условиях и о том, как избежать вреда от их использования.
Несколько генетических полиморфизмов связаны с различными ответами на вазопрессоры [73, 74], но эта таргетная стратегия еще не подходит для применения у постели больного. В качестве альтернативы можно использовать биомаркеры, чтобы указать, какая группа пациентов может получить больше пользы от конкретного агента. Плазменный ангиопоэтин 1 (Ang1) и ангиопоэтин 2 (Ang2), медиаторы сосудистой проницаемости, стали потенциальными биомаркерами для управления терапией вазопрессином. Ренин сыворотки и соотношение ангиотензин I/II отражают активность ангиотензин-превращающих ферментов [75] и являются многообещающими биомаркерами для выявления пациентов с вазодилататорным шоком, для которых лечение ангиотензином II может быть полезным [76]. Необходимо подтверждение в проспективных исследованиях.
Наконец, недостаточно данных об оптимальной терапевтической стратегии при шоке, требующем высоких доз вазопрессоров. Рецепторы α1, как и любые другие вазопрессорные рецепторы, могут быть насыщенными и/или гипореактивными при рефрактерном шоке. Имеет смысл рассмотреть альтернативные вазопрессоры, действующие на разные рецепторы (производные вазопрессина или ангиотензин II), а не использовать агент того же класса. Точно так же показания к дополнительной терапии различаются, и необходимы прогностические критерии для определения показаний и оценки эффективности. Выявить пациентов, отвечающих на кортикостероиды, может помочь анализ выбранных цитокинов [77] или идентификация специфических транскриптомных эндотипов [78]. В связи с отсутствием своевременного выполнения этих методик использование гидрокортизован в настоящее время рассматривается у больных, получающих высокие дозы вазопрессорных средств.
Персонализированное использование инотропных средств
Нет данных, подтверждающих систематическое использование инотропных средств. Неразборчивое применение левосимендана у таких больных оказалось безуспешным [79]. Даже попытка идентифицировать пациентов с повреждением миокарда на основе биомаркеров оказалась бесполезной [80]. Это неудивительно, поскольку последствия сепсис-ассоциированной депрессии миокарда весьма вариабельны. У некоторых пациентов наблюдается высокий СВ [47] или даже динамическая обструкция выводного тракта левого желудочка [81], несмотря на значительное нарушение сердечной функции или высокие уровни биомаркеров.
Их не следует лечить инотропными средствами. С другой стороны, у некоторых пациентов низкий СВ связан с дисфункцией левого или правого желудочка [47], и им могут помочь инотропные препараты. Соответственно, как указано выше, инотропы могут быть показаны только пациентам с признаками тканевой гипоперфузии, связанной с низким СВ, вызванным нарушением функции сердца. Побочные эффекты (тахикардия, аритмии) и специфические риски у некоторых категорий пациентов (гипертрофические кардиомиопатии, ишемия миокарда) должны быть тщательно изучены, а риск/польза вмешательства оценены.
Обсуждение типа агента является более сложным. Доказано, что ни один из агентов не превосходит другой у пациентов с шоком. Следует отметить, что большинство исследований, сравнивающих инотропные препараты, проводились у пациентов с сердечной недостаточностью и исключали пациентов с кардиогенным шоком. Соответственно, метаанализы этих исследований следует рассматривать с осторожностью.
Основываясь на фармакологических свойствах, мы предлагаем следующий поэтапный подход: сначала протестируйте ограниченную дозу добутамина (от 2,5 до 5 мкг/кг/мин) и оцените эффективность и переносимость. В случаях тяжелого нарушения сократимости миокарда можно рассмотреть более высокие дозы (до 20 мкг/кг/мин). Во-вторых, замените или добавьте эноксимон или милринон и оцените эффективность и переносимость (остерегайтесь риска гипотензии). В-третьих, замените или добавьте левосимендан в случаях тяжелых нарушений. На каждом этапе следует оценивать эффективность (улучшение сердечной функции и сердечного выброса, устранение тканевой гипоперфузии) и переносимость (например, отсутствие тахикардии, аритмий и т. д.). Для каждого из агентов следует вводить наименьшую дозу, связанную с желаемым эффектом. Как только ситуация улучшится, следует попытаться отменить инотропы.
Выводы
Несмотря на то, что для ведения септического шока применяются некоторые общие правила, следует учитывать индивидуальный подход для гемодинамического мониторинга и поддержки. Важно отметить, что мониторинг и поддержка должны быть адаптированы к четырем стадиям шока, а воздействие вмешательств должно постоянно оцениваться.
References:
1. Cecconi M ,DeBacker D, Antonelli M, Beale RJ, Bakker J, Hofer C, Jaeschke R, Mebazaa A, Pinsky MR,T ebou lJL,et al. Consensus on circulatory shock and hemodynamic monitoring. Task force of the European Society of Intensive Care Medicine. IntensiveCareMed.2014;40(12):1795–815.
2. Vincent JL, DeBacker D. Circulatory shock.NEnglJMed.2013;369(18):1726–34.
3. Evans L, Rhodes A, Alhazzani W, Antonelli M, Coopersmith CM , French C, Machado FR, McIntyre L, Ostermann M, Prescott HC, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021.IntensiveCareMed.2021;47(11):1181–247.
4. Vincent JL, Singer M, Einav S, Moreno R, Wendon J, Teboul JL, Bakker J, Hernandez G, AnnaneD, deManAME, et al. Equilibrating SSC guidelines with individualized care. CritCare.2021;25(1):397.
5. Coopersmith CM, DeBackerD, DeutschmanCS, FerrerR, MachadoFR, MartinGS, Martin‑Loeches I,Nunnally ME, Antonelli M, et al. Surviving sepsis campaign: research priorities for sepsis and septic shock.IntensiveCareMed.2018;44(9):1400–26.
6. Ait‑Oufella H, BigeN, BoellePY, PichereauC, Alves M,Bertinchamp R, BaudelJL, GalboisA, MauryE, GuidetB. Capillary refill time exploration during septic shock. Intensive Care Med. 2014. https://doi.org/10.1007/s00134‑014‑3326‑4.
7. Ait‑Oufella H, LemoinneS, BoellePY, Galbois A,Baudel JL,Lemant J, JoffreJ, MargetisD, GuidetB, MauryE, et al. Mottlings core predicts survivalin septic shock.IntensiveCareMed.2011;37(5):801–7.
8. DeBackerD, Vieillard‑Baron A.Clinical examination: a trigger but not a substitute for hemodynamic evaluation. Intensive Care Med. 2019;45(2):269–71.
9. Zieleskiewicz L, Lopez A, Hraiech S, Baumstarck K, Pastene B, Di BisceglieM, Coiffard B, Duclos G, Boussuges A, Bobbia X, et al. Bedside POCUS during ward emergencies is associated with improved diagnosis and outcome: an observational, prospective, controlled study. Crit Care.2021;25(1):34.
10. Teboul JL, Saugel B, Cecconi M, De Backer D, Hofer CK, Monnet X, PerelA, PinskyMR, ReuterDA, RhodesA, e tal. Less invasive hemodynamic Monitoring in critically ill patients.IntensiveCareMed.2016;42(9):1350–9.
11. BréchotN, HajageD, KimmounA, DemiselleJ, AgerstrandC, MonteroS, SchmidtM, LuytCE, LebretonG, HékimianG,et al.Venoarterial extraсorporeal membrane oxygenation to rescue sepsis‑induced cardiogenic shock: a retrospective, multicentre, international cohort study. Lancet.2020;396(10250):545–52.
12. Cecconi M, HernandezG, DunserM, AntonelliM, BakerT, BakkerJ, DuranteauJ , Einav S, GroeneveldABJ, HarrisT,et al. Fluid administration for acute circulatory dysfunction using basic monitoring: narrative review and expert panel recommendations from an ESICM task force. IntensiveCareMed.2019;45(1):21–32.
13. Hernandez G, Ospina‑Tascon GA, Damiani LP, Estenssoro E, DubinA,Hurtado J,Friedman G,Castro R,Alegria L,Teboul JL, et al. Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate level son 28‑daymortality among patients with septic shock:theANDROMEDA‑SHOCKrandomizedclinicaltrial.JAMA.2019;321(7):654–64.
14. Ait‑HamouZ,TeboulJL,AnguelN,MonnetX.How to detect appositive response to a fluid bolus when cardiac output is not measured?AnnIntensiveCare.2019;9(1):138.
15. Jacquet‑LagrezeM,BouhamriN,PortranP,SchweizerR,BaudinF,LilotM,FornierW,FellahiJL.Capillaryrefilltimevariationinducedbypassivelegraising predicts capillary refill time response to volume expansion. CritCare.2019;23(1):281.
16. Vincent JL, Nielsen ND, Shapiro NI, Gerbasi ME, Grossman A, Doroff R, ZengF,YoungPJ,RussellJA.Meanarterialpressureandmortalityinpatientswithdistributiveshock:aretrospectiveanalysisoftheMIMIC‑IIIdatabase.AnnIntensiveCare.2018;8:107.
17. Persichini R, Silva S, Teboul JL, Jozwiak M, Chemla D, Richard C, Monnet X. Effects of norepinephrine on mean systemic pressure and venous return in human septic shock.CritCareMed.2012;40(12):3146–53.
18. Ospina‑Tascon GA, Hernandez G,Alvarez I, Calderon‑TapiaLE, Manzano‑Nunez R, Sanchez‑Ortiz AI, Quinones E, Ruiz‑Yucuma JE, Aldana JL, TeboulJL, et al. Effects of very early start of norepinephrine in patients with septic shock: a propensity score‑basedanalysis.CritCare.2020;24(1):52.
19. Ospina‑Tascón GA, Teboul JL, Hernandez G, Alvarez I, Sánchez‑Ortiz AI,Calderón‑TapiaLE,Manzano‑NunezR,QuiñonesE,Madriñan‑NaviaHJ,RuizJE,etal.Diastolic shock index and clinical outcomes in patients with septic shock.AnnIntensiveCare.2020;10(1):41.
20. DeBacker D,Creteur J, NoordallyO, SmailN, Gulbis B,Vincent JL. Does hepato‑splanchnic VO2/DO2 dependency exist in critically ill septicpatients?AmJRespirCritCareMed.1998;157:1219–25.
21. De Backer D, Creteur J, Preiser JC, Dubois MJ, Vincent JL. Microvascular blood flow is altered in patients with sepsis.AmJRespirCritCareMed.2002;166:98–104.
22. Hernandez G, Luengo C, Bruhn A, Kattan E, Friedman G, Ospina‑Tascon GA, Fuentealba A, CastroR, RegueiraT, RomeroC, et al. When to stop septic shock resuscitation: clues from a dynamic perfusion monitoring.AnnIntensiveCare.2014;4:30.
23. BakkerJ, DeBackerD, HernandezG. Lactate‑guided resuscitation saves lives: weare not sure.IntensiveCareMed.2016;42(3):472–4.
24. Brunauer A, KoköferA, BataarO, Gradwohl‑MatisI, Dankl D,Bakker J,Dünser MW. Changes in peripheral perfusion relate to visceral organ perfusion in early septic shock: a pilot study.JCritCare.2016;35:105–9.
25. BoermaEC, KuiperMA, KingmaWP, EgbersPH, GerritsenRT, InceC. Disparity between skin perfusion and sublingual microcirculatory alteration sinse vere sepsis and septic shock: a prospective observational study.IntensiveCareMed.2008;34:1294–8.
26. Brabrand M, Hosbond S, Folkestad L. Capillary refill time: a study of inter‑observer reliability among nurses and nurse assistants. Eur J Emerg Med.2011;18(1):46–9.
27. ZampieriFG,DamianiLP,BakkerJ,Ospina‑TasconGA,CastroR,CavalcantiAB, Hernandez G. Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate levels on 28‑day mortality among patients with septic shock:a Bayesian Re analysis of the ANDROMEDA‑SHOCKTrial.AmJRespirCritCareMed.2019.https://doi.org/10.1164/rccm.201905‑0968OC.
28. LiuX, LuoD, ZhangJ,DuL. Distribution and relative expression of vasoactive receptors on arteries. SciRep. 2020;10(1):15383.
29. Asfar P, Meziani F, Hamel JF, Grelon F, Megarbane B, Anguel N, Mira JP, DequinPF, GergaudS, WeissN,etal. High versus low blood‑pressure target in patients with septic shock.NEnglJMed.2014;370(17):1583–93.
30. LamontagneF,Richards‑BelleA,ThomasK,HarrisonDA,SadiqueMZ,Grieve RD, Camsooksai J, Darnell R, Gordon AC, Henry D, et al. Effect of reduced exposure to vasopressors on 90‑day mortality in older critically Ill patients with vasodilatory hypotension: a randomized clinical trial.JAMA.2020;323(10):938–49.
31. DeruddreS, CheissonG, MazoitJX,VicautE,BenhamouD,DuranteauJ. Renal arterial resistance in septic shock: effects of in creasing mean arterial pressure with norepinephrine on the renal resistive index assessedwithDopplerultrasonography.IntensiveCareMed.2007;33(9):1557–62.
32. Gershengorn HB, StelfoxHT, NivenDJ, WunschH.Association of premorbid blood pressure with vasopressor infusion duration in patients with shock. Am J Respir Crit Care Med. 2020;202(1):91–9.
33. DeBackerD,VincentJL. Should we measure the central venous pressure to guide fluid management? Ten answers to 10 questions. Crit Care.2018;22(1):43.
34. DeBackerD,AissaouiN,CecconiM,ChewMS,DenaultA,HajjarL,Her‑nandezG,MessinaA,MyatraSN,OstermannM,etal.Howcanassessinghemodynamicshelptoassessvolumestatus?IntensiveCareMed.2022.https://doi.org/10.1007/s00134‑022‑06808‑9.
35. DeBackerD,CreteurJ,Dubois MJ,SakrY,VincentJL. Microvascular alterations in patients with acute severe heart failure and cardiogenic shock.AmHeartJ.2004;147:91–9.
36. DeBacker D, VincentJL. Early goal‑directed therapy: do we have a definitive answer?IntensiveCareMed.2016;42(6):1048–50.
37. Ospina‑Tascon GA, Umana M, Bermudez WF, Bautista‑Rincon DF, Valencia JD, Madrinan HJ, HernandezьG, Bruhn A, Arango‑Davila C, DeBacker D. Can venous‑to‑arterial carbon dioxide differences reflect microcirculatory alterations in patients with septic shock?IntensiveCareMed.2016;42(2):211–21.
38. ValleeF, ValletB ,MatheO, ParraguetteJ, MariA, SilvaS, SamiiK, FourcadeO, GenestalM .Central venous‑to‑arterial carbondioxide difference: an additional target for goal‑directed therapy in septic shock? Intensive CareMed.2008;34(12):2218–25.
39. Mesquida J, Saludes P, Gruartmoner G, Espinal C, Torrents E, Baigorri F, ArtigasA. Central venous‑to‑arterial carbondioxide difference combined with arterial‑to‑venous oxygen content difference is associated with lactate volution in the hemodynamic resuscitation process in early septic shock.CritCare.2015;19:126.
40. Ospina‑TasconGA, Bautista‑Rincon DF, Umana M, Tafur JD, Gutierrez A,GarciaAF,BermudezW,GranadosM,Arango‑DavilaC,HernandezG.Persistently high venous‑to‑arterial carbondioxide differences during early resuscitation are associated with poor outcomes in septic shock.CritCare.2013;17(6):R294.
41. DuW, LiuDW, WangXT, LongY, ChaiWZ, ZhouX, RuiX. Combining central venous‑to‑arterial partial pressure of carbon dioxide difference and central venous oxygen saturation to guide resuscitation in septic shock. JCritCare.2013;28(6):1110–5.
42. Ospina‑TasconGA, UmanaM, BermudezW, Bautista‑RinconDF, Hern‑dez G, Bruhn A, Granados M, Salazar B, Arango‑Davila C, De Backer D. Combination of arterial lactate levels and venous‑arterial CO to arterial‑venous O content difference ratio as markers of resuscitation in patientswithsepticshock.IntensiveCareMed.2015;41:796–805.
43. MonnetX,JulienF,Ait‑HamouN,LequoyM,GossetC,JozwiakM,Persi‑chiniR,AnguelN,RichardC,TeboulJL. Lactate and venoarterial carbon dioxide difference/arterial‑venous oxygen difference ratio, but not central venous oxygen saturation, predict increase in oxygen consumption in fluid responders.CritCareMed.2013;41(6):1412–20.
44. Jansen TC, van Bommel J, Schoonderbeek J, Sleeswijk Visser SJ, van der Klooster JM, LimaAP, Willemsen SP, Bakker J. Early lactate‑guided therapy in ICU patients: a multicenter, open‑label, randomized, controlled trial.AmJRespirCritCareMed.2010;182(6):752–61.
45. RimachiR, Bruzzi DC, Orellano‑Jimenez C, Cotton F,Vincent J, De Backer D. Lactate/pyruvate ratio a samarker of tissue hypoxia in circulatory and septic shock. Anaesth Intensive Care.2012;40(3):427–32.
46. KattanE, Hernández G,ьOspina‑Tascón G, Valenzuela ED, Bakker J, CastroR.A lactate‑targeted resuscitation strategy may be associated with higher mortality in patients with septic shock and normal capillary refill time: a posthoc analysis of the ANDROMEDA‑SHOCK study. Ann Intensive Care.2020;10(1):114.
47. GeriG,VignonP,AubryA,FedouAL,CharronC,SilvaS,RepesséX,Vieillard‑Baron A. Cardiovascular clusters in septic shock combining clinical and echocardiographic parameters: a posthoc analysis. Intensive Care Med.2019;45(5):657–67.
48. Kouz K, Scheeren TWL, de Backer D, Saugel B. Pulse wave analysis to estimate cardiac output. Anesthesiology.2021;134:119–26.
49. Monnet X, Teboul JL. Transpulmonary thermodilution: advantages and limits. Crit Care.2017;21(1):147.
50. Teboul JL, Sauge lB, Cecconi M, De BD, Hofer CK, Monnet X, Perel A, Pinsky MR, Reuter DA, Rhodes A, et al. Less invasive hemodynamic monitoring in critically ill patients. Intensive Care Med. 2016. https://doi.org/10.1007/s00134‑016‑4375‑7.
51. Boissier F, Katsahian S, Razazi K, Thille AW, Roche‑CampoF, Leon R, Vivier E, Brochard L, Vieillard‑Baron A, Brun‑Buisson C, et al. Prevalence and prognosis of corpulmonale during protective ventilation for acute Respiratory distress syndrome. IntensiveCareMed.2013;39(10):1725–33.
52. Murugan R, Kerti SJ, Chang CH, Gallagher M, Clermont G, Palevsky PM, Kellum JA, Bellomo R. Association of net ultrafiltration rate with mortality among critically Ill adults with acute kidney injury receiving continuous veno venous hemodiafiltration: a secondary analysis of the randomized evaluation of normal vs augmented level (RENAL) of renal replacementtherapytrial.JAMANetwOpen.2019;2(6):e195418.
53. Monnet X, Cipriani F, Camous L, Sentenac P, Dres M, Krastinova E, Anguel N, Richard C, Teboul JL. The passive legraising test to guide fluid removal in critically ill patients.AnnIntensiveCare.2016;6(1):46.
54. MongkolpunW, BakosP, VincentJL, CreteurJ. Monitoring skin blood flow to rapidly identify alterations in tissue perfusion during fluid removal using continuous veno‑venous hemofiltration in patients with circulatory shock. AnnIntensive Care.2021;11(1):59.
55. Guinot PG, Bernard E, Levrard M, Dupont H, Lorne E. Dynamic arterial elastance predicts mean arterial pressure decrease associated with decreasing norepinephrine dosage in septic shock. Crit Care.2015;19:14.
56. Meyhoff TS, Hjortrup PB, Wetterslev J, Sivapalan P, Laake JH, Cronhjort M, Jakob SM, Cecconi M, Nalos M, Ostermann M ,et al .Restriction Of intravenous fluid in ICU patients with septic shock. N Eng l J Med.2022;386(26):2459–70.
57. Monnet X, Shi R, Teboul JL. Prediction of fluid responsiveness.What’s new? Annal Intensive Care.2022;12(1):46.
58. VanRegenmorte lN, Verbrugghe W, Roelant E, VandenWyngaert T, Jorens PG. Maintenance fluid therapy and fluid creep impose more significant fluid, sodium, and chloride burdens than resuscitation fluids in critically ill patients: a retrospective study in a tertiary mixed ICU popula‑tion.IntensiveCareMed.2018;44(4):409–17.
59. De Backer D, Biston P, Devriendt J, Madl C, Chochrad D, Aldecoa C, Brasseur A, Defrance P, Gottignies P, VincentJL. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med.2010;362(9):779–89.
60. DeBacker D, Aldecoa C, Njimi H, Vincent J‑L. Dopamine versus norepinephrine in the treatment of septic shock: a meta analysis.CritCareMed.2012;40:725–30.
61. Vail E, Gershengorn HB, Hua M, Walkey AJ, Rubenfeld G, Wunsch H. Association between US norepinephrine short age and mortality among patients with septic shock. JAMA.2017;317(14):1433–42.
62. Russell JA, Walley KR, Singer J, Gordon AC, Hebert PC, Cooper DJ, Holmes CL, Mehta S, Granton JT, Storms MM, et al. Vasopressin versus norepinephrine infusion in patients with septic shock.NEnglJMed.2008;358(9):877–87.
63. Gordon AC, Mason AJ, Thirunavukkarasu N, Perkins GD, Cecconi M, Cepkova M, Pogson DG, Aya HD, Anjum A, Frazier GJ, et al. Effect of early vasopressin vs norepinephrine on kidney failure in patients with septic shock: The VANISHrandomizedclinicaltrial.JAMA.2016;316(5):509–18.
64. Hajjar LA, Vincent JL, Barbosa Gomes Galas FR, Rhodes A, Landoni G, Osawa EA, Melo RR, Sundin MR, Grande SM, Gaiotto FA, et al. Vasopressin versus norepinephrine in patients with vasoplegic shock after cardiac surgery: the VANCS randomized controlled trial. Anesthesiology.2017;126(1):85–93.
65. Nagendran M, Russell JA, Walley KR, Brett SJ, Perkins GD, HajjarL, MasonAJ, AshbyD, Gordon AC. Vasopressin in septic shock: an individual patient datameta‑analysis of randomized controlled trials.IntensiveCareMed.2019;45(6):844–55.
66. Liu ZM, Chen J, Kou Q, Lin Q, Huang X, Tang Z, Kang Y, Li K, Zhou L, Song Q, et al. Terlipressin versus norepinephrine as infusion in patients with septic shock: a multicentre, randomised, double‑blinded trial. Intensive Care Med.2018;44(11):1816–25.
67. Zhu Y, Huang H, Xi X, Du B. Terlipressin for septic shock patients: a meta‑analysis of randomized controlled study. J Intensive Care.2019;7:16.
68. Laterre PF, Berry SM, Blemings A, Carlsen JE, Francois B, Graves T, Jacobsen K, Lewis RJ, Opal SM, PernerA, et al. Effect of selepressin vs placebo on ventilator‑ and vasopressor‑free days in patients with septic shock: the SEPSIS‑ACT randomized clinical trial.JAMA.2019.https://doi.org/10.1001/jama.2019.14607.
69. Rehberg S , Ertmer C, Vincent JL, Morelli A, Schneider M, Lange M, VanAken H, Traber DL, Westphal M. Role of selective V1a receptor agonism in ovine septic shock. Crit Care Med.2011;39(1):119–25.
70. Khanna A, English SW , Wang XS, Ham K, Tumlin J, Szerlip H, Busse LW, Altawee lL, Albertson TE, Mackey C, et al. Angiotensin II for the treatment of vasodilatory shock. N Engl J Med.2017;377(5):419–30.
71. Tumlin JA, Murugan R, Deane AM, Ostermann M, Busse LW, Ham KR, Kashani K, Szerlip HM, Prowle JR, Bihorac A, et al. Outcomes in patients with vasodilatory shock and renal replacement therapy treated with intravenous angiotensin II. Crit Care Med.2018;46(6):949–57.
72. Chawla LS, Ostermann M, ForniL, Tidmarsh GF. Broad spectrum vasopressors: a new approach to the initial management of septic shock? CritCare.2019;23(1):124.
73. Nakada TA, Russell JA, Boyd JH, Aguirre‑Hernandez R, Thain KR, Thair SA, Nakada E, McConechy M, Walley KR. beta2‑Adrenergic receptor gene polymorphism is associated with mortality in septic shock. Am J RespirCritCareMed.2010;181(2):143–9.
74. Anantasit N, Boyd JH, Walley KR, Russell JA. Serious adverse events associated with vasopressin and norepinephrine infusion in septic shock. CritCareMed.2014;42(8):1812–20.
75. Chawla LS, Chen S, Bellomo R, Tidmarsh GF. Angiotensin converting enzyme defects in shock: implications for future therapy. Crit Care.2018;22(1):274.
76. Bellomo R, Forni LG, Busse LW, McCurdy MT, Ham KR, Boldt DW, Hästbacka J, Khanna AK, Albertson TE, Tumlin J, et al. Renin and survival inpatients given angiotensin II for catecholamine‑resistant vasodilatoryshock.Aclinicaltrial.AmJRespirCritCareMed.2020;202(9):1253–61.
77. Bentzer P, Fjell C, Walley KR, Boyd J, Russell JA. Plasma cytokine levels predict response to corticosteroids in septic shock. Intensive Care Med.2016;42(12):1970–9.
78. Antcliffe DB, Burnham KL, Al‑Beidh F, Santhakumaran S, Brett SJ, Hinds CJ, Ashby D, Knight JC, Gordon AC. Transcriptomic signatures in sepsis and a differential response to steroids. From the VANISH randomized trial. Am JRespirCritCareMed.2019;199(8):980–6.
79. GordonAC,PerkinsGD,SingerM,McAuleyDF,OrmeRM,Santhaku‑maranS,MasonAJ,CrossM,Al‑BeidhF,Best‑LaneJ,etal.Levosimendanfor the prevention of acute organ dysfunction in sepsis. N Engl J Med.2016;375:1638–48.
80. Antcliffe DB, Santhakumaran S, Orme RML, Ward JK, Al‑Beidh F, O’Dea K, Perkins GD, Singer M, McAuley DF, Mason A J, et al. Levosimendan in septic shock in patients with biochemical evidence of cardiac dysfunction: a subgroup analysis of the LeoPARDS randomized trial. Intensive Care Med.2019;45(10):1392–400.
81. Chauvet JL, El‑Dash S, Delastre O, Bouffandeau B, Jusserand D, Michot JB, Bauer F , Maizel J, Slama M. Early dynamic left intraventricular obstructtion is associated with hypovolemia and high mortality in septic shock patients. Crit Care.2015;19:262.
Источник фотоиллюстрации - www.freepik.com
[~DETAIL_TEXT] => DeBacker D. et al. A plea for personalization of the hemodynamic management of septic shock Призыв кперсонализации коррекции гемодинамики при септическом шоке Critical Care (2022)26:372doi.org/10.1186/s13054-022-04255-y
Абстракт
Несмотря на то, что руководства содержат отличные рекомендации специалистов по ведению пациентов с септическим шоком, они оставляют место для персонализации в зависимости от состояния пациентов. Мониторинг гемодинамики зависит от фазы развития: спасение, оптимизация, стабилизация и деэскалация. На начальном этапе во время спасательной фазы мониторинг для определения этиологии и тяжести шока должен включать измерение артериального давления и лактата вместе с клиническим обследованием, особенно определением пятнистости кожи и времени наполнения капилляров. Низкое диастолическое давление может мотивировать к использованию вазопрессоров.
На этой стадии эхокардиография может быть полезна для выявления выраженной сердечной дисфункции. На этапе оптимизации следует проводить эхокардиографический мониторинг, с оценкой тканевой перфузии путем измерения центральной или смешанной венозной сатурации кислородом, измерения лактата и вено-артериального градиента углекислого газа. Транспульмональная термомодуляция и катетеризация легочной артерии должны рассматриваться у наиболее тяжелых пациентов. Инфузионная терапия также зависит от фаз шока. В то время как предусмотрена либеральная стратегия инфузионной терапии во время фазы реанимации, следует оценить реакцию на инфузионную терапию во время фазы оптимизации. Во время стабилизации инфузия жидкости должна быть сведена к минимуму. На этапе деэскалации может быть обеспечено безопасное удаление жидкости за счет сохранения тканевой перфузии. В качестве вазопрессорной терапии первой линии рекомендуется норэпинефрин, в то время как у некоторых пациентов предпочтение отдается вазопрессину.
Остаются важные вопросы относительно оптимального выбора вазопрессоров, комбинированной терапии и наиболее эффективной и безопасной эскалации. Ренин сыворотки и соотношение ангиотензина I/II могут выявить пациентов, которые получают наибольшую пользу от ангиотензина II.Оптимальная терапевтическая стратегия при шоке, требующем высоких доз вазопрессоров, ограничена. Во всех случаях вазопрессорная терапия должна быть индивидуализирована и основана на клинической оценке и измерениях кровотока, чтобы избежать чрезмерной вазоконстрикции. Инотропы следует рассматривать у пациентов со сниженной сердечной сократимостью, связанной с нарушением тканевой перфузии. Исходя из фармакологических свойств, мы предлагаем в качестве первого теста ограниченную дозу добутамина, добавить эноксимон или милринон во вторую линию и заменить или добавить левосимендан, если нет эффекта. Что касается дополнительной терапии, то хотя гидрокортизон в настоящее время рекомендуется пациентам, получающим высокие дозы вазопрессоров, в будущем пациентов, отвечающих на кортикостероиды, можно будет идентифицировать с помощью анализа выбранных цитокинов или специфических транскриптомныхэ ндотипов.
Несмотря на то, что для лечения шока применяются некоторые общие правила, следует учитывать индивидуальный подход для мониторинга и поддержки гемодинамики.
Ключевые слова: артериальное давление, сердечный выброс, тканевая перфузия, жидкости, вазопрессорные средства, инотропные средства.
Шок — опасное для жизни состояние, характеризующееся неадекватной доставкой кислорода к тканям [1]. Септический шок является одной из наиболее частых причин шока в отделении интенсивной терапии(ОИТ) [2]. Рекомендации Surviving Sepsis Campaign (SSC) представляют собой отличное руководство по ведению пациентов с сепсисом [3], но по ряду причин здесь есть место для персонализации [4]. Во-первых, хотя эти рекомендации подтверждаются доказательствами, они основаны главным образом на рандомизированных контролируемых исследованиях (РКИ), в которых изучалась реакция больших групп пациентов на вмешательство. Эти исследования, как правило, негативны, т. е. не выявляют различий в смертности. Важно осознавать, что индивидуальные особенности пациента могут влиять на реакцию или переносимость данного вмешательства. Во-вторых, многие области реанимации до сих пор являются предметом дискуссий и остаются пробелы в исследованиях [5].
Следовательно, руководящие принципы часто не содержат сильных и точных рекомендаций в конкретных областях. В-третьих, существуют разные этапы лечения шока [2], каждый из которых требует своего подхода. Таким образом, может быть оправдано индивидуализация терапевтических подходов в зависимости от состояния пациента. В этом экспертном заключении мы обсуждаем различные варианты персонализации гемодинамического мониторинга и ведения пациентов на разных стадиях септического шока. Общий принцип персонализированного лечения шока заключается в измерении, интерпретации, применении терапии, оценке ее эффектов и реагировании, в отличие от применения стандартных мер.
Персонализация мониторинга
Персонализация гемодинамического мониторинга подразумевает рассмотрение различных фаз SOSD(спасение, оптимизация, стабилизация и деэскалация). На каждом этапе доступные методы и цели различаются (Fig.1and Table1).


Время распознавания шока: фаза спасения
Во время распознавания и идентификации шока первоначальное лечение направлено на обеспечение уровня перфузии тканей, совместимого с жизнью. В этой фазе гемодинамический мониторинг часто является очень простым, а терапевтические возможности ограничены жидкостями и вазопрессорами.
Какую информацию можно получить из базового гемодинамического мониторинга при проведении реанимационных мероприятий?
Клиническая оценка имеет решающее значение для выявления гипоперфузии тканей. Измерение артериального давления, пятнистость кожи и время наполнения капилляров (CRT) информируют о ходе реанимации. Изменения показателей CRT и пятнистости могут использоваться для базового мониторинга, поскольку они коррелируют с исходом [6, 7] и быстро реагируют на проводимую терапию. Однако они плохо коррелируют с сердечным выбросом (СВ), не позволяют идентифицировать источник тканевой гипоперфузии и определить необходимые мероприятия [8].
Если есть кардиологический анамнез или если пациент не реагирует на жидкости, для уточнения оценки гемодинамики полезно быстрое эхокардиографическое исследование [1]. Эхокардиография у постели больного является единственным методом, который позволяет быстро оценить СВ наряду с идентификацией причины низкого СВ. В недавнем РКИ использование эхокардиографии группой быстрого реагирования было связано с улучшением выживаемости [9].
Во время фазы спасения инотропы могут быть показаны, когда соответствующий кардиогенный компонент (связанный с септической кардиомиопатией или сопутствующими заболеваниями пациента) способствует шоковому процессу [1, 10]. Это можно определить только с помощью эхокардиографии, и инотропы следует рассматривать, когда СВ низкий из-за серьезного нарушения сократительной способности сердца. При тяжелом кардиогенном шоке эхокардиография может также быстро выявить пациентов, не отвечающих на первоначальную терапию, и для которых может быть рассмотрена механическая поддержка сердца [11].
Базовый клинический мониторинг играет роль в выявлении пациентов, которые могут реагировать на жидкости, и оценке их реакции [12]. В частности, время наполнения капилляров можно использовать для оценки перфузионной реакции тканей и определения необходимости дальнейшего введения жидкостей [13].
Динамические тесты, такие как реакция пульсового давления или время наполнения капилляров на пассивное поднятие ноги, могут использоваться для прогнозирования реакции на жидкость [14, 15]. Однако эти тесты трудно проводить на этапе спасения, когда одновременно применяется множество вмешательств. Прогнозирование реакции на инфузию и оценка эффектов инфузии должны быть предприняты как можно скорее, особенно у пациентов с плохой функцией сердца.
Измерение уровня лактата в крови полезно для выявления нарушений тканевой перфузии. Кроме того, когда установлен центральный венозный катетер, центральная венозная сатурация O2 (ScvO2) и градиент парциального давления углекислого газа (pCO2) между центральной венозной и артериальной кровью (Pv-aCO2) могут быть полезны для оценки эффективности проводимых мероприятий.
Как определить пациентов, у которых немедленная вазопрессорная терапия приносит пользу, не дожидаясь результатов инфузионной терапии?
В то время как некоторые пациенты могут реагировать только на инфузионную терапию, другим требуется вазопрессорная поддержка. Руководящие принципы SSC рекомендуют поддерживать среднее артериальное давление (САД) ≥ 65 мм рт. ст., но не указывают сроки или не дают указаний по приоритетности жидкости по сравнению с вазопрессорами. Некоторым пациентам с тяжелой гипотензией может потребоваться раннее начало введения вазопрессоров, т. е. не дожидаясь эффекта жидкости, для ускорения восстановления артериального давления. Действительно, отсрочка коррекции гипотензии связана с плохим исходом [16]. Более того, норадреналин может способствовать увеличению преднагрузки на сердце [17], что может снизить потребность в жидкости. В обсервационном исследовании с использованием сопоставления склонности раннее начало норадреналина было связано с менее положительным балансом жидкости и более низкой 28-дневной смертностью [18].
Решение о раннем назначении вазопрессоров наряду с инфузионной терапией кажется логичным в случаях выраженной гипотензии, хотя точного порога САД дать нельзя. Диастолическое давление (ДАД) также может влиять на принятие решения.. При сепсисе низкое ДАД часто отражает выраженную вазодилатацию и связано с повышенной смертностью [19]. Поэтому представляется логичным начинать назначение вазопрессоров при очень низком ДАД, например, < 45 мм рт.ст. У пациентов с тахикардией высокие значения индекса диастолического шока (ИДШ): соотношение между ДАД и ЧСС, связаны с более высоким риском смерти у больных с септическим шоком [19]. Следует ли использовать ИДШ> 2 для начала введения вазопрессоров, остается неизвестным.
Фаза оптимизации: инструменты и цели
На этом этапе целью реанимационных мероприятий является оптимизация тканевой перфузии за счет оптимизации перфузионного давления и СВ. В идеале это также должно включать оптимизацию регионарного распределения кровотока и микроциркуляторной перфузии. Хотя изменения в распределении регионарного кровотока [20] и микрососудистой перфузии [21] часты при шоке и могут быть отделены от системного кровообращения, в клинической практике их нелегко контролировать.
Наиболее частые показатели тканевой гипоперфузии, используемые у постели больного, включают артериальное давление, диурез, кожную перфузию, время наполнения капилляров, ScvO2, Pv-aCO2 и концентрацию лактата. Важно отметить, что даже если на исходном уровне существует некоторая корреляция между различными индексами, некоторые переменные нормализуются быстрее, чем другие [22]. ScvO2, по-видимому, нормализуется быстрее всего, за ним следуют CRT и Pv-aCO2, которые обычно нормализуются в течение 6–8 часов, в то время как лактат и подъязычная микроциркуляция могут нормализоваться более, чем через 24 часа [13]. Кажется логичным объединить несколько переменных и прекратить реанимационные мероприятия, когда большинство из них нормализуются, не прибегая к нормализации переменных, таких как концентрации лактата [23]. При обнаружении тканевой гипоперфузии следует оценить реакцию на инфузионную терапию, а в некоторых случаях следует рассмотреть возможность применения передовых гемодинамических методов для оценки сердечно-сосудистой функции.
Время наполнения капилляров (CRT)
CRT является маркером гипоперфузии кожи, динамически реагирующей на вазоактивные вещества. В какой степени время наполнения капилляров отражает центральную перфузию остается неизвестной. В то время как одно исследование пришло к выводу, что CRTотражает центральное кровообращение [24], другие исследования предполагают некоторую диссоциацию [22, 25]. Измерения CRT показывают значительную изменчивость между наблюдателями [26], но это можно свести к минимуму с помощью стандартизации метода [13]. По сравнению с реанимацией, нацеленной на лактат при раннем септическом шоке реанимация под контролем CRT, как правило, лучше [13, 27]. Среди факторов, способствующих этим различиям, более частые оценки кровообращения в группе CRT. Достижение значения CRT< 3 с является ценным ориентиром эффективных мероприятий, в то время как медленное снижение уровня лактата само по себе может привести к дополнительному введению жидкости, даже если перфузия тканей могла нормализоваться на момент оценки.
Среднее артериальное давление
Определение целевого системного артериального давления, необходимого для достижения адекватной тканевой перфузии, остается сложной задачей. В принципе, органный кровоток зависит от перфузионного давления (т. е. разницы между давлением притока и оттока) и сопротивления. Однако сохранения системного артериального давления недостаточно для обеспечения адекватности микроциркуляторного русла. Важно отметить, что перфузионное давление различается в зависимости от сосудистого русла (Table2), и эти уровни также могут повреждаться при сепсисе.

Большинство органов обладают эндогенной способностью сохранять микроциркуляцию в определенном диапазоне перфузионных давлений. Например, сердце и мозг могут поддерживать постоянный кровоток, несмотря на большие изменения перфузионного давления. В случае, если давление падает ниже органоспецифической зоны ауторегуляции, органный кровоток становится зависимым от давления притока, поэтому основное внимание уделяется устранению гипотонии в фазу спасения.
Неоднородность пациентов, различная органоспецифическая регуляция микроциркуляции, вариабельная плотность рецепторов и влияние фармакологических взаимодействий затрудняют единый подход к лечению септического шока [28]. Руководство SSC рекомендует начальное целевое среднее артериальное давление 65 мм рт. ст. [3], но не содержит рекомендаций для более поздних стадий. Данные наблюдений показывают, что органная дисфункция иногда может начаться уже при падении СрАД ниже 75–80 мм рт. ст. [16], но для достижения более высоких целевых значений СрАД часто требуются более высокие дозы вазопрессоров, которые могут быть связаны с большим количеством побочных эффектов.
Исследования, рандомизирующие пациентов с сепсисом в группы с целевым значением СрАД ~ 65 мм рт. ст. или даже меньше по сравнению с от~ 75 и до ~ 85 мм рт. ст., не показали различий в смертности [29, 30]. Положительное влияние более высокого среднего артериального давления на функцию почек у ранее страдающих артериальной гипертензией пациентов можно наблюдать [29], но оно не является систематическим [30]. Различия в влиянии более высоких целевых значений СрАД на функцию почек можно частично объяснить высокой вариабельностью реакции почечного кровотока на увеличение СрАД [31].
Несостоятельность подхода «один размер подходит всем» была также продемонстрирована у пациентов с артериальной гипотензией. Анализ 3542 пациентов в критическом состоянии с шоком показал, что пациенты с естественно низким АД (систолическое АД < 100 мм рт. ст.) лечились дольше и с более высокими дозами норадреналина и имели более длительное пребывание в ОИТ и более высокую смертность [32]. Соответственно, в то время как начальное целевое среднее артериальное давление 65 мм рт. ст. представляется разумным подходом для многих пациентов, идеальное среднее артериальное давление должно быть индивидуальным. Подтверждение эффективности выбранного индивидуального целевого СрАД заключается в оценке изменений показателей перфузии, таких как диурез, уровень сознания и кожная перфузия. Если наблюдаются положительные эффекты, можно использовать это новое целевое значение СрАД, если оно неэффективно или непереносимо, то следует установить начальное значение СрАД.
Центральное венозное давление (ЦВД)
ЦВД представляет собой сложную переменную, отражающую преднагрузку и функцию правого желудочка [33]. Несмотря на то, что его способность точно предсказывать реакцию на инфузионную терапию сомнительна, оно по-прежнему предоставляет важную информацию о волемическом статусе и резерве правого желудочка и должно измеряться при шоке [34]. ЦВД может быть важным ранним индикатором недостаточности правого желудочка. Устойчивое повышение ЦВД > 12 мм рт. ст. связано с нарушением функции почек и кишечника, даже когда перфузионное давление в органах остается постоянным, что свидетельствует о том, что венозный застой играет роль в органной дисфункции. Для ЦВД не должно быть целевого значения, так как идеальное ЦВД — это самое низкое ЦВД, связанное с гемодинамической стабильностью.
Сердечный выброс (СВ)
CВ является ключевым фактором перфузии тканей. Однако не существует фиксированного значения оптимального СВ при шоке, и СВ следует оптимизировать в соответствии с индексами тканевой перфузии, перечисленными ниже, и функцией органов. Важно отметить, что микрососудистые изменения могут сохраняться даже после коррекции низкого СВ, что ухудшает тканевую перфузию [21, 35]. При гиперкинетическом шоке стойкие нарушения перфузии связаны с изменениями регионарной перфузии и/или изменениями микроваскулярной перфузии. Эти микрососудистые изменения могут быть нечувствительны к увеличению СВ, поэтому следует использовать другие стратегии для улучшения микроциркуляции. Соответственно, CВ следует рассматривать как средство улучшения тканевой перфузии, а не как мишень.
Смешанное венозное (SvO2) и центральное венозное (ScvO2) насыщение кислородом
Хотя ScvO2 или SvO2 даже не упоминаются в новых рекомендациях SSC [3], они являются очень важными физиологическими переменными, которые необходимо понимать и измерять. Они отражают баланс между фактическим потреблением кислорода и доставкой кислорода тканям. Соответственно, низкий уровень ScvO2указывает на нарушение или неадекватную доставку O2, что объясняется неадекватным СО, если гемоглобин и сатурация артериальной крови O2 находятся в пределах нормы. Ожидается, что при сепсисе SvO2 и ScvO2 будут нормальными или повышенными даже при нарушении тканевой перфузии [21]. В то время как определение конкретных значений SvO2 или ScvO2 у всех пациентов было затруднено [36], обнаружение низкого SvO2 или ScvO2 может выявить пациентов, которым должны помочь дальнейшие реанимационные мероприятия. Это может заключаться в увеличении СО с помощью инфузионной терапии или инотропного агента, а иногда и гемоглобина путем переливания крови у пациентов с анемией. У пациентов с высоким ScvO2 следует тщательно проверять другие показатели нарушения перфузии.
Разница венозной и артериальной концентрации углекислого газа (Pv-aCO2)
Pv-aCO2 зависит от общего производства углекислого газа (CO2), CO и перфузии микрососудов, а также от сложной взаимосвязи между парциальным давлением CO2 и содержанием CO2 в крови. Согласно модифицированному уравнению Фика, Pv-aCO2 находится в обратной зависимости от CO (криволинейная зависимость). При стабильных условиях как потребления кислорода (VO2), так и продукции CO2 (VCO2) Pv-aCO2 прогрессивно увеличивается в ответ на снижение CO из-за застояCO2 в микрососудах. Прогрессирующее увеличение Pv-aCO2 отражает снижение микроциркуляторной перфузии на ранних стадиях септического шока [37]. Таким образом, высокое значение Pv-aCO2 может идентифицировать пациентов с сепсисом, которые неадекватно реанимированы [38]. ЗначениеPv-aCO2 [39] и изменение Pv-aCO2 в ответ на терапию связаны с исходом [40]. Измерение Pv-aCO2 может быть особенно полезным у пациентов с нормальными значениями лактата или ScvO2 для выявления пациентов с риском неблагоприятного исхода, несмотря на очевидную адекватную реанимацию [40–42]. Тем не менее, трудно рекомендовать конкретное целевое значение Pv-aCO2 на основе наблюдательных испытаний. Отношение Pv-aCO2 к артериовенозной разнице содержания кислорода является оценкой дыхательного коэффициента и, как таковая, может быть прямым показателем анаэробного метаболизма с более быстрыми изменениями, чем у лактата [42, 43].
Концентрация лактата в крови
Уровни лактата имеют сильное прогностическое значение и поэтому могут использоваться для скрининга. Оценка серийных уровней лактата полезна, так как они обычно снижаются у пациентов, которым становится лучше, и часто остаются повышенными или даже увеличиваются, когда септический шок плохо контролируется. Стратегии реанимации, направленные на снижение уровня лактата, были связаны со снижением госпитальной летальности [44]. Таким образом, кажется логичным направить реанимационную стратегию на снижение уровня лактата [3].Однако повышенный уровень лактата также может быть вызван другими причинами, помимо тканевой гипоксии (например, воспалением, снижением клиренса лактата и т. д.). У больных с шоком гиперлактатемия в первые несколько часов после поступления преимущественно гипоксического происхождения, тогда как не гипоксические причины преобладают на более поздних стадиях [45]. Снижение уровня лактата также требует времени, поэтому изолированная гиперлактатемия может сохраняться после нормализации других показателей тканевой гипоперфузии [22]. Следовательно, погоня за нормализацией лактата может быть нецелесообразной [23]. У пациентов с нормализованным временем наполнения капилляров реанимация под контролем лактата была связана с повышенной смертностью [46]. Соответственно, мониторинг уровня лактата в крови играет роль в оценке эффективности реанимационных процедур в сочетании с другими показателями тканевой гипоперфузии.
Эхокардиография
Следует рассмотреть вопрос о проведении эхокардиографии, поскольку первоначальные реанимационные процедуры могли повлиять на функцию левого и правого желудочков: дисфункция левого желудочка может возникнуть из-за увеличения постнагрузки после коррекции тяжелой гипотензии; динамическая обструкция могла быть вызвана инотропными или вазопрессорными агентами; и, наконец, правожелудочковая дисфункция может быть связана с искусственной вентиляцией легких. Кроме того, сепсис-индуцированная кардиопатия может нарушать функцию левого и правого желудочков. Эхокардиографию можно использовать для оценки объемного статуса [34].При сепсисе различные фенотипы можно идентифицировать по комбинации эхокардиографических показателей [47]. Это позволяет точно настроить терапевтические вмешательства (Fig. 2). Важно измерять ударный объем (УО), поскольку инотропные препараты показаны только в том случае, если нарушение сердечной функции связано с низким или неадекватным УО и нарушением тканевой перфузии. Кроме того, особое внимание должно быть сосредоточено на правом желудочке, так как дисфункция правого желудочка может потребовать специального лечения.

Расширенный мониторинг
Для надежного измерения СВ можно использовать различные инструменты, но выбор метода должен основываться на представляющих интерес переменных, в зависимости от состояния пациента (Fig. 3). У пациентов без сопутствующих заболеваний и с минимальной органной дисфункцией можно использовать некалиброванные устройства с внутренней калибровкой доя для мониторинга CВ [48], но более сложные пациенты (с сопутствующими заболеваниями, сопутствующей органной дисфункцией) выиграют от использования транспульмональной термодилюции [49] или, в конечном итоге, катетеризации легочную артерии в сочетании с эхокардиографией по мере необходимости [50].
Транспульмональная термодилюция (TPTD) сочетает в себе калиброванное измерение CВ, пошаговое и точное определение УО, что полезно для прогнозирования реакции на инфузию, показателей статической объемной преднагрузки, индексов сердечной функции, внесосудистой жидкости в легких (EVLW) и сосудистой проницаемости. Эта всесторонняя гемодинамическая оценка особенно полезна при управлении инфузионной терапией, поскольку она обеспечивает динамическую оценку реакции на инфузионную терапию в сочетании с оценкой рисков, связанных с объемом введенной жидкости [34].
Благодаря комбинированным измерениям СВ, легочного давления и SvO2 использование катетера легочной артерии (КЛА), обеспечивает оценку адекватности СВ и его детерминант. Несмотря на то, что КЛА не позволяет предсказать реакцию на введение жидкости, он отлично подходит для оценки эффективности и толерантности к инфузионной терапии во время введения жидкости. Одновременное измерение ЦВД и давления в легочной артерии делает КЛА идеальным для мониторинга пациентов с дисфункцией правых отделов сердца. В конце концов, выбор метода мониторинга должен основываться на состоянии пациента, местном опыте и доступности, а также ожидаемом ответе на терапию. Предлагается поэтапный подход к пациенту с септическим шоком (Fig.3).

Стабилизация и деэскалация: подходы и показатели толерантности
Во время стабилизации и деэскалации подходы и цели должны быть адаптированы. На этих этапах цель гемодинамической поддержки меняется с оптимизации перфузии тканей на предотвращение осложнений при обеспечении поддержки органов. Он включает эвакуацию скопившейся жидкости и отказ от вазоактивной поддержки при сохранении тканевой перфузии.
В фазе стабилизации распространены сердечная дисфункция и объемная перегрузка и часто продолжают использовать уже внедренные методы поддержки гемодинамики. УЗИ легких и оценка печеночного, почечного и портального венозного кровотока с помощью ультразвука могут выявить признаки венозного застоя, которые могут указывать на необходимость удаления жидкости и/или введения инотропов [34]. Комбинация визуализации легких/вен с эхокардиографией особенно полезна для дифференциальной диагностики между перегрузкой объемом и сердечной дисфункцией.
Частым осложнением является развитие дисфункции правого желудочка, которая может развиться у 20% пациентов с острым респираторным дистресс-синдромом (ОРДС), подвергающихся легочно-защитным стратегиям вентиляции [51]. Соответственно, повторение эхокардиографии через регулярные промежутки времени может быть полезным, особенно при повышении ЦВД. Ведение таких пациентов является сложной задачей и может включать изменение параметров вентиляции и введение инотропных препаратов. Выбор терапии для данного пациента основан на комплексном анализе последствий дисфункции правого желудочка на тканевую перфузию, венозный застой и постоянную потребность в определенных параметрах вентиляции.
На этапе деэскалации ситуация еще более сложная. Пациенты обычно находятся под минимальным наблюдением, а показатели толерантности четко не определены. Должны ли мы по-прежнему ориентироваться на те же значения, что и на этапе оптимизации? Вероятно, нет, но остается неизвестным, как определить допустимый уровень нарушений. Логично не возвращаться к шоку (поэтому термин «де-раенимация» неуместен). Тем не менее, некоторая степень снижения артериального давления и кровотока может быть допустима при условии сохранения оксигенации тканей и их функции. Очевидно, что деэскалация должна быть остановлена до возникновения гипоперфузии. Например, было показано, что чрезмерное удаление жидкости с помощью ультрафильтрации связано с повышенной смертностью [52]. Мониторинг может помочь ограничить или предотвратить неблагоприятные события во время деэскалации. Тестирование реакции на преднагрузку перед удалением жидкости может выявить пациентов, для которых это будет вредно [53]. Кроме того, измерение кожной перфузии во время удаления жидкости может выявить пациентов, у которых она будет плохо переноситься, до появления гипоперфузии и новой гиперлактатемии [54]. Для деэскалации вазопрессоров оценка динамической эластичности артерий, отношение изменений пульсового давления к визменениям УО может помочь в прогнозировании гипотензии и выявлении кандидатов на снижение дозы вазопрессоров [55].
Персонализация жизнеспасающей терапии
Персонализированные подходы к инфузии, использованию вазопрессоров и инотропов должны быть адаптирована к оценке состояния тканевой перфузии и сердечно-сосудистой системы с учетом ответа на терапию.
Индивидуальное подходы к инфузионной терапии
При септическом шоке крайне важно обеспечить инфузионную терапию. Во время фазы спасения жидкости можно вводить в больших количествах, так как польза в значительной степени перевешивает риски. При оптимизации ситуация сложнее. Доля пациентов, отвечающих на введение жидкости, прогрессивно снижается [13], а вероятность нежелательных явлений возрастает. Стратегии по формуле, будь то «сухие» или «влажные», явно не подходят [56], и предпочтение отдается персонализированным стратегиям.
Персонализированный способ введения жидкости включает несколько этапов. Во-первых, должно быть четкое указание на необходимость введения жидкости, т. е. нарушение перфузии, которое, как ожидается, будет корректироваться в ответ на введение жидкости. Во-вторых, следует прогнозировать реакцию пациента на жидкости. Прогноз реакции на инфузию лучше достигается с помощью динамических тестов [57], а не статических измерений преднагрузки. В-третьих, следует тщательно оценить реакцию на введение жидкости [34]. Во время фазы стабилизации следует свести к минимуму введение жидкости [58]. В фазе деэскалации необходимо обеспечить безопасный вывод жидкости с помощью диуретиков или ультрафильтрации при минимальном мониторинге. Во-первых, идентификация пациента, потенциально получающего пользу от удаления жидкости, имеет решающее значение. Пациенты с признаками легочного или системного венозного застоя являются идеальными кандидатами [34]. Измерение внесосудистой жидкости легких (EVLW) с помощью TPTD или ультразвука) может использоваться для начала удаления жидкости и оценки его эффективности. Как и для многих других переменных, цель EVLW должна быть индивидуальной. Как указывалось выше, кажется логичным не отменять инфузионную терапию у пациентов, реагирующих на инфузию, поскольку это может поставить под угрозу состояние их гемодинамики [53]. Во-вторых, следует проверить показатели непереносимости удаления жидкости. Действительно, индивидуальную скорость наполнения капилляров трудно оценить в клинической практике, а высокая скорость удаления жидкости недопустима.
В то время как рекомендации предлагают сбалансированные кристаллоиды [3], при выборе между альбумином и кристаллоидами, а также между 0,9% физиологическим раствором и сбалансированными кристаллоидами (на основе уровней хлоридов) следует учитывать индивидуальные факторы, такие как уровни хлоридов и альбумина, а также наличие отека. Во время стабилизации и деэскалации следует также попытаться свести к минимуму «нереанимационные жидкости» и натриевую нагрузку [58].
Персонализированное использование вазопрессоров
Вазопрессоры начинают, титруют и отменяют в соответствии с СрАД, показателями перфузии и функции органов, как указано выше. Они различаются по своей фармакологии, влиянию на капиллярную перфузию, функции органов и профилям безопасности (Table3).

Норэпинефрин рекомендуется в качестве вазопрессора первой линии при септическом шоке на основании данных большого количества РКИ, сравнивающих норадреналин и дофамин, и нескольких мета-анализов [59, 60]. Кроме того, дефицит норадреналина и его замена другими вазопрессорами были связаны с повышенной смертностью [61]. В целом эти данные подтверждают, что норадреналин является вазопрессором первой линии. Вазопрессин изучался в качестве основного агента и в комбинации с норадреналином [62–64]. В то время как не было никакой разницы в смертности, вазопрессин был связан с меньшим количеством аритмий, меньшей потребностью в заместительной почечной терапии (ЗПТ), но более высокой частотой ишемии внутренних органов и пальцев [65]. Об аналогичном эффекте сообщалось при применении терлипрессина [66, 67], но прямого сравнения с вазопрессином не проводилось. Применение селепрессина у пациентов с септическим шоком без оценки кровотока не продемонстрировало положительного влияния на исход [68], несмотря на благоприятный профиль в доклинических исследованиях [69].
Ангиотензин II появился как новый вазопрессор в лечении вазодилататорного шока. Он эффективен для повышении артериального давления и обладает катехоламин-сберегающим эффектом по сравнению с плацебо [70]. Апостериорный анализ пациентов, получавших ЗПТ, показал улучшение выживаемости и более раннее прекращение ЗПТ у пациентов, которые были рандомизированы в группу ангиотензина II [71]. Остаются важные вопросы, касающиеся оптимального выбора вазопрессоров, роли комбинированной терапии и наиболее эффективного и безопасного метода эскалации в различных когортах пациентов [72]. Необходимы дополнительные методы информирования клиницистов о наиболее эффективных вазопрессорах в конкретных условиях и о том, как избежать вреда от их использования.
Несколько генетических полиморфизмов связаны с различными ответами на вазопрессоры [73, 74], но эта таргетная стратегия еще не подходит для применения у постели больного. В качестве альтернативы можно использовать биомаркеры, чтобы указать, какая группа пациентов может получить больше пользы от конкретного агента. Плазменный ангиопоэтин 1 (Ang1) и ангиопоэтин 2 (Ang2), медиаторы сосудистой проницаемости, стали потенциальными биомаркерами для управления терапией вазопрессином. Ренин сыворотки и соотношение ангиотензин I/II отражают активность ангиотензин-превращающих ферментов [75] и являются многообещающими биомаркерами для выявления пациентов с вазодилататорным шоком, для которых лечение ангиотензином II может быть полезным [76]. Необходимо подтверждение в проспективных исследованиях.
Наконец, недостаточно данных об оптимальной терапевтической стратегии при шоке, требующем высоких доз вазопрессоров. Рецепторы α1, как и любые другие вазопрессорные рецепторы, могут быть насыщенными и/или гипореактивными при рефрактерном шоке. Имеет смысл рассмотреть альтернативные вазопрессоры, действующие на разные рецепторы (производные вазопрессина или ангиотензин II), а не использовать агент того же класса. Точно так же показания к дополнительной терапии различаются, и необходимы прогностические критерии для определения показаний и оценки эффективности. Выявить пациентов, отвечающих на кортикостероиды, может помочь анализ выбранных цитокинов [77] или идентификация специфических транскриптомных эндотипов [78]. В связи с отсутствием своевременного выполнения этих методик использование гидрокортизован в настоящее время рассматривается у больных, получающих высокие дозы вазопрессорных средств.
Персонализированное использование инотропных средств
Нет данных, подтверждающих систематическое использование инотропных средств. Неразборчивое применение левосимендана у таких больных оказалось безуспешным [79]. Даже попытка идентифицировать пациентов с повреждением миокарда на основе биомаркеров оказалась бесполезной [80]. Это неудивительно, поскольку последствия сепсис-ассоциированной депрессии миокарда весьма вариабельны. У некоторых пациентов наблюдается высокий СВ [47] или даже динамическая обструкция выводного тракта левого желудочка [81], несмотря на значительное нарушение сердечной функции или высокие уровни биомаркеров.
Их не следует лечить инотропными средствами. С другой стороны, у некоторых пациентов низкий СВ связан с дисфункцией левого или правого желудочка [47], и им могут помочь инотропные препараты. Соответственно, как указано выше, инотропы могут быть показаны только пациентам с признаками тканевой гипоперфузии, связанной с низким СВ, вызванным нарушением функции сердца. Побочные эффекты (тахикардия, аритмии) и специфические риски у некоторых категорий пациентов (гипертрофические кардиомиопатии, ишемия миокарда) должны быть тщательно изучены, а риск/польза вмешательства оценены.
Обсуждение типа агента является более сложным. Доказано, что ни один из агентов не превосходит другой у пациентов с шоком. Следует отметить, что большинство исследований, сравнивающих инотропные препараты, проводились у пациентов с сердечной недостаточностью и исключали пациентов с кардиогенным шоком. Соответственно, метаанализы этих исследований следует рассматривать с осторожностью.
Основываясь на фармакологических свойствах, мы предлагаем следующий поэтапный подход: сначала протестируйте ограниченную дозу добутамина (от 2,5 до 5 мкг/кг/мин) и оцените эффективность и переносимость. В случаях тяжелого нарушения сократимости миокарда можно рассмотреть более высокие дозы (до 20 мкг/кг/мин). Во-вторых, замените или добавьте эноксимон или милринон и оцените эффективность и переносимость (остерегайтесь риска гипотензии). В-третьих, замените или добавьте левосимендан в случаях тяжелых нарушений. На каждом этапе следует оценивать эффективность (улучшение сердечной функции и сердечного выброса, устранение тканевой гипоперфузии) и переносимость (например, отсутствие тахикардии, аритмий и т. д.). Для каждого из агентов следует вводить наименьшую дозу, связанную с желаемым эффектом. Как только ситуация улучшится, следует попытаться отменить инотропы.
Выводы
Несмотря на то, что для ведения септического шока применяются некоторые общие правила, следует учитывать индивидуальный подход для гемодинамического мониторинга и поддержки. Важно отметить, что мониторинг и поддержка должны быть адаптированы к четырем стадиям шока, а воздействие вмешательств должно постоянно оцениваться.
References:
1. Cecconi M ,DeBacker D, Antonelli M, Beale RJ, Bakker J, Hofer C, Jaeschke R, Mebazaa A, Pinsky MR,T ebou lJL,et al. Consensus on circulatory shock and hemodynamic monitoring. Task force of the European Society of Intensive Care Medicine. IntensiveCareMed.2014;40(12):1795–815.
2. Vincent JL, DeBacker D. Circulatory shock.NEnglJMed.2013;369(18):1726–34.
3. Evans L, Rhodes A, Alhazzani W, Antonelli M, Coopersmith CM , French C, Machado FR, McIntyre L, Ostermann M, Prescott HC, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021.IntensiveCareMed.2021;47(11):1181–247.
4. Vincent JL, Singer M, Einav S, Moreno R, Wendon J, Teboul JL, Bakker J, Hernandez G, AnnaneD, deManAME, et al. Equilibrating SSC guidelines with individualized care. CritCare.2021;25(1):397.
5. Coopersmith CM, DeBackerD, DeutschmanCS, FerrerR, MachadoFR, MartinGS, Martin‑Loeches I,Nunnally ME, Antonelli M, et al. Surviving sepsis campaign: research priorities for sepsis and septic shock.IntensiveCareMed.2018;44(9):1400–26.
6. Ait‑Oufella H, BigeN, BoellePY, PichereauC, Alves M,Bertinchamp R, BaudelJL, GalboisA, MauryE, GuidetB. Capillary refill time exploration during septic shock. Intensive Care Med. 2014. https://doi.org/10.1007/s00134‑014‑3326‑4.
7. Ait‑Oufella H, LemoinneS, BoellePY, Galbois A,Baudel JL,Lemant J, JoffreJ, MargetisD, GuidetB, MauryE, et al. Mottlings core predicts survivalin septic shock.IntensiveCareMed.2011;37(5):801–7.
8. DeBackerD, Vieillard‑Baron A.Clinical examination: a trigger but not a substitute for hemodynamic evaluation. Intensive Care Med. 2019;45(2):269–71.
9. Zieleskiewicz L, Lopez A, Hraiech S, Baumstarck K, Pastene B, Di BisceglieM, Coiffard B, Duclos G, Boussuges A, Bobbia X, et al. Bedside POCUS during ward emergencies is associated with improved diagnosis and outcome: an observational, prospective, controlled study. Crit Care.2021;25(1):34.
10. Teboul JL, Saugel B, Cecconi M, De Backer D, Hofer CK, Monnet X, PerelA, PinskyMR, ReuterDA, RhodesA, e tal. Less invasive hemodynamic Monitoring in critically ill patients.IntensiveCareMed.2016;42(9):1350–9.
11. BréchotN, HajageD, KimmounA, DemiselleJ, AgerstrandC, MonteroS, SchmidtM, LuytCE, LebretonG, HékimianG,et al.Venoarterial extraсorporeal membrane oxygenation to rescue sepsis‑induced cardiogenic shock: a retrospective, multicentre, international cohort study. Lancet.2020;396(10250):545–52.
12. Cecconi M, HernandezG, DunserM, AntonelliM, BakerT, BakkerJ, DuranteauJ , Einav S, GroeneveldABJ, HarrisT,et al. Fluid administration for acute circulatory dysfunction using basic monitoring: narrative review and expert panel recommendations from an ESICM task force. IntensiveCareMed.2019;45(1):21–32.
13. Hernandez G, Ospina‑Tascon GA, Damiani LP, Estenssoro E, DubinA,Hurtado J,Friedman G,Castro R,Alegria L,Teboul JL, et al. Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate level son 28‑daymortality among patients with septic shock:theANDROMEDA‑SHOCKrandomizedclinicaltrial.JAMA.2019;321(7):654–64.
14. Ait‑HamouZ,TeboulJL,AnguelN,MonnetX.How to detect appositive response to a fluid bolus when cardiac output is not measured?AnnIntensiveCare.2019;9(1):138.
15. Jacquet‑LagrezeM,BouhamriN,PortranP,SchweizerR,BaudinF,LilotM,FornierW,FellahiJL.Capillaryrefilltimevariationinducedbypassivelegraising predicts capillary refill time response to volume expansion. CritCare.2019;23(1):281.
16. Vincent JL, Nielsen ND, Shapiro NI, Gerbasi ME, Grossman A, Doroff R, ZengF,YoungPJ,RussellJA.Meanarterialpressureandmortalityinpatientswithdistributiveshock:aretrospectiveanalysisoftheMIMIC‑IIIdatabase.AnnIntensiveCare.2018;8:107.
17. Persichini R, Silva S, Teboul JL, Jozwiak M, Chemla D, Richard C, Monnet X. Effects of norepinephrine on mean systemic pressure and venous return in human septic shock.CritCareMed.2012;40(12):3146–53.
18. Ospina‑Tascon GA, Hernandez G,Alvarez I, Calderon‑TapiaLE, Manzano‑Nunez R, Sanchez‑Ortiz AI, Quinones E, Ruiz‑Yucuma JE, Aldana JL, TeboulJL, et al. Effects of very early start of norepinephrine in patients with septic shock: a propensity score‑basedanalysis.CritCare.2020;24(1):52.
19. Ospina‑Tascón GA, Teboul JL, Hernandez G, Alvarez I, Sánchez‑Ortiz AI,Calderón‑TapiaLE,Manzano‑NunezR,QuiñonesE,Madriñan‑NaviaHJ,RuizJE,etal.Diastolic shock index and clinical outcomes in patients with septic shock.AnnIntensiveCare.2020;10(1):41.
20. DeBacker D,Creteur J, NoordallyO, SmailN, Gulbis B,Vincent JL. Does hepato‑splanchnic VO2/DO2 dependency exist in critically ill septicpatients?AmJRespirCritCareMed.1998;157:1219–25.
21. De Backer D, Creteur J, Preiser JC, Dubois MJ, Vincent JL. Microvascular blood flow is altered in patients with sepsis.AmJRespirCritCareMed.2002;166:98–104.
22. Hernandez G, Luengo C, Bruhn A, Kattan E, Friedman G, Ospina‑Tascon GA, Fuentealba A, CastroR, RegueiraT, RomeroC, et al. When to stop septic shock resuscitation: clues from a dynamic perfusion monitoring.AnnIntensiveCare.2014;4:30.
23. BakkerJ, DeBackerD, HernandezG. Lactate‑guided resuscitation saves lives: weare not sure.IntensiveCareMed.2016;42(3):472–4.
24. Brunauer A, KoköferA, BataarO, Gradwohl‑MatisI, Dankl D,Bakker J,Dünser MW. Changes in peripheral perfusion relate to visceral organ perfusion in early septic shock: a pilot study.JCritCare.2016;35:105–9.
25. BoermaEC, KuiperMA, KingmaWP, EgbersPH, GerritsenRT, InceC. Disparity between skin perfusion and sublingual microcirculatory alteration sinse vere sepsis and septic shock: a prospective observational study.IntensiveCareMed.2008;34:1294–8.
26. Brabrand M, Hosbond S, Folkestad L. Capillary refill time: a study of inter‑observer reliability among nurses and nurse assistants. Eur J Emerg Med.2011;18(1):46–9.
27. ZampieriFG,DamianiLP,BakkerJ,Ospina‑TasconGA,CastroR,CavalcantiAB, Hernandez G. Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate levels on 28‑day mortality among patients with septic shock:a Bayesian Re analysis of the ANDROMEDA‑SHOCKTrial.AmJRespirCritCareMed.2019.https://doi.org/10.1164/rccm.201905‑0968OC.
28. LiuX, LuoD, ZhangJ,DuL. Distribution and relative expression of vasoactive receptors on arteries. SciRep. 2020;10(1):15383.
29. Asfar P, Meziani F, Hamel JF, Grelon F, Megarbane B, Anguel N, Mira JP, DequinPF, GergaudS, WeissN,etal. High versus low blood‑pressure target in patients with septic shock.NEnglJMed.2014;370(17):1583–93.
30. LamontagneF,Richards‑BelleA,ThomasK,HarrisonDA,SadiqueMZ,Grieve RD, Camsooksai J, Darnell R, Gordon AC, Henry D, et al. Effect of reduced exposure to vasopressors on 90‑day mortality in older critically Ill patients with vasodilatory hypotension: a randomized clinical trial.JAMA.2020;323(10):938–49.
31. DeruddreS, CheissonG, MazoitJX,VicautE,BenhamouD,DuranteauJ. Renal arterial resistance in septic shock: effects of in creasing mean arterial pressure with norepinephrine on the renal resistive index assessedwithDopplerultrasonography.IntensiveCareMed.2007;33(9):1557–62.
32. Gershengorn HB, StelfoxHT, NivenDJ, WunschH.Association of premorbid blood pressure with vasopressor infusion duration in patients with shock. Am J Respir Crit Care Med. 2020;202(1):91–9.
33. DeBackerD,VincentJL. Should we measure the central venous pressure to guide fluid management? Ten answers to 10 questions. Crit Care.2018;22(1):43.
34. DeBackerD,AissaouiN,CecconiM,ChewMS,DenaultA,HajjarL,Her‑nandezG,MessinaA,MyatraSN,OstermannM,etal.Howcanassessinghemodynamicshelptoassessvolumestatus?IntensiveCareMed.2022.https://doi.org/10.1007/s00134‑022‑06808‑9.
35. DeBackerD,CreteurJ,Dubois MJ,SakrY,VincentJL. Microvascular alterations in patients with acute severe heart failure and cardiogenic shock.AmHeartJ.2004;147:91–9.
36. DeBacker D, VincentJL. Early goal‑directed therapy: do we have a definitive answer?IntensiveCareMed.2016;42(6):1048–50.
37. Ospina‑Tascon GA, Umana M, Bermudez WF, Bautista‑Rincon DF, Valencia JD, Madrinan HJ, HernandezьG, Bruhn A, Arango‑Davila C, DeBacker D. Can venous‑to‑arterial carbon dioxide differences reflect microcirculatory alterations in patients with septic shock?IntensiveCareMed.2016;42(2):211–21.
38. ValleeF, ValletB ,MatheO, ParraguetteJ, MariA, SilvaS, SamiiK, FourcadeO, GenestalM .Central venous‑to‑arterial carbondioxide difference: an additional target for goal‑directed therapy in septic shock? Intensive CareMed.2008;34(12):2218–25.
39. Mesquida J, Saludes P, Gruartmoner G, Espinal C, Torrents E, Baigorri F, ArtigasA. Central venous‑to‑arterial carbondioxide difference combined with arterial‑to‑venous oxygen content difference is associated with lactate volution in the hemodynamic resuscitation process in early septic shock.CritCare.2015;19:126.
40. Ospina‑TasconGA, Bautista‑Rincon DF, Umana M, Tafur JD, Gutierrez A,GarciaAF,BermudezW,GranadosM,Arango‑DavilaC,HernandezG.Persistently high venous‑to‑arterial carbondioxide differences during early resuscitation are associated with poor outcomes in septic shock.CritCare.2013;17(6):R294.
41. DuW, LiuDW, WangXT, LongY, ChaiWZ, ZhouX, RuiX. Combining central venous‑to‑arterial partial pressure of carbon dioxide difference and central venous oxygen saturation to guide resuscitation in septic shock. JCritCare.2013;28(6):1110–5.
42. Ospina‑TasconGA, UmanaM, BermudezW, Bautista‑RinconDF, Hern‑dez G, Bruhn A, Granados M, Salazar B, Arango‑Davila C, De Backer D. Combination of arterial lactate levels and venous‑arterial CO to arterial‑venous O content difference ratio as markers of resuscitation in patientswithsepticshock.IntensiveCareMed.2015;41:796–805.
43. MonnetX,JulienF,Ait‑HamouN,LequoyM,GossetC,JozwiakM,Persi‑chiniR,AnguelN,RichardC,TeboulJL. Lactate and venoarterial carbon dioxide difference/arterial‑venous oxygen difference ratio, but not central venous oxygen saturation, predict increase in oxygen consumption in fluid responders.CritCareMed.2013;41(6):1412–20.
44. Jansen TC, van Bommel J, Schoonderbeek J, Sleeswijk Visser SJ, van der Klooster JM, LimaAP, Willemsen SP, Bakker J. Early lactate‑guided therapy in ICU patients: a multicenter, open‑label, randomized, controlled trial.AmJRespirCritCareMed.2010;182(6):752–61.
45. RimachiR, Bruzzi DC, Orellano‑Jimenez C, Cotton F,Vincent J, De Backer D. Lactate/pyruvate ratio a samarker of tissue hypoxia in circulatory and septic shock. Anaesth Intensive Care.2012;40(3):427–32.
46. KattanE, Hernández G,ьOspina‑Tascón G, Valenzuela ED, Bakker J, CastroR.A lactate‑targeted resuscitation strategy may be associated with higher mortality in patients with septic shock and normal capillary refill time: a posthoc analysis of the ANDROMEDA‑SHOCK study. Ann Intensive Care.2020;10(1):114.
47. GeriG,VignonP,AubryA,FedouAL,CharronC,SilvaS,RepesséX,Vieillard‑Baron A. Cardiovascular clusters in septic shock combining clinical and echocardiographic parameters: a posthoc analysis. Intensive Care Med.2019;45(5):657–67.
48. Kouz K, Scheeren TWL, de Backer D, Saugel B. Pulse wave analysis to estimate cardiac output. Anesthesiology.2021;134:119–26.
49. Monnet X, Teboul JL. Transpulmonary thermodilution: advantages and limits. Crit Care.2017;21(1):147.
50. Teboul JL, Sauge lB, Cecconi M, De BD, Hofer CK, Monnet X, Perel A, Pinsky MR, Reuter DA, Rhodes A, et al. Less invasive hemodynamic monitoring in critically ill patients. Intensive Care Med. 2016. https://doi.org/10.1007/s00134‑016‑4375‑7.
51. Boissier F, Katsahian S, Razazi K, Thille AW, Roche‑CampoF, Leon R, Vivier E, Brochard L, Vieillard‑Baron A, Brun‑Buisson C, et al. Prevalence and prognosis of corpulmonale during protective ventilation for acute Respiratory distress syndrome. IntensiveCareMed.2013;39(10):1725–33.
52. Murugan R, Kerti SJ, Chang CH, Gallagher M, Clermont G, Palevsky PM, Kellum JA, Bellomo R. Association of net ultrafiltration rate with mortality among critically Ill adults with acute kidney injury receiving continuous veno venous hemodiafiltration: a secondary analysis of the randomized evaluation of normal vs augmented level (RENAL) of renal replacementtherapytrial.JAMANetwOpen.2019;2(6):e195418.
53. Monnet X, Cipriani F, Camous L, Sentenac P, Dres M, Krastinova E, Anguel N, Richard C, Teboul JL. The passive legraising test to guide fluid removal in critically ill patients.AnnIntensiveCare.2016;6(1):46.
54. MongkolpunW, BakosP, VincentJL, CreteurJ. Monitoring skin blood flow to rapidly identify alterations in tissue perfusion during fluid removal using continuous veno‑venous hemofiltration in patients with circulatory shock. AnnIntensive Care.2021;11(1):59.
55. Guinot PG, Bernard E, Levrard M, Dupont H, Lorne E. Dynamic arterial elastance predicts mean arterial pressure decrease associated with decreasing norepinephrine dosage in septic shock. Crit Care.2015;19:14.
56. Meyhoff TS, Hjortrup PB, Wetterslev J, Sivapalan P, Laake JH, Cronhjort M, Jakob SM, Cecconi M, Nalos M, Ostermann M ,et al .Restriction Of intravenous fluid in ICU patients with septic shock. N Eng l J Med.2022;386(26):2459–70.
57. Monnet X, Shi R, Teboul JL. Prediction of fluid responsiveness.What’s new? Annal Intensive Care.2022;12(1):46.
58. VanRegenmorte lN, Verbrugghe W, Roelant E, VandenWyngaert T, Jorens PG. Maintenance fluid therapy and fluid creep impose more significant fluid, sodium, and chloride burdens than resuscitation fluids in critically ill patients: a retrospective study in a tertiary mixed ICU popula‑tion.IntensiveCareMed.2018;44(4):409–17.
59. De Backer D, Biston P, Devriendt J, Madl C, Chochrad D, Aldecoa C, Brasseur A, Defrance P, Gottignies P, VincentJL. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med.2010;362(9):779–89.
60. DeBacker D, Aldecoa C, Njimi H, Vincent J‑L. Dopamine versus norepinephrine in the treatment of septic shock: a meta analysis.CritCareMed.2012;40:725–30.
61. Vail E, Gershengorn HB, Hua M, Walkey AJ, Rubenfeld G, Wunsch H. Association between US norepinephrine short age and mortality among patients with septic shock. JAMA.2017;317(14):1433–42.
62. Russell JA, Walley KR, Singer J, Gordon AC, Hebert PC, Cooper DJ, Holmes CL, Mehta S, Granton JT, Storms MM, et al. Vasopressin versus norepinephrine infusion in patients with septic shock.NEnglJMed.2008;358(9):877–87.
63. Gordon AC, Mason AJ, Thirunavukkarasu N, Perkins GD, Cecconi M, Cepkova M, Pogson DG, Aya HD, Anjum A, Frazier GJ, et al. Effect of early vasopressin vs norepinephrine on kidney failure in patients with septic shock: The VANISHrandomizedclinicaltrial.JAMA.2016;316(5):509–18.
64. Hajjar LA, Vincent JL, Barbosa Gomes Galas FR, Rhodes A, Landoni G, Osawa EA, Melo RR, Sundin MR, Grande SM, Gaiotto FA, et al. Vasopressin versus norepinephrine in patients with vasoplegic shock after cardiac surgery: the VANCS randomized controlled trial. Anesthesiology.2017;126(1):85–93.
65. Nagendran M, Russell JA, Walley KR, Brett SJ, Perkins GD, HajjarL, MasonAJ, AshbyD, Gordon AC. Vasopressin in septic shock: an individual patient datameta‑analysis of randomized controlled trials.IntensiveCareMed.2019;45(6):844–55.
66. Liu ZM, Chen J, Kou Q, Lin Q, Huang X, Tang Z, Kang Y, Li K, Zhou L, Song Q, et al. Terlipressin versus norepinephrine as infusion in patients with septic shock: a multicentre, randomised, double‑blinded trial. Intensive Care Med.2018;44(11):1816–25.
67. Zhu Y, Huang H, Xi X, Du B. Terlipressin for septic shock patients: a meta‑analysis of randomized controlled study. J Intensive Care.2019;7:16.
68. Laterre PF, Berry SM, Blemings A, Carlsen JE, Francois B, Graves T, Jacobsen K, Lewis RJ, Opal SM, PernerA, et al. Effect of selepressin vs placebo on ventilator‑ and vasopressor‑free days in patients with septic shock: the SEPSIS‑ACT randomized clinical trial.JAMA.2019.https://doi.org/10.1001/jama.2019.14607.
69. Rehberg S , Ertmer C, Vincent JL, Morelli A, Schneider M, Lange M, VanAken H, Traber DL, Westphal M. Role of selective V1a receptor agonism in ovine septic shock. Crit Care Med.2011;39(1):119–25.
70. Khanna A, English SW , Wang XS, Ham K, Tumlin J, Szerlip H, Busse LW, Altawee lL, Albertson TE, Mackey C, et al. Angiotensin II for the treatment of vasodilatory shock. N Engl J Med.2017;377(5):419–30.
71. Tumlin JA, Murugan R, Deane AM, Ostermann M, Busse LW, Ham KR, Kashani K, Szerlip HM, Prowle JR, Bihorac A, et al. Outcomes in patients with vasodilatory shock and renal replacement therapy treated with intravenous angiotensin II. Crit Care Med.2018;46(6):949–57.
72. Chawla LS, Ostermann M, ForniL, Tidmarsh GF. Broad spectrum vasopressors: a new approach to the initial management of septic shock? CritCare.2019;23(1):124.
73. Nakada TA, Russell JA, Boyd JH, Aguirre‑Hernandez R, Thain KR, Thair SA, Nakada E, McConechy M, Walley KR. beta2‑Adrenergic receptor gene polymorphism is associated with mortality in septic shock. Am J RespirCritCareMed.2010;181(2):143–9.
74. Anantasit N, Boyd JH, Walley KR, Russell JA. Serious adverse events associated with vasopressin and norepinephrine infusion in septic shock. CritCareMed.2014;42(8):1812–20.
75. Chawla LS, Chen S, Bellomo R, Tidmarsh GF. Angiotensin converting enzyme defects in shock: implications for future therapy. Crit Care.2018;22(1):274.
76. Bellomo R, Forni LG, Busse LW, McCurdy MT, Ham KR, Boldt DW, Hästbacka J, Khanna AK, Albertson TE, Tumlin J, et al. Renin and survival inpatients given angiotensin II for catecholamine‑resistant vasodilatoryshock.Aclinicaltrial.AmJRespirCritCareMed.2020;202(9):1253–61.
77. Bentzer P, Fjell C, Walley KR, Boyd J, Russell JA. Plasma cytokine levels predict response to corticosteroids in septic shock. Intensive Care Med.2016;42(12):1970–9.
78. Antcliffe DB, Burnham KL, Al‑Beidh F, Santhakumaran S, Brett SJ, Hinds CJ, Ashby D, Knight JC, Gordon AC. Transcriptomic signatures in sepsis and a differential response to steroids. From the VANISH randomized trial. Am JRespirCritCareMed.2019;199(8):980–6.
79. GordonAC,PerkinsGD,SingerM,McAuleyDF,OrmeRM,Santhaku‑maranS,MasonAJ,CrossM,Al‑BeidhF,Best‑LaneJ,etal.Levosimendanfor the prevention of acute organ dysfunction in sepsis. N Engl J Med.2016;375:1638–48.
80. Antcliffe DB, Santhakumaran S, Orme RML, Ward JK, Al‑Beidh F, O’Dea K, Perkins GD, Singer M, McAuley DF, Mason A J, et al. Levosimendan in septic shock in patients with biochemical evidence of cardiac dysfunction: a subgroup analysis of the LeoPARDS randomized trial. Intensive Care Med.2019;45(10):1392–400.
81. Chauvet JL, El‑Dash S, Delastre O, Bouffandeau B, Jusserand D, Michot JB, Bauer F , Maizel J, Slama M. Early dynamic left intraventricular obstructtion is associated with hypovolemia and high mortality in septic shock patients. Crit Care.2015;19:262.
Источник фотоиллюстрации - www.freepik.com
[DETAIL_PICTURE] =>
[~DETAIL_PICTURE] =>
[DATE_ACTIVE_FROM] => 23.01.2023
[~DATE_ACTIVE_FROM] => 23.01.2023
[ACTIVE_FROM_X] => 2023-01-23 00:00:00
[~ACTIVE_FROM_X] => 2023-01-23 00:00:00
[ACTIVE_FROM] => 23.01.2023
[~ACTIVE_FROM] => 23.01.2023
[SHOW_COUNTER] => 1288
[~SHOW_COUNTER] => 1288
[ID] => 8327
[~ID] => 8327
[IBLOCK_ID] => 2
[~IBLOCK_ID] => 2
[IBLOCK_SECTION_ID] =>
[~IBLOCK_SECTION_ID] =>
[DETAIL_TEXT_TYPE] => html
[~DETAIL_TEXT_TYPE] => html
[PREVIEW_TEXT] =>
[~PREVIEW_TEXT] =>
[PREVIEW_TEXT_TYPE] => html
[~PREVIEW_TEXT_TYPE] => html
[TIMESTAMP_X] => 11.11.2024 15:24:54
[~TIMESTAMP_X] => 11.11.2024 15:24:54
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/prizyv-k-personalizatsii-korrektsii-gemodinamiki-pri-septicheskom-shoke/
[~DETAIL_PAGE_URL] => /library/articles/prizyv-k-personalizatsii-korrektsii-gemodinamiki-pri-septicheskom-shoke/
[LANG_DIR] => /
[~LANG_DIR] => /
[CODE] => prizyv-k-personalizatsii-korrektsii-gemodinamiki-pri-septicheskom-shoke
[~CODE] => prizyv-k-personalizatsii-korrektsii-gemodinamiki-pri-septicheskom-shoke
[EXTERNAL_ID] => 8327
[~EXTERNAL_ID] => 8327
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[IBLOCK_CODE] => articles
[~IBLOCK_CODE] => articles
[IBLOCK_EXTERNAL_ID] => content-articles
[~IBLOCK_EXTERNAL_ID] => content-articles
[LID] => s1
[~LID] => s1
[NAV_RESULT] =>
[NAV_CACHED_DATA] =>
[DISPLAY_ACTIVE_FROM] => 23 января 2023
[IPROPERTY_VALUES] => Array
(
)
[FIELDS] => Array
(
[NAME] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[PREVIEW_PICTURE] => Array
(
[ID] => 5108
[TIMESTAMP_X] => 11.11.2024 15:24:54
[MODULE_ID] => iblock
[HEIGHT] => 720
[WIDTH] => 900
[FILE_SIZE] => 136557
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk
[FILE_NAME] => red-blood-cells.jpg
[ORIGINAL_NAME] => red-blood-cells.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 04509b0cec63a27995ce0eca5eaa2ef0
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk/red-blood-cells.jpg
[UNSAFE_SRC] => /upload/iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk/red-blood-cells.jpg
[SAFE_SRC] => /upload/iblock/e1f/hhu3z2jq0c0hozozwhc62slnybjr81wk/red-blood-cells.jpg
[ALT] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[TITLE] => Призыв к персонализации коррекции гемодинамики при септическом шоке
)
[DETAIL_TEXT] => DeBacker D. et al. A plea for personalization of the hemodynamic management of septic shock Призыв кперсонализации коррекции гемодинамики при септическом шоке Critical Care (2022)26:372doi.org/10.1186/s13054-022-04255-y
Абстракт
Несмотря на то, что руководства содержат отличные рекомендации специалистов по ведению пациентов с септическим шоком, они оставляют место для персонализации в зависимости от состояния пациентов. Мониторинг гемодинамики зависит от фазы развития: спасение, оптимизация, стабилизация и деэскалация. На начальном этапе во время спасательной фазы мониторинг для определения этиологии и тяжести шока должен включать измерение артериального давления и лактата вместе с клиническим обследованием, особенно определением пятнистости кожи и времени наполнения капилляров. Низкое диастолическое давление может мотивировать к использованию вазопрессоров.
На этой стадии эхокардиография может быть полезна для выявления выраженной сердечной дисфункции. На этапе оптимизации следует проводить эхокардиографический мониторинг, с оценкой тканевой перфузии путем измерения центральной или смешанной венозной сатурации кислородом, измерения лактата и вено-артериального градиента углекислого газа. Транспульмональная термомодуляция и катетеризация легочной артерии должны рассматриваться у наиболее тяжелых пациентов. Инфузионная терапия также зависит от фаз шока. В то время как предусмотрена либеральная стратегия инфузионной терапии во время фазы реанимации, следует оценить реакцию на инфузионную терапию во время фазы оптимизации. Во время стабилизации инфузия жидкости должна быть сведена к минимуму. На этапе деэскалации может быть обеспечено безопасное удаление жидкости за счет сохранения тканевой перфузии. В качестве вазопрессорной терапии первой линии рекомендуется норэпинефрин, в то время как у некоторых пациентов предпочтение отдается вазопрессину.
Остаются важные вопросы относительно оптимального выбора вазопрессоров, комбинированной терапии и наиболее эффективной и безопасной эскалации. Ренин сыворотки и соотношение ангиотензина I/II могут выявить пациентов, которые получают наибольшую пользу от ангиотензина II.Оптимальная терапевтическая стратегия при шоке, требующем высоких доз вазопрессоров, ограничена. Во всех случаях вазопрессорная терапия должна быть индивидуализирована и основана на клинической оценке и измерениях кровотока, чтобы избежать чрезмерной вазоконстрикции. Инотропы следует рассматривать у пациентов со сниженной сердечной сократимостью, связанной с нарушением тканевой перфузии. Исходя из фармакологических свойств, мы предлагаем в качестве первого теста ограниченную дозу добутамина, добавить эноксимон или милринон во вторую линию и заменить или добавить левосимендан, если нет эффекта. Что касается дополнительной терапии, то хотя гидрокортизон в настоящее время рекомендуется пациентам, получающим высокие дозы вазопрессоров, в будущем пациентов, отвечающих на кортикостероиды, можно будет идентифицировать с помощью анализа выбранных цитокинов или специфических транскриптомныхэ ндотипов.
Несмотря на то, что для лечения шока применяются некоторые общие правила, следует учитывать индивидуальный подход для мониторинга и поддержки гемодинамики.
Ключевые слова: артериальное давление, сердечный выброс, тканевая перфузия, жидкости, вазопрессорные средства, инотропные средства.
Шок — опасное для жизни состояние, характеризующееся неадекватной доставкой кислорода к тканям [1]. Септический шок является одной из наиболее частых причин шока в отделении интенсивной терапии(ОИТ) [2]. Рекомендации Surviving Sepsis Campaign (SSC) представляют собой отличное руководство по ведению пациентов с сепсисом [3], но по ряду причин здесь есть место для персонализации [4]. Во-первых, хотя эти рекомендации подтверждаются доказательствами, они основаны главным образом на рандомизированных контролируемых исследованиях (РКИ), в которых изучалась реакция больших групп пациентов на вмешательство. Эти исследования, как правило, негативны, т. е. не выявляют различий в смертности. Важно осознавать, что индивидуальные особенности пациента могут влиять на реакцию или переносимость данного вмешательства. Во-вторых, многие области реанимации до сих пор являются предметом дискуссий и остаются пробелы в исследованиях [5].
Следовательно, руководящие принципы часто не содержат сильных и точных рекомендаций в конкретных областях. В-третьих, существуют разные этапы лечения шока [2], каждый из которых требует своего подхода. Таким образом, может быть оправдано индивидуализация терапевтических подходов в зависимости от состояния пациента. В этом экспертном заключении мы обсуждаем различные варианты персонализации гемодинамического мониторинга и ведения пациентов на разных стадиях септического шока. Общий принцип персонализированного лечения шока заключается в измерении, интерпретации, применении терапии, оценке ее эффектов и реагировании, в отличие от применения стандартных мер.
Персонализация мониторинга
Персонализация гемодинамического мониторинга подразумевает рассмотрение различных фаз SOSD(спасение, оптимизация, стабилизация и деэскалация). На каждом этапе доступные методы и цели различаются (Fig.1and Table1).


Время распознавания шока: фаза спасения
Во время распознавания и идентификации шока первоначальное лечение направлено на обеспечение уровня перфузии тканей, совместимого с жизнью. В этой фазе гемодинамический мониторинг часто является очень простым, а терапевтические возможности ограничены жидкостями и вазопрессорами.
Какую информацию можно получить из базового гемодинамического мониторинга при проведении реанимационных мероприятий?
Клиническая оценка имеет решающее значение для выявления гипоперфузии тканей. Измерение артериального давления, пятнистость кожи и время наполнения капилляров (CRT) информируют о ходе реанимации. Изменения показателей CRT и пятнистости могут использоваться для базового мониторинга, поскольку они коррелируют с исходом [6, 7] и быстро реагируют на проводимую терапию. Однако они плохо коррелируют с сердечным выбросом (СВ), не позволяют идентифицировать источник тканевой гипоперфузии и определить необходимые мероприятия [8].
Если есть кардиологический анамнез или если пациент не реагирует на жидкости, для уточнения оценки гемодинамики полезно быстрое эхокардиографическое исследование [1]. Эхокардиография у постели больного является единственным методом, который позволяет быстро оценить СВ наряду с идентификацией причины низкого СВ. В недавнем РКИ использование эхокардиографии группой быстрого реагирования было связано с улучшением выживаемости [9].
Во время фазы спасения инотропы могут быть показаны, когда соответствующий кардиогенный компонент (связанный с септической кардиомиопатией или сопутствующими заболеваниями пациента) способствует шоковому процессу [1, 10]. Это можно определить только с помощью эхокардиографии, и инотропы следует рассматривать, когда СВ низкий из-за серьезного нарушения сократительной способности сердца. При тяжелом кардиогенном шоке эхокардиография может также быстро выявить пациентов, не отвечающих на первоначальную терапию, и для которых может быть рассмотрена механическая поддержка сердца [11].
Базовый клинический мониторинг играет роль в выявлении пациентов, которые могут реагировать на жидкости, и оценке их реакции [12]. В частности, время наполнения капилляров можно использовать для оценки перфузионной реакции тканей и определения необходимости дальнейшего введения жидкостей [13].
Динамические тесты, такие как реакция пульсового давления или время наполнения капилляров на пассивное поднятие ноги, могут использоваться для прогнозирования реакции на жидкость [14, 15]. Однако эти тесты трудно проводить на этапе спасения, когда одновременно применяется множество вмешательств. Прогнозирование реакции на инфузию и оценка эффектов инфузии должны быть предприняты как можно скорее, особенно у пациентов с плохой функцией сердца.
Измерение уровня лактата в крови полезно для выявления нарушений тканевой перфузии. Кроме того, когда установлен центральный венозный катетер, центральная венозная сатурация O2 (ScvO2) и градиент парциального давления углекислого газа (pCO2) между центральной венозной и артериальной кровью (Pv-aCO2) могут быть полезны для оценки эффективности проводимых мероприятий.
Как определить пациентов, у которых немедленная вазопрессорная терапия приносит пользу, не дожидаясь результатов инфузионной терапии?
В то время как некоторые пациенты могут реагировать только на инфузионную терапию, другим требуется вазопрессорная поддержка. Руководящие принципы SSC рекомендуют поддерживать среднее артериальное давление (САД) ≥ 65 мм рт. ст., но не указывают сроки или не дают указаний по приоритетности жидкости по сравнению с вазопрессорами. Некоторым пациентам с тяжелой гипотензией может потребоваться раннее начало введения вазопрессоров, т. е. не дожидаясь эффекта жидкости, для ускорения восстановления артериального давления. Действительно, отсрочка коррекции гипотензии связана с плохим исходом [16]. Более того, норадреналин может способствовать увеличению преднагрузки на сердце [17], что может снизить потребность в жидкости. В обсервационном исследовании с использованием сопоставления склонности раннее начало норадреналина было связано с менее положительным балансом жидкости и более низкой 28-дневной смертностью [18].
Решение о раннем назначении вазопрессоров наряду с инфузионной терапией кажется логичным в случаях выраженной гипотензии, хотя точного порога САД дать нельзя. Диастолическое давление (ДАД) также может влиять на принятие решения.. При сепсисе низкое ДАД часто отражает выраженную вазодилатацию и связано с повышенной смертностью [19]. Поэтому представляется логичным начинать назначение вазопрессоров при очень низком ДАД, например, < 45 мм рт.ст. У пациентов с тахикардией высокие значения индекса диастолического шока (ИДШ): соотношение между ДАД и ЧСС, связаны с более высоким риском смерти у больных с септическим шоком [19]. Следует ли использовать ИДШ> 2 для начала введения вазопрессоров, остается неизвестным.
Фаза оптимизации: инструменты и цели
На этом этапе целью реанимационных мероприятий является оптимизация тканевой перфузии за счет оптимизации перфузионного давления и СВ. В идеале это также должно включать оптимизацию регионарного распределения кровотока и микроциркуляторной перфузии. Хотя изменения в распределении регионарного кровотока [20] и микрососудистой перфузии [21] часты при шоке и могут быть отделены от системного кровообращения, в клинической практике их нелегко контролировать.
Наиболее частые показатели тканевой гипоперфузии, используемые у постели больного, включают артериальное давление, диурез, кожную перфузию, время наполнения капилляров, ScvO2, Pv-aCO2 и концентрацию лактата. Важно отметить, что даже если на исходном уровне существует некоторая корреляция между различными индексами, некоторые переменные нормализуются быстрее, чем другие [22]. ScvO2, по-видимому, нормализуется быстрее всего, за ним следуют CRT и Pv-aCO2, которые обычно нормализуются в течение 6–8 часов, в то время как лактат и подъязычная микроциркуляция могут нормализоваться более, чем через 24 часа [13]. Кажется логичным объединить несколько переменных и прекратить реанимационные мероприятия, когда большинство из них нормализуются, не прибегая к нормализации переменных, таких как концентрации лактата [23]. При обнаружении тканевой гипоперфузии следует оценить реакцию на инфузионную терапию, а в некоторых случаях следует рассмотреть возможность применения передовых гемодинамических методов для оценки сердечно-сосудистой функции.
Время наполнения капилляров (CRT)
CRT является маркером гипоперфузии кожи, динамически реагирующей на вазоактивные вещества. В какой степени время наполнения капилляров отражает центральную перфузию остается неизвестной. В то время как одно исследование пришло к выводу, что CRTотражает центральное кровообращение [24], другие исследования предполагают некоторую диссоциацию [22, 25]. Измерения CRT показывают значительную изменчивость между наблюдателями [26], но это можно свести к минимуму с помощью стандартизации метода [13]. По сравнению с реанимацией, нацеленной на лактат при раннем септическом шоке реанимация под контролем CRT, как правило, лучше [13, 27]. Среди факторов, способствующих этим различиям, более частые оценки кровообращения в группе CRT. Достижение значения CRT< 3 с является ценным ориентиром эффективных мероприятий, в то время как медленное снижение уровня лактата само по себе может привести к дополнительному введению жидкости, даже если перфузия тканей могла нормализоваться на момент оценки.
Среднее артериальное давление
Определение целевого системного артериального давления, необходимого для достижения адекватной тканевой перфузии, остается сложной задачей. В принципе, органный кровоток зависит от перфузионного давления (т. е. разницы между давлением притока и оттока) и сопротивления. Однако сохранения системного артериального давления недостаточно для обеспечения адекватности микроциркуляторного русла. Важно отметить, что перфузионное давление различается в зависимости от сосудистого русла (Table2), и эти уровни также могут повреждаться при сепсисе.

Большинство органов обладают эндогенной способностью сохранять микроциркуляцию в определенном диапазоне перфузионных давлений. Например, сердце и мозг могут поддерживать постоянный кровоток, несмотря на большие изменения перфузионного давления. В случае, если давление падает ниже органоспецифической зоны ауторегуляции, органный кровоток становится зависимым от давления притока, поэтому основное внимание уделяется устранению гипотонии в фазу спасения.
Неоднородность пациентов, различная органоспецифическая регуляция микроциркуляции, вариабельная плотность рецепторов и влияние фармакологических взаимодействий затрудняют единый подход к лечению септического шока [28]. Руководство SSC рекомендует начальное целевое среднее артериальное давление 65 мм рт. ст. [3], но не содержит рекомендаций для более поздних стадий. Данные наблюдений показывают, что органная дисфункция иногда может начаться уже при падении СрАД ниже 75–80 мм рт. ст. [16], но для достижения более высоких целевых значений СрАД часто требуются более высокие дозы вазопрессоров, которые могут быть связаны с большим количеством побочных эффектов.
Исследования, рандомизирующие пациентов с сепсисом в группы с целевым значением СрАД ~ 65 мм рт. ст. или даже меньше по сравнению с от~ 75 и до ~ 85 мм рт. ст., не показали различий в смертности [29, 30]. Положительное влияние более высокого среднего артериального давления на функцию почек у ранее страдающих артериальной гипертензией пациентов можно наблюдать [29], но оно не является систематическим [30]. Различия в влиянии более высоких целевых значений СрАД на функцию почек можно частично объяснить высокой вариабельностью реакции почечного кровотока на увеличение СрАД [31].
Несостоятельность подхода «один размер подходит всем» была также продемонстрирована у пациентов с артериальной гипотензией. Анализ 3542 пациентов в критическом состоянии с шоком показал, что пациенты с естественно низким АД (систолическое АД < 100 мм рт. ст.) лечились дольше и с более высокими дозами норадреналина и имели более длительное пребывание в ОИТ и более высокую смертность [32]. Соответственно, в то время как начальное целевое среднее артериальное давление 65 мм рт. ст. представляется разумным подходом для многих пациентов, идеальное среднее артериальное давление должно быть индивидуальным. Подтверждение эффективности выбранного индивидуального целевого СрАД заключается в оценке изменений показателей перфузии, таких как диурез, уровень сознания и кожная перфузия. Если наблюдаются положительные эффекты, можно использовать это новое целевое значение СрАД, если оно неэффективно или непереносимо, то следует установить начальное значение СрАД.
Центральное венозное давление (ЦВД)
ЦВД представляет собой сложную переменную, отражающую преднагрузку и функцию правого желудочка [33]. Несмотря на то, что его способность точно предсказывать реакцию на инфузионную терапию сомнительна, оно по-прежнему предоставляет важную информацию о волемическом статусе и резерве правого желудочка и должно измеряться при шоке [34]. ЦВД может быть важным ранним индикатором недостаточности правого желудочка. Устойчивое повышение ЦВД > 12 мм рт. ст. связано с нарушением функции почек и кишечника, даже когда перфузионное давление в органах остается постоянным, что свидетельствует о том, что венозный застой играет роль в органной дисфункции. Для ЦВД не должно быть целевого значения, так как идеальное ЦВД — это самое низкое ЦВД, связанное с гемодинамической стабильностью.
Сердечный выброс (СВ)
CВ является ключевым фактором перфузии тканей. Однако не существует фиксированного значения оптимального СВ при шоке, и СВ следует оптимизировать в соответствии с индексами тканевой перфузии, перечисленными ниже, и функцией органов. Важно отметить, что микрососудистые изменения могут сохраняться даже после коррекции низкого СВ, что ухудшает тканевую перфузию [21, 35]. При гиперкинетическом шоке стойкие нарушения перфузии связаны с изменениями регионарной перфузии и/или изменениями микроваскулярной перфузии. Эти микрососудистые изменения могут быть нечувствительны к увеличению СВ, поэтому следует использовать другие стратегии для улучшения микроциркуляции. Соответственно, CВ следует рассматривать как средство улучшения тканевой перфузии, а не как мишень.
Смешанное венозное (SvO2) и центральное венозное (ScvO2) насыщение кислородом
Хотя ScvO2 или SvO2 даже не упоминаются в новых рекомендациях SSC [3], они являются очень важными физиологическими переменными, которые необходимо понимать и измерять. Они отражают баланс между фактическим потреблением кислорода и доставкой кислорода тканям. Соответственно, низкий уровень ScvO2указывает на нарушение или неадекватную доставку O2, что объясняется неадекватным СО, если гемоглобин и сатурация артериальной крови O2 находятся в пределах нормы. Ожидается, что при сепсисе SvO2 и ScvO2 будут нормальными или повышенными даже при нарушении тканевой перфузии [21]. В то время как определение конкретных значений SvO2 или ScvO2 у всех пациентов было затруднено [36], обнаружение низкого SvO2 или ScvO2 может выявить пациентов, которым должны помочь дальнейшие реанимационные мероприятия. Это может заключаться в увеличении СО с помощью инфузионной терапии или инотропного агента, а иногда и гемоглобина путем переливания крови у пациентов с анемией. У пациентов с высоким ScvO2 следует тщательно проверять другие показатели нарушения перфузии.
Разница венозной и артериальной концентрации углекислого газа (Pv-aCO2)
Pv-aCO2 зависит от общего производства углекислого газа (CO2), CO и перфузии микрососудов, а также от сложной взаимосвязи между парциальным давлением CO2 и содержанием CO2 в крови. Согласно модифицированному уравнению Фика, Pv-aCO2 находится в обратной зависимости от CO (криволинейная зависимость). При стабильных условиях как потребления кислорода (VO2), так и продукции CO2 (VCO2) Pv-aCO2 прогрессивно увеличивается в ответ на снижение CO из-за застояCO2 в микрососудах. Прогрессирующее увеличение Pv-aCO2 отражает снижение микроциркуляторной перфузии на ранних стадиях септического шока [37]. Таким образом, высокое значение Pv-aCO2 может идентифицировать пациентов с сепсисом, которые неадекватно реанимированы [38]. ЗначениеPv-aCO2 [39] и изменение Pv-aCO2 в ответ на терапию связаны с исходом [40]. Измерение Pv-aCO2 может быть особенно полезным у пациентов с нормальными значениями лактата или ScvO2 для выявления пациентов с риском неблагоприятного исхода, несмотря на очевидную адекватную реанимацию [40–42]. Тем не менее, трудно рекомендовать конкретное целевое значение Pv-aCO2 на основе наблюдательных испытаний. Отношение Pv-aCO2 к артериовенозной разнице содержания кислорода является оценкой дыхательного коэффициента и, как таковая, может быть прямым показателем анаэробного метаболизма с более быстрыми изменениями, чем у лактата [42, 43].
Концентрация лактата в крови
Уровни лактата имеют сильное прогностическое значение и поэтому могут использоваться для скрининга. Оценка серийных уровней лактата полезна, так как они обычно снижаются у пациентов, которым становится лучше, и часто остаются повышенными или даже увеличиваются, когда септический шок плохо контролируется. Стратегии реанимации, направленные на снижение уровня лактата, были связаны со снижением госпитальной летальности [44]. Таким образом, кажется логичным направить реанимационную стратегию на снижение уровня лактата [3].Однако повышенный уровень лактата также может быть вызван другими причинами, помимо тканевой гипоксии (например, воспалением, снижением клиренса лактата и т. д.). У больных с шоком гиперлактатемия в первые несколько часов после поступления преимущественно гипоксического происхождения, тогда как не гипоксические причины преобладают на более поздних стадиях [45]. Снижение уровня лактата также требует времени, поэтому изолированная гиперлактатемия может сохраняться после нормализации других показателей тканевой гипоперфузии [22]. Следовательно, погоня за нормализацией лактата может быть нецелесообразной [23]. У пациентов с нормализованным временем наполнения капилляров реанимация под контролем лактата была связана с повышенной смертностью [46]. Соответственно, мониторинг уровня лактата в крови играет роль в оценке эффективности реанимационных процедур в сочетании с другими показателями тканевой гипоперфузии.
Эхокардиография
Следует рассмотреть вопрос о проведении эхокардиографии, поскольку первоначальные реанимационные процедуры могли повлиять на функцию левого и правого желудочков: дисфункция левого желудочка может возникнуть из-за увеличения постнагрузки после коррекции тяжелой гипотензии; динамическая обструкция могла быть вызвана инотропными или вазопрессорными агентами; и, наконец, правожелудочковая дисфункция может быть связана с искусственной вентиляцией легких. Кроме того, сепсис-индуцированная кардиопатия может нарушать функцию левого и правого желудочков. Эхокардиографию можно использовать для оценки объемного статуса [34].При сепсисе различные фенотипы можно идентифицировать по комбинации эхокардиографических показателей [47]. Это позволяет точно настроить терапевтические вмешательства (Fig. 2). Важно измерять ударный объем (УО), поскольку инотропные препараты показаны только в том случае, если нарушение сердечной функции связано с низким или неадекватным УО и нарушением тканевой перфузии. Кроме того, особое внимание должно быть сосредоточено на правом желудочке, так как дисфункция правого желудочка может потребовать специального лечения.

Расширенный мониторинг
Для надежного измерения СВ можно использовать различные инструменты, но выбор метода должен основываться на представляющих интерес переменных, в зависимости от состояния пациента (Fig. 3). У пациентов без сопутствующих заболеваний и с минимальной органной дисфункцией можно использовать некалиброванные устройства с внутренней калибровкой доя для мониторинга CВ [48], но более сложные пациенты (с сопутствующими заболеваниями, сопутствующей органной дисфункцией) выиграют от использования транспульмональной термодилюции [49] или, в конечном итоге, катетеризации легочную артерии в сочетании с эхокардиографией по мере необходимости [50].
Транспульмональная термодилюция (TPTD) сочетает в себе калиброванное измерение CВ, пошаговое и точное определение УО, что полезно для прогнозирования реакции на инфузию, показателей статической объемной преднагрузки, индексов сердечной функции, внесосудистой жидкости в легких (EVLW) и сосудистой проницаемости. Эта всесторонняя гемодинамическая оценка особенно полезна при управлении инфузионной терапией, поскольку она обеспечивает динамическую оценку реакции на инфузионную терапию в сочетании с оценкой рисков, связанных с объемом введенной жидкости [34].
Благодаря комбинированным измерениям СВ, легочного давления и SvO2 использование катетера легочной артерии (КЛА), обеспечивает оценку адекватности СВ и его детерминант. Несмотря на то, что КЛА не позволяет предсказать реакцию на введение жидкости, он отлично подходит для оценки эффективности и толерантности к инфузионной терапии во время введения жидкости. Одновременное измерение ЦВД и давления в легочной артерии делает КЛА идеальным для мониторинга пациентов с дисфункцией правых отделов сердца. В конце концов, выбор метода мониторинга должен основываться на состоянии пациента, местном опыте и доступности, а также ожидаемом ответе на терапию. Предлагается поэтапный подход к пациенту с септическим шоком (Fig.3).

Стабилизация и деэскалация: подходы и показатели толерантности
Во время стабилизации и деэскалации подходы и цели должны быть адаптированы. На этих этапах цель гемодинамической поддержки меняется с оптимизации перфузии тканей на предотвращение осложнений при обеспечении поддержки органов. Он включает эвакуацию скопившейся жидкости и отказ от вазоактивной поддержки при сохранении тканевой перфузии.
В фазе стабилизации распространены сердечная дисфункция и объемная перегрузка и часто продолжают использовать уже внедренные методы поддержки гемодинамики. УЗИ легких и оценка печеночного, почечного и портального венозного кровотока с помощью ультразвука могут выявить признаки венозного застоя, которые могут указывать на необходимость удаления жидкости и/или введения инотропов [34]. Комбинация визуализации легких/вен с эхокардиографией особенно полезна для дифференциальной диагностики между перегрузкой объемом и сердечной дисфункцией.
Частым осложнением является развитие дисфункции правого желудочка, которая может развиться у 20% пациентов с острым респираторным дистресс-синдромом (ОРДС), подвергающихся легочно-защитным стратегиям вентиляции [51]. Соответственно, повторение эхокардиографии через регулярные промежутки времени может быть полезным, особенно при повышении ЦВД. Ведение таких пациентов является сложной задачей и может включать изменение параметров вентиляции и введение инотропных препаратов. Выбор терапии для данного пациента основан на комплексном анализе последствий дисфункции правого желудочка на тканевую перфузию, венозный застой и постоянную потребность в определенных параметрах вентиляции.
На этапе деэскалации ситуация еще более сложная. Пациенты обычно находятся под минимальным наблюдением, а показатели толерантности четко не определены. Должны ли мы по-прежнему ориентироваться на те же значения, что и на этапе оптимизации? Вероятно, нет, но остается неизвестным, как определить допустимый уровень нарушений. Логично не возвращаться к шоку (поэтому термин «де-раенимация» неуместен). Тем не менее, некоторая степень снижения артериального давления и кровотока может быть допустима при условии сохранения оксигенации тканей и их функции. Очевидно, что деэскалация должна быть остановлена до возникновения гипоперфузии. Например, было показано, что чрезмерное удаление жидкости с помощью ультрафильтрации связано с повышенной смертностью [52]. Мониторинг может помочь ограничить или предотвратить неблагоприятные события во время деэскалации. Тестирование реакции на преднагрузку перед удалением жидкости может выявить пациентов, для которых это будет вредно [53]. Кроме того, измерение кожной перфузии во время удаления жидкости может выявить пациентов, у которых она будет плохо переноситься, до появления гипоперфузии и новой гиперлактатемии [54]. Для деэскалации вазопрессоров оценка динамической эластичности артерий, отношение изменений пульсового давления к визменениям УО может помочь в прогнозировании гипотензии и выявлении кандидатов на снижение дозы вазопрессоров [55].
Персонализация жизнеспасающей терапии
Персонализированные подходы к инфузии, использованию вазопрессоров и инотропов должны быть адаптирована к оценке состояния тканевой перфузии и сердечно-сосудистой системы с учетом ответа на терапию.
Индивидуальное подходы к инфузионной терапии
При септическом шоке крайне важно обеспечить инфузионную терапию. Во время фазы спасения жидкости можно вводить в больших количествах, так как польза в значительной степени перевешивает риски. При оптимизации ситуация сложнее. Доля пациентов, отвечающих на введение жидкости, прогрессивно снижается [13], а вероятность нежелательных явлений возрастает. Стратегии по формуле, будь то «сухие» или «влажные», явно не подходят [56], и предпочтение отдается персонализированным стратегиям.
Персонализированный способ введения жидкости включает несколько этапов. Во-первых, должно быть четкое указание на необходимость введения жидкости, т. е. нарушение перфузии, которое, как ожидается, будет корректироваться в ответ на введение жидкости. Во-вторых, следует прогнозировать реакцию пациента на жидкости. Прогноз реакции на инфузию лучше достигается с помощью динамических тестов [57], а не статических измерений преднагрузки. В-третьих, следует тщательно оценить реакцию на введение жидкости [34]. Во время фазы стабилизации следует свести к минимуму введение жидкости [58]. В фазе деэскалации необходимо обеспечить безопасный вывод жидкости с помощью диуретиков или ультрафильтрации при минимальном мониторинге. Во-первых, идентификация пациента, потенциально получающего пользу от удаления жидкости, имеет решающее значение. Пациенты с признаками легочного или системного венозного застоя являются идеальными кандидатами [34]. Измерение внесосудистой жидкости легких (EVLW) с помощью TPTD или ультразвука) может использоваться для начала удаления жидкости и оценки его эффективности. Как и для многих других переменных, цель EVLW должна быть индивидуальной. Как указывалось выше, кажется логичным не отменять инфузионную терапию у пациентов, реагирующих на инфузию, поскольку это может поставить под угрозу состояние их гемодинамики [53]. Во-вторых, следует проверить показатели непереносимости удаления жидкости. Действительно, индивидуальную скорость наполнения капилляров трудно оценить в клинической практике, а высокая скорость удаления жидкости недопустима.
В то время как рекомендации предлагают сбалансированные кристаллоиды [3], при выборе между альбумином и кристаллоидами, а также между 0,9% физиологическим раствором и сбалансированными кристаллоидами (на основе уровней хлоридов) следует учитывать индивидуальные факторы, такие как уровни хлоридов и альбумина, а также наличие отека. Во время стабилизации и деэскалации следует также попытаться свести к минимуму «нереанимационные жидкости» и натриевую нагрузку [58].
Персонализированное использование вазопрессоров
Вазопрессоры начинают, титруют и отменяют в соответствии с СрАД, показателями перфузии и функции органов, как указано выше. Они различаются по своей фармакологии, влиянию на капиллярную перфузию, функции органов и профилям безопасности (Table3).

Норэпинефрин рекомендуется в качестве вазопрессора первой линии при септическом шоке на основании данных большого количества РКИ, сравнивающих норадреналин и дофамин, и нескольких мета-анализов [59, 60]. Кроме того, дефицит норадреналина и его замена другими вазопрессорами были связаны с повышенной смертностью [61]. В целом эти данные подтверждают, что норадреналин является вазопрессором первой линии. Вазопрессин изучался в качестве основного агента и в комбинации с норадреналином [62–64]. В то время как не было никакой разницы в смертности, вазопрессин был связан с меньшим количеством аритмий, меньшей потребностью в заместительной почечной терапии (ЗПТ), но более высокой частотой ишемии внутренних органов и пальцев [65]. Об аналогичном эффекте сообщалось при применении терлипрессина [66, 67], но прямого сравнения с вазопрессином не проводилось. Применение селепрессина у пациентов с септическим шоком без оценки кровотока не продемонстрировало положительного влияния на исход [68], несмотря на благоприятный профиль в доклинических исследованиях [69].
Ангиотензин II появился как новый вазопрессор в лечении вазодилататорного шока. Он эффективен для повышении артериального давления и обладает катехоламин-сберегающим эффектом по сравнению с плацебо [70]. Апостериорный анализ пациентов, получавших ЗПТ, показал улучшение выживаемости и более раннее прекращение ЗПТ у пациентов, которые были рандомизированы в группу ангиотензина II [71]. Остаются важные вопросы, касающиеся оптимального выбора вазопрессоров, роли комбинированной терапии и наиболее эффективного и безопасного метода эскалации в различных когортах пациентов [72]. Необходимы дополнительные методы информирования клиницистов о наиболее эффективных вазопрессорах в конкретных условиях и о том, как избежать вреда от их использования.
Несколько генетических полиморфизмов связаны с различными ответами на вазопрессоры [73, 74], но эта таргетная стратегия еще не подходит для применения у постели больного. В качестве альтернативы можно использовать биомаркеры, чтобы указать, какая группа пациентов может получить больше пользы от конкретного агента. Плазменный ангиопоэтин 1 (Ang1) и ангиопоэтин 2 (Ang2), медиаторы сосудистой проницаемости, стали потенциальными биомаркерами для управления терапией вазопрессином. Ренин сыворотки и соотношение ангиотензин I/II отражают активность ангиотензин-превращающих ферментов [75] и являются многообещающими биомаркерами для выявления пациентов с вазодилататорным шоком, для которых лечение ангиотензином II может быть полезным [76]. Необходимо подтверждение в проспективных исследованиях.
Наконец, недостаточно данных об оптимальной терапевтической стратегии при шоке, требующем высоких доз вазопрессоров. Рецепторы α1, как и любые другие вазопрессорные рецепторы, могут быть насыщенными и/или гипореактивными при рефрактерном шоке. Имеет смысл рассмотреть альтернативные вазопрессоры, действующие на разные рецепторы (производные вазопрессина или ангиотензин II), а не использовать агент того же класса. Точно так же показания к дополнительной терапии различаются, и необходимы прогностические критерии для определения показаний и оценки эффективности. Выявить пациентов, отвечающих на кортикостероиды, может помочь анализ выбранных цитокинов [77] или идентификация специфических транскриптомных эндотипов [78]. В связи с отсутствием своевременного выполнения этих методик использование гидрокортизован в настоящее время рассматривается у больных, получающих высокие дозы вазопрессорных средств.
Персонализированное использование инотропных средств
Нет данных, подтверждающих систематическое использование инотропных средств. Неразборчивое применение левосимендана у таких больных оказалось безуспешным [79]. Даже попытка идентифицировать пациентов с повреждением миокарда на основе биомаркеров оказалась бесполезной [80]. Это неудивительно, поскольку последствия сепсис-ассоциированной депрессии миокарда весьма вариабельны. У некоторых пациентов наблюдается высокий СВ [47] или даже динамическая обструкция выводного тракта левого желудочка [81], несмотря на значительное нарушение сердечной функции или высокие уровни биомаркеров.
Их не следует лечить инотропными средствами. С другой стороны, у некоторых пациентов низкий СВ связан с дисфункцией левого или правого желудочка [47], и им могут помочь инотропные препараты. Соответственно, как указано выше, инотропы могут быть показаны только пациентам с признаками тканевой гипоперфузии, связанной с низким СВ, вызванным нарушением функции сердца. Побочные эффекты (тахикардия, аритмии) и специфические риски у некоторых категорий пациентов (гипертрофические кардиомиопатии, ишемия миокарда) должны быть тщательно изучены, а риск/польза вмешательства оценены.
Обсуждение типа агента является более сложным. Доказано, что ни один из агентов не превосходит другой у пациентов с шоком. Следует отметить, что большинство исследований, сравнивающих инотропные препараты, проводились у пациентов с сердечной недостаточностью и исключали пациентов с кардиогенным шоком. Соответственно, метаанализы этих исследований следует рассматривать с осторожностью.
Основываясь на фармакологических свойствах, мы предлагаем следующий поэтапный подход: сначала протестируйте ограниченную дозу добутамина (от 2,5 до 5 мкг/кг/мин) и оцените эффективность и переносимость. В случаях тяжелого нарушения сократимости миокарда можно рассмотреть более высокие дозы (до 20 мкг/кг/мин). Во-вторых, замените или добавьте эноксимон или милринон и оцените эффективность и переносимость (остерегайтесь риска гипотензии). В-третьих, замените или добавьте левосимендан в случаях тяжелых нарушений. На каждом этапе следует оценивать эффективность (улучшение сердечной функции и сердечного выброса, устранение тканевой гипоперфузии) и переносимость (например, отсутствие тахикардии, аритмий и т. д.). Для каждого из агентов следует вводить наименьшую дозу, связанную с желаемым эффектом. Как только ситуация улучшится, следует попытаться отменить инотропы.
Выводы
Несмотря на то, что для ведения септического шока применяются некоторые общие правила, следует учитывать индивидуальный подход для гемодинамического мониторинга и поддержки. Важно отметить, что мониторинг и поддержка должны быть адаптированы к четырем стадиям шока, а воздействие вмешательств должно постоянно оцениваться.
References:
1. Cecconi M ,DeBacker D, Antonelli M, Beale RJ, Bakker J, Hofer C, Jaeschke R, Mebazaa A, Pinsky MR,T ebou lJL,et al. Consensus on circulatory shock and hemodynamic monitoring. Task force of the European Society of Intensive Care Medicine. IntensiveCareMed.2014;40(12):1795–815.
2. Vincent JL, DeBacker D. Circulatory shock.NEnglJMed.2013;369(18):1726–34.
3. Evans L, Rhodes A, Alhazzani W, Antonelli M, Coopersmith CM , French C, Machado FR, McIntyre L, Ostermann M, Prescott HC, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021.IntensiveCareMed.2021;47(11):1181–247.
4. Vincent JL, Singer M, Einav S, Moreno R, Wendon J, Teboul JL, Bakker J, Hernandez G, AnnaneD, deManAME, et al. Equilibrating SSC guidelines with individualized care. CritCare.2021;25(1):397.
5. Coopersmith CM, DeBackerD, DeutschmanCS, FerrerR, MachadoFR, MartinGS, Martin‑Loeches I,Nunnally ME, Antonelli M, et al. Surviving sepsis campaign: research priorities for sepsis and septic shock.IntensiveCareMed.2018;44(9):1400–26.
6. Ait‑Oufella H, BigeN, BoellePY, PichereauC, Alves M,Bertinchamp R, BaudelJL, GalboisA, MauryE, GuidetB. Capillary refill time exploration during septic shock. Intensive Care Med. 2014. https://doi.org/10.1007/s00134‑014‑3326‑4.
7. Ait‑Oufella H, LemoinneS, BoellePY, Galbois A,Baudel JL,Lemant J, JoffreJ, MargetisD, GuidetB, MauryE, et al. Mottlings core predicts survivalin septic shock.IntensiveCareMed.2011;37(5):801–7.
8. DeBackerD, Vieillard‑Baron A.Clinical examination: a trigger but not a substitute for hemodynamic evaluation. Intensive Care Med. 2019;45(2):269–71.
9. Zieleskiewicz L, Lopez A, Hraiech S, Baumstarck K, Pastene B, Di BisceglieM, Coiffard B, Duclos G, Boussuges A, Bobbia X, et al. Bedside POCUS during ward emergencies is associated with improved diagnosis and outcome: an observational, prospective, controlled study. Crit Care.2021;25(1):34.
10. Teboul JL, Saugel B, Cecconi M, De Backer D, Hofer CK, Monnet X, PerelA, PinskyMR, ReuterDA, RhodesA, e tal. Less invasive hemodynamic Monitoring in critically ill patients.IntensiveCareMed.2016;42(9):1350–9.
11. BréchotN, HajageD, KimmounA, DemiselleJ, AgerstrandC, MonteroS, SchmidtM, LuytCE, LebretonG, HékimianG,et al.Venoarterial extraсorporeal membrane oxygenation to rescue sepsis‑induced cardiogenic shock: a retrospective, multicentre, international cohort study. Lancet.2020;396(10250):545–52.
12. Cecconi M, HernandezG, DunserM, AntonelliM, BakerT, BakkerJ, DuranteauJ , Einav S, GroeneveldABJ, HarrisT,et al. Fluid administration for acute circulatory dysfunction using basic monitoring: narrative review and expert panel recommendations from an ESICM task force. IntensiveCareMed.2019;45(1):21–32.
13. Hernandez G, Ospina‑Tascon GA, Damiani LP, Estenssoro E, DubinA,Hurtado J,Friedman G,Castro R,Alegria L,Teboul JL, et al. Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate level son 28‑daymortality among patients with septic shock:theANDROMEDA‑SHOCKrandomizedclinicaltrial.JAMA.2019;321(7):654–64.
14. Ait‑HamouZ,TeboulJL,AnguelN,MonnetX.How to detect appositive response to a fluid bolus when cardiac output is not measured?AnnIntensiveCare.2019;9(1):138.
15. Jacquet‑LagrezeM,BouhamriN,PortranP,SchweizerR,BaudinF,LilotM,FornierW,FellahiJL.Capillaryrefilltimevariationinducedbypassivelegraising predicts capillary refill time response to volume expansion. CritCare.2019;23(1):281.
16. Vincent JL, Nielsen ND, Shapiro NI, Gerbasi ME, Grossman A, Doroff R, ZengF,YoungPJ,RussellJA.Meanarterialpressureandmortalityinpatientswithdistributiveshock:aretrospectiveanalysisoftheMIMIC‑IIIdatabase.AnnIntensiveCare.2018;8:107.
17. Persichini R, Silva S, Teboul JL, Jozwiak M, Chemla D, Richard C, Monnet X. Effects of norepinephrine on mean systemic pressure and venous return in human septic shock.CritCareMed.2012;40(12):3146–53.
18. Ospina‑Tascon GA, Hernandez G,Alvarez I, Calderon‑TapiaLE, Manzano‑Nunez R, Sanchez‑Ortiz AI, Quinones E, Ruiz‑Yucuma JE, Aldana JL, TeboulJL, et al. Effects of very early start of norepinephrine in patients with septic shock: a propensity score‑basedanalysis.CritCare.2020;24(1):52.
19. Ospina‑Tascón GA, Teboul JL, Hernandez G, Alvarez I, Sánchez‑Ortiz AI,Calderón‑TapiaLE,Manzano‑NunezR,QuiñonesE,Madriñan‑NaviaHJ,RuizJE,etal.Diastolic shock index and clinical outcomes in patients with septic shock.AnnIntensiveCare.2020;10(1):41.
20. DeBacker D,Creteur J, NoordallyO, SmailN, Gulbis B,Vincent JL. Does hepato‑splanchnic VO2/DO2 dependency exist in critically ill septicpatients?AmJRespirCritCareMed.1998;157:1219–25.
21. De Backer D, Creteur J, Preiser JC, Dubois MJ, Vincent JL. Microvascular blood flow is altered in patients with sepsis.AmJRespirCritCareMed.2002;166:98–104.
22. Hernandez G, Luengo C, Bruhn A, Kattan E, Friedman G, Ospina‑Tascon GA, Fuentealba A, CastroR, RegueiraT, RomeroC, et al. When to stop septic shock resuscitation: clues from a dynamic perfusion monitoring.AnnIntensiveCare.2014;4:30.
23. BakkerJ, DeBackerD, HernandezG. Lactate‑guided resuscitation saves lives: weare not sure.IntensiveCareMed.2016;42(3):472–4.
24. Brunauer A, KoköferA, BataarO, Gradwohl‑MatisI, Dankl D,Bakker J,Dünser MW. Changes in peripheral perfusion relate to visceral organ perfusion in early septic shock: a pilot study.JCritCare.2016;35:105–9.
25. BoermaEC, KuiperMA, KingmaWP, EgbersPH, GerritsenRT, InceC. Disparity between skin perfusion and sublingual microcirculatory alteration sinse vere sepsis and septic shock: a prospective observational study.IntensiveCareMed.2008;34:1294–8.
26. Brabrand M, Hosbond S, Folkestad L. Capillary refill time: a study of inter‑observer reliability among nurses and nurse assistants. Eur J Emerg Med.2011;18(1):46–9.
27. ZampieriFG,DamianiLP,BakkerJ,Ospina‑TasconGA,CastroR,CavalcantiAB, Hernandez G. Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate levels on 28‑day mortality among patients with septic shock:a Bayesian Re analysis of the ANDROMEDA‑SHOCKTrial.AmJRespirCritCareMed.2019.https://doi.org/10.1164/rccm.201905‑0968OC.
28. LiuX, LuoD, ZhangJ,DuL. Distribution and relative expression of vasoactive receptors on arteries. SciRep. 2020;10(1):15383.
29. Asfar P, Meziani F, Hamel JF, Grelon F, Megarbane B, Anguel N, Mira JP, DequinPF, GergaudS, WeissN,etal. High versus low blood‑pressure target in patients with septic shock.NEnglJMed.2014;370(17):1583–93.
30. LamontagneF,Richards‑BelleA,ThomasK,HarrisonDA,SadiqueMZ,Grieve RD, Camsooksai J, Darnell R, Gordon AC, Henry D, et al. Effect of reduced exposure to vasopressors on 90‑day mortality in older critically Ill patients with vasodilatory hypotension: a randomized clinical trial.JAMA.2020;323(10):938–49.
31. DeruddreS, CheissonG, MazoitJX,VicautE,BenhamouD,DuranteauJ. Renal arterial resistance in septic shock: effects of in creasing mean arterial pressure with norepinephrine on the renal resistive index assessedwithDopplerultrasonography.IntensiveCareMed.2007;33(9):1557–62.
32. Gershengorn HB, StelfoxHT, NivenDJ, WunschH.Association of premorbid blood pressure with vasopressor infusion duration in patients with shock. Am J Respir Crit Care Med. 2020;202(1):91–9.
33. DeBackerD,VincentJL. Should we measure the central venous pressure to guide fluid management? Ten answers to 10 questions. Crit Care.2018;22(1):43.
34. DeBackerD,AissaouiN,CecconiM,ChewMS,DenaultA,HajjarL,Her‑nandezG,MessinaA,MyatraSN,OstermannM,etal.Howcanassessinghemodynamicshelptoassessvolumestatus?IntensiveCareMed.2022.https://doi.org/10.1007/s00134‑022‑06808‑9.
35. DeBackerD,CreteurJ,Dubois MJ,SakrY,VincentJL. Microvascular alterations in patients with acute severe heart failure and cardiogenic shock.AmHeartJ.2004;147:91–9.
36. DeBacker D, VincentJL. Early goal‑directed therapy: do we have a definitive answer?IntensiveCareMed.2016;42(6):1048–50.
37. Ospina‑Tascon GA, Umana M, Bermudez WF, Bautista‑Rincon DF, Valencia JD, Madrinan HJ, HernandezьG, Bruhn A, Arango‑Davila C, DeBacker D. Can venous‑to‑arterial carbon dioxide differences reflect microcirculatory alterations in patients with septic shock?IntensiveCareMed.2016;42(2):211–21.
38. ValleeF, ValletB ,MatheO, ParraguetteJ, MariA, SilvaS, SamiiK, FourcadeO, GenestalM .Central venous‑to‑arterial carbondioxide difference: an additional target for goal‑directed therapy in septic shock? Intensive CareMed.2008;34(12):2218–25.
39. Mesquida J, Saludes P, Gruartmoner G, Espinal C, Torrents E, Baigorri F, ArtigasA. Central venous‑to‑arterial carbondioxide difference combined with arterial‑to‑venous oxygen content difference is associated with lactate volution in the hemodynamic resuscitation process in early septic shock.CritCare.2015;19:126.
40. Ospina‑TasconGA, Bautista‑Rincon DF, Umana M, Tafur JD, Gutierrez A,GarciaAF,BermudezW,GranadosM,Arango‑DavilaC,HernandezG.Persistently high venous‑to‑arterial carbondioxide differences during early resuscitation are associated with poor outcomes in septic shock.CritCare.2013;17(6):R294.
41. DuW, LiuDW, WangXT, LongY, ChaiWZ, ZhouX, RuiX. Combining central venous‑to‑arterial partial pressure of carbon dioxide difference and central venous oxygen saturation to guide resuscitation in septic shock. JCritCare.2013;28(6):1110–5.
42. Ospina‑TasconGA, UmanaM, BermudezW, Bautista‑RinconDF, Hern‑dez G, Bruhn A, Granados M, Salazar B, Arango‑Davila C, De Backer D. Combination of arterial lactate levels and venous‑arterial CO to arterial‑venous O content difference ratio as markers of resuscitation in patientswithsepticshock.IntensiveCareMed.2015;41:796–805.
43. MonnetX,JulienF,Ait‑HamouN,LequoyM,GossetC,JozwiakM,Persi‑chiniR,AnguelN,RichardC,TeboulJL. Lactate and venoarterial carbon dioxide difference/arterial‑venous oxygen difference ratio, but not central venous oxygen saturation, predict increase in oxygen consumption in fluid responders.CritCareMed.2013;41(6):1412–20.
44. Jansen TC, van Bommel J, Schoonderbeek J, Sleeswijk Visser SJ, van der Klooster JM, LimaAP, Willemsen SP, Bakker J. Early lactate‑guided therapy in ICU patients: a multicenter, open‑label, randomized, controlled trial.AmJRespirCritCareMed.2010;182(6):752–61.
45. RimachiR, Bruzzi DC, Orellano‑Jimenez C, Cotton F,Vincent J, De Backer D. Lactate/pyruvate ratio a samarker of tissue hypoxia in circulatory and septic shock. Anaesth Intensive Care.2012;40(3):427–32.
46. KattanE, Hernández G,ьOspina‑Tascón G, Valenzuela ED, Bakker J, CastroR.A lactate‑targeted resuscitation strategy may be associated with higher mortality in patients with septic shock and normal capillary refill time: a posthoc analysis of the ANDROMEDA‑SHOCK study. Ann Intensive Care.2020;10(1):114.
47. GeriG,VignonP,AubryA,FedouAL,CharronC,SilvaS,RepesséX,Vieillard‑Baron A. Cardiovascular clusters in septic shock combining clinical and echocardiographic parameters: a posthoc analysis. Intensive Care Med.2019;45(5):657–67.
48. Kouz K, Scheeren TWL, de Backer D, Saugel B. Pulse wave analysis to estimate cardiac output. Anesthesiology.2021;134:119–26.
49. Monnet X, Teboul JL. Transpulmonary thermodilution: advantages and limits. Crit Care.2017;21(1):147.
50. Teboul JL, Sauge lB, Cecconi M, De BD, Hofer CK, Monnet X, Perel A, Pinsky MR, Reuter DA, Rhodes A, et al. Less invasive hemodynamic monitoring in critically ill patients. Intensive Care Med. 2016. https://doi.org/10.1007/s00134‑016‑4375‑7.
51. Boissier F, Katsahian S, Razazi K, Thille AW, Roche‑CampoF, Leon R, Vivier E, Brochard L, Vieillard‑Baron A, Brun‑Buisson C, et al. Prevalence and prognosis of corpulmonale during protective ventilation for acute Respiratory distress syndrome. IntensiveCareMed.2013;39(10):1725–33.
52. Murugan R, Kerti SJ, Chang CH, Gallagher M, Clermont G, Palevsky PM, Kellum JA, Bellomo R. Association of net ultrafiltration rate with mortality among critically Ill adults with acute kidney injury receiving continuous veno venous hemodiafiltration: a secondary analysis of the randomized evaluation of normal vs augmented level (RENAL) of renal replacementtherapytrial.JAMANetwOpen.2019;2(6):e195418.
53. Monnet X, Cipriani F, Camous L, Sentenac P, Dres M, Krastinova E, Anguel N, Richard C, Teboul JL. The passive legraising test to guide fluid removal in critically ill patients.AnnIntensiveCare.2016;6(1):46.
54. MongkolpunW, BakosP, VincentJL, CreteurJ. Monitoring skin blood flow to rapidly identify alterations in tissue perfusion during fluid removal using continuous veno‑venous hemofiltration in patients with circulatory shock. AnnIntensive Care.2021;11(1):59.
55. Guinot PG, Bernard E, Levrard M, Dupont H, Lorne E. Dynamic arterial elastance predicts mean arterial pressure decrease associated with decreasing norepinephrine dosage in septic shock. Crit Care.2015;19:14.
56. Meyhoff TS, Hjortrup PB, Wetterslev J, Sivapalan P, Laake JH, Cronhjort M, Jakob SM, Cecconi M, Nalos M, Ostermann M ,et al .Restriction Of intravenous fluid in ICU patients with septic shock. N Eng l J Med.2022;386(26):2459–70.
57. Monnet X, Shi R, Teboul JL. Prediction of fluid responsiveness.What’s new? Annal Intensive Care.2022;12(1):46.
58. VanRegenmorte lN, Verbrugghe W, Roelant E, VandenWyngaert T, Jorens PG. Maintenance fluid therapy and fluid creep impose more significant fluid, sodium, and chloride burdens than resuscitation fluids in critically ill patients: a retrospective study in a tertiary mixed ICU popula‑tion.IntensiveCareMed.2018;44(4):409–17.
59. De Backer D, Biston P, Devriendt J, Madl C, Chochrad D, Aldecoa C, Brasseur A, Defrance P, Gottignies P, VincentJL. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med.2010;362(9):779–89.
60. DeBacker D, Aldecoa C, Njimi H, Vincent J‑L. Dopamine versus norepinephrine in the treatment of septic shock: a meta analysis.CritCareMed.2012;40:725–30.
61. Vail E, Gershengorn HB, Hua M, Walkey AJ, Rubenfeld G, Wunsch H. Association between US norepinephrine short age and mortality among patients with septic shock. JAMA.2017;317(14):1433–42.
62. Russell JA, Walley KR, Singer J, Gordon AC, Hebert PC, Cooper DJ, Holmes CL, Mehta S, Granton JT, Storms MM, et al. Vasopressin versus norepinephrine infusion in patients with septic shock.NEnglJMed.2008;358(9):877–87.
63. Gordon AC, Mason AJ, Thirunavukkarasu N, Perkins GD, Cecconi M, Cepkova M, Pogson DG, Aya HD, Anjum A, Frazier GJ, et al. Effect of early vasopressin vs norepinephrine on kidney failure in patients with septic shock: The VANISHrandomizedclinicaltrial.JAMA.2016;316(5):509–18.
64. Hajjar LA, Vincent JL, Barbosa Gomes Galas FR, Rhodes A, Landoni G, Osawa EA, Melo RR, Sundin MR, Grande SM, Gaiotto FA, et al. Vasopressin versus norepinephrine in patients with vasoplegic shock after cardiac surgery: the VANCS randomized controlled trial. Anesthesiology.2017;126(1):85–93.
65. Nagendran M, Russell JA, Walley KR, Brett SJ, Perkins GD, HajjarL, MasonAJ, AshbyD, Gordon AC. Vasopressin in septic shock: an individual patient datameta‑analysis of randomized controlled trials.IntensiveCareMed.2019;45(6):844–55.
66. Liu ZM, Chen J, Kou Q, Lin Q, Huang X, Tang Z, Kang Y, Li K, Zhou L, Song Q, et al. Terlipressin versus norepinephrine as infusion in patients with septic shock: a multicentre, randomised, double‑blinded trial. Intensive Care Med.2018;44(11):1816–25.
67. Zhu Y, Huang H, Xi X, Du B. Terlipressin for septic shock patients: a meta‑analysis of randomized controlled study. J Intensive Care.2019;7:16.
68. Laterre PF, Berry SM, Blemings A, Carlsen JE, Francois B, Graves T, Jacobsen K, Lewis RJ, Opal SM, PernerA, et al. Effect of selepressin vs placebo on ventilator‑ and vasopressor‑free days in patients with septic shock: the SEPSIS‑ACT randomized clinical trial.JAMA.2019.https://doi.org/10.1001/jama.2019.14607.
69. Rehberg S , Ertmer C, Vincent JL, Morelli A, Schneider M, Lange M, VanAken H, Traber DL, Westphal M. Role of selective V1a receptor agonism in ovine septic shock. Crit Care Med.2011;39(1):119–25.
70. Khanna A, English SW , Wang XS, Ham K, Tumlin J, Szerlip H, Busse LW, Altawee lL, Albertson TE, Mackey C, et al. Angiotensin II for the treatment of vasodilatory shock. N Engl J Med.2017;377(5):419–30.
71. Tumlin JA, Murugan R, Deane AM, Ostermann M, Busse LW, Ham KR, Kashani K, Szerlip HM, Prowle JR, Bihorac A, et al. Outcomes in patients with vasodilatory shock and renal replacement therapy treated with intravenous angiotensin II. Crit Care Med.2018;46(6):949–57.
72. Chawla LS, Ostermann M, ForniL, Tidmarsh GF. Broad spectrum vasopressors: a new approach to the initial management of septic shock? CritCare.2019;23(1):124.
73. Nakada TA, Russell JA, Boyd JH, Aguirre‑Hernandez R, Thain KR, Thair SA, Nakada E, McConechy M, Walley KR. beta2‑Adrenergic receptor gene polymorphism is associated with mortality in septic shock. Am J RespirCritCareMed.2010;181(2):143–9.
74. Anantasit N, Boyd JH, Walley KR, Russell JA. Serious adverse events associated with vasopressin and norepinephrine infusion in septic shock. CritCareMed.2014;42(8):1812–20.
75. Chawla LS, Chen S, Bellomo R, Tidmarsh GF. Angiotensin converting enzyme defects in shock: implications for future therapy. Crit Care.2018;22(1):274.
76. Bellomo R, Forni LG, Busse LW, McCurdy MT, Ham KR, Boldt DW, Hästbacka J, Khanna AK, Albertson TE, Tumlin J, et al. Renin and survival inpatients given angiotensin II for catecholamine‑resistant vasodilatoryshock.Aclinicaltrial.AmJRespirCritCareMed.2020;202(9):1253–61.
77. Bentzer P, Fjell C, Walley KR, Boyd J, Russell JA. Plasma cytokine levels predict response to corticosteroids in septic shock. Intensive Care Med.2016;42(12):1970–9.
78. Antcliffe DB, Burnham KL, Al‑Beidh F, Santhakumaran S, Brett SJ, Hinds CJ, Ashby D, Knight JC, Gordon AC. Transcriptomic signatures in sepsis and a differential response to steroids. From the VANISH randomized trial. Am JRespirCritCareMed.2019;199(8):980–6.
79. GordonAC,PerkinsGD,SingerM,McAuleyDF,OrmeRM,Santhaku‑maranS,MasonAJ,CrossM,Al‑BeidhF,Best‑LaneJ,etal.Levosimendanfor the prevention of acute organ dysfunction in sepsis. N Engl J Med.2016;375:1638–48.
80. Antcliffe DB, Santhakumaran S, Orme RML, Ward JK, Al‑Beidh F, O’Dea K, Perkins GD, Singer M, McAuley DF, Mason A J, et al. Levosimendan in septic shock in patients with biochemical evidence of cardiac dysfunction: a subgroup analysis of the LeoPARDS randomized trial. Intensive Care Med.2019;45(10):1392–400.
81. Chauvet JL, El‑Dash S, Delastre O, Bouffandeau B, Jusserand D, Michot JB, Bauer F , Maizel J, Slama M. Early dynamic left intraventricular obstructtion is associated with hypovolemia and high mortality in septic shock patients. Crit Care.2015;19:262.
Источник фотоиллюстрации - www.freepik.com
[DETAIL_PICTURE] =>
[DATE_ACTIVE_FROM] => 23.01.2023
[ACTIVE_FROM] => 23.01.2023
[SHOW_COUNTER] => 1288
)
[PROPERTIES] => Array
(
[KEYWORDS] => Array
(
[ID] => 1
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 100
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 102
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 828304
[VALUE] => гемодинамика, септический шок
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => гемодинамика, септический шок
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[DESCRIPTION] => Array
(
[ID] => 64
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Описание
[ACTIVE] => Y
[SORT] => 200
[CODE] => DESCRIPTION
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Описание
[~DEFAULT_VALUE] =>
)
[BROWSER_TITLE] => Array
(
[ID] => 9
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Заголовок окна браузера
[ACTIVE] => Y
[SORT] => 300
[CODE] => BROWSER_TITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => content-articles-property-browser_title
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => Y
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 828305
[VALUE] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[~DESCRIPTION] =>
[~NAME] => Заголовок окна браузера
[~DEFAULT_VALUE] =>
)
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 830458
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
)
[vote_count] => Array
(
[ID] => 100
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Количество проголосовавших
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_count
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество проголосовавших
[~DEFAULT_VALUE] =>
)
[vote_sum] => Array
(
[ID] => 101
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Сумма оценок
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_sum
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Сумма оценок
[~DEFAULT_VALUE] =>
)
[rating] => Array
(
[ID] => 102
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Рейтинг
[ACTIVE] => Y
[SORT] => 500
[CODE] => rating
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Рейтинг
[~DEFAULT_VALUE] =>
)
[FAVORITES] => Array
(
[ID] => 148
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Избранное
[ACTIVE] => Y
[SORT] => 500
[CODE] => FAVORITES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Избранное
[~DEFAULT_VALUE] =>
)
[LIKE] => Array
(
[ID] => 153
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Понравилось
[ACTIVE] => Y
[SORT] => 500
[CODE] => LIKE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Понравилось
[~DEFAULT_VALUE] =>
)
[SUBTITLE] => Array
(
[ID] => 93
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Подзаголовок
[ACTIVE] => Y
[SORT] => 501
[CODE] => SUBTITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Подзаголовок
[~DEFAULT_VALUE] =>
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828309
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
)
[QUOTE] => Array
(
[ID] => 95
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Цитата
[ACTIVE] => Y
[SORT] => 503
[CODE] => QUOTE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Цитата
[~DEFAULT_VALUE] =>
)
[SLIDER] => Array
(
[ID] => 98
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Слайдер
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер
[~DEFAULT_VALUE] =>
)
[SLIDER_DESC] => Array
(
[ID] => 99
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Слайдер описание
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER_DESC
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер описание
[~DEFAULT_VALUE] =>
)
[INFO_SOURCES] => Array
(
[ID] => 96
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Информация и источники
[ACTIVE] => Y
[SORT] => 504
[CODE] => INFO_SOURCES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Информация и источники
[~DEFAULT_VALUE] =>
)
[MATERIALS] => Array
(
[ID] => 97
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Материалы к статье
[ACTIVE] => Y
[SORT] => 505
[CODE] => MATERIALS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Материалы к статье
[~DEFAULT_VALUE] =>
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828307
[1] => 828308
)
[VALUE] => Array
(
[0] => sepsis
[1] => Infekcionnyj kontrol'
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => sepsis
[1] => Infekcionnyj kontrol'
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
)
[COMMENTS_COUNT] => Array
(
[ID] => 103
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Количество комментариев
[ACTIVE] => Y
[SORT] => 5010
[CODE] => COMMENTS_COUNT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество комментариев
[~DEFAULT_VALUE] =>
)
[FB2] => Array
(
[ID] => 173
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => FB2
[ACTIVE] => Y
[SORT] => 5020
[CODE] => FB2
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] => fb2
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => FB2
[~DEFAULT_VALUE] =>
)
[ADD_DATES] => Array
(
[ID] => 207
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Дата добавления материалов
[ACTIVE] => Y
[SORT] => 5030
[CODE] => ADD_DATES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => Date
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата добавления материалов
[~DEFAULT_VALUE] =>
)
[LENGHT] =>
[VIDEO_PREVIEW] =>
[VIDEO_FULL] =>
)
[DISPLAY_PROPERTIES] => Array
(
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 830458
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => да
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828309
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => [8] (info@sepsisforum.ru) Команда Сепсис Форума
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-07-03 10:45:52
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 828307
[1] => 828308
)
[VALUE] => Array
(
[0] => sepsis
[1] => Infekcionnyj kontrol'
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => sepsis
[1] => Infekcionnyj kontrol'
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => Array
(
[0] => Сепсис
[1] => Инфекционный контроль
)
)
)
[IBLOCK] => Array
(
[ID] => 2
[~ID] => 2
[TIMESTAMP_X] => 03.07.2025 10:45:52
[~TIMESTAMP_X] => 03.07.2025 10:45:52
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[LID] => s1
[~LID] => s1
[CODE] => articles
[~CODE] => articles
[API_CODE] =>
[~API_CODE] =>
[NAME] => Статьи
[~NAME] => Статьи
[ACTIVE] => Y
[~ACTIVE] => Y
[SORT] => 200
[~SORT] => 200
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[~DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[~SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[CANONICAL_PAGE_URL] =>
[~CANONICAL_PAGE_URL] =>
[PICTURE] =>
[~PICTURE] =>
[DESCRIPTION] => Статьи
[~DESCRIPTION] => Статьи
[DESCRIPTION_TYPE] => html
[~DESCRIPTION_TYPE] => html
[RSS_TTL] => 24
[~RSS_TTL] => 24
[RSS_ACTIVE] => Y
[~RSS_ACTIVE] => Y
[RSS_FILE_ACTIVE] => N
[~RSS_FILE_ACTIVE] => N
[RSS_FILE_LIMIT] =>
[~RSS_FILE_LIMIT] =>
[RSS_FILE_DAYS] =>
[~RSS_FILE_DAYS] =>
[RSS_YANDEX_ACTIVE] => N
[~RSS_YANDEX_ACTIVE] => N
[XML_ID] => content-articles
[~XML_ID] => content-articles
[TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[~TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[INDEX_ELEMENT] => Y
[~INDEX_ELEMENT] => Y
[INDEX_SECTION] => Y
[~INDEX_SECTION] => Y
[WORKFLOW] => N
[~WORKFLOW] => N
[BIZPROC] => N
[~BIZPROC] => N
[SECTION_CHOOSER] => L
[~SECTION_CHOOSER] => L
[LIST_MODE] =>
[~LIST_MODE] =>
[RIGHTS_MODE] => S
[~RIGHTS_MODE] => S
[SECTION_PROPERTY] => Y
[~SECTION_PROPERTY] => Y
[PROPERTY_INDEX] => I
[~PROPERTY_INDEX] => I
[VERSION] => 1
[~VERSION] => 1
[LAST_CONV_ELEMENT] => 0
[~LAST_CONV_ELEMENT] => 0
[SOCNET_GROUP_ID] =>
[~SOCNET_GROUP_ID] =>
[EDIT_FILE_BEFORE] =>
[~EDIT_FILE_BEFORE] =>
[EDIT_FILE_AFTER] =>
[~EDIT_FILE_AFTER] =>
[SECTIONS_NAME] => Разделы статей
[~SECTIONS_NAME] => Разделы статей
[SECTION_NAME] => Раздел статей
[~SECTION_NAME] => Раздел статей
[ELEMENTS_NAME] => Статьи
[~ELEMENTS_NAME] => Статьи
[ELEMENT_NAME] => Статья
[~ELEMENT_NAME] => Статья
[REST_ON] => N
[~REST_ON] => N
[FULLTEXT_INDEX] => N
[~FULLTEXT_INDEX] => N
[EXTERNAL_ID] => content-articles
[~EXTERNAL_ID] => content-articles
[LANG_DIR] => /
[~LANG_DIR] => /
[SERVER_NAME] => sepsisforum.ru
[~SERVER_NAME] => sepsisforum.ru
)
[SECTION] => Array
(
[PATH] => Array
(
)
)
[SECTION_URL] =>
[META_TAGS] => Array
(
[TITLE] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[BROWSER_TITLE] => Призыв к персонализации коррекции гемодинамики при септическом шоке
[KEYWORDS] => гемодинамика, септический шок
[DESCRIPTION] =>
)
)





