Инфузионная терапия у пациетов с септическим шоком и ожирением
Journal of Critical Care
B.R. Kiracofe-Hoyte, B.A. Doepker, H.M. Riha et al.
Оценка интенсивной инфузионной терапии по времени до стабилизации состояния у пациентов с ожирением и септическим шоком
Перевод оригинальной статьи «Assessment of fluid resuscitation on time to hemodynamic stability in obese patients with septic shock».
Ключевые слова: сепсис, септический шок, интенсивная инфузионная терапия, ожирение, индекс массы тела, гемодинамическая стабильность
Введение
Септический шок продолжает лидировать среди причин госпитальной летальности, составляя 1/3 от всей госпитальной летальности [1, 2]. В поисках решения этой проблемы Общество по медицине критических состояний (the Society of Critical Care Medicine) и Европейское общество по интенсивной медицине (the European Society of Intensive Care Medicine) в 2016 и в 2018 годах обновили клинические рекомендации «the Surviving Sepsis Campaign (SSC)», касающихся менеджмента сепсиса и септического шока. Незамедлительное лечение сепсиса показало снижение летальности, а краеугольными камнями терапии остаются антибиотики широкого спектра действия и интенсивная инфузионная терапия [3-5]. Текущие рекомендации по проведению интенсивной инфузионной терапии говорят о быстром введении жидкости в виде кристаллоидных растворов в течение первого часа из расчета 30 мл/кг, при этом при расчете учитывается актуальная масса тела пациента [4].
Но один, но очень существенный вопрос, еще далек от решения и этот вопрос можно сформулировать так - а действительно ли начальное введение кристаллоидов в дозе 30 мл/кг, ориентируясь на актуальную массу тела (АМТ), улучшает клинические исходы пациентов с ожирением тогда, когда уже показано, что избыточное введение жидкости приводит к неблагоприятным клиническим исходам? [6,7]. Исследования показали, что пациенты, страдающие от сепсиса и септического шока на фоне ожирения, получают меньший объем жидкости при расчете этого объема на основании АМТ, чем пациенты без ожирения и при этом летальность пациентов с ожирением ниже [6,8-14]. Другое недавнее исследование при анализе подгрупп показало, что улучшение летальности у пациентов с ожирением было достигнуто тогда, когда объем начальной интенсивной инфузионной терапии рассчитывался, исходя из скорректированной массы тела (СМТ) (англ. adjusted body weight) [8]. Но на сегодняшний день не имеется исследований, направленных на поиск оптимального объема инфузии при реанимации пациентов с ожирением, страдающих от сепсиса и септического шока, того объема, который бы привел к улучшению клинических исходов у таких пациентов. И отсюда, цель нашего исследования заключалась в сравнении времени, необходимого для достижения гемодинамический стабильности (ГДС) у пациентов с ожирением и сепсисом/септическим шоком, которым проводилась начальная интенсивная инфузионная терапия в объемах или <30 мл/кг, или ≥30 мл/кг.
Материалы и методы
Дизайн исследования и популяция пациентов
Многоцентровое ретроспективное когортное исследование, проведенное в The Ohio State University Wexner Medical Center и в Methodist Le Bonheur Healthcare Hospitals в период между 01 января 2012 года и 31 сентябрь 2017 года. Каждый центр получил одобрение исследования от своих этических комитетов. В исследование были включены взрослые пациенты с ожирением [индекс массы тела (ИМТ) ≥30 кг/м2], поступившие в отделение интенсивной терапии из департамента неотложной помощи или из общей палаты госпиталя с септическим шоком, при котором требовалось проведение интенсивной инфузионной терапии и вазопрессорная поддержка. Из исследования были исключены пациенты менее 18 лет, беременные, инкурабельные со злокачественными новообразованиями, поступившие не из госпиталя, требующие продвинутой кардиальной поддержки жизни в первые 48 часов после установления диагноза сепсиса, а также пациенты с декомпенсированным циррозом или с острой печеночной недостаточностью, что требовало введения альбумина.
Оценка исходов
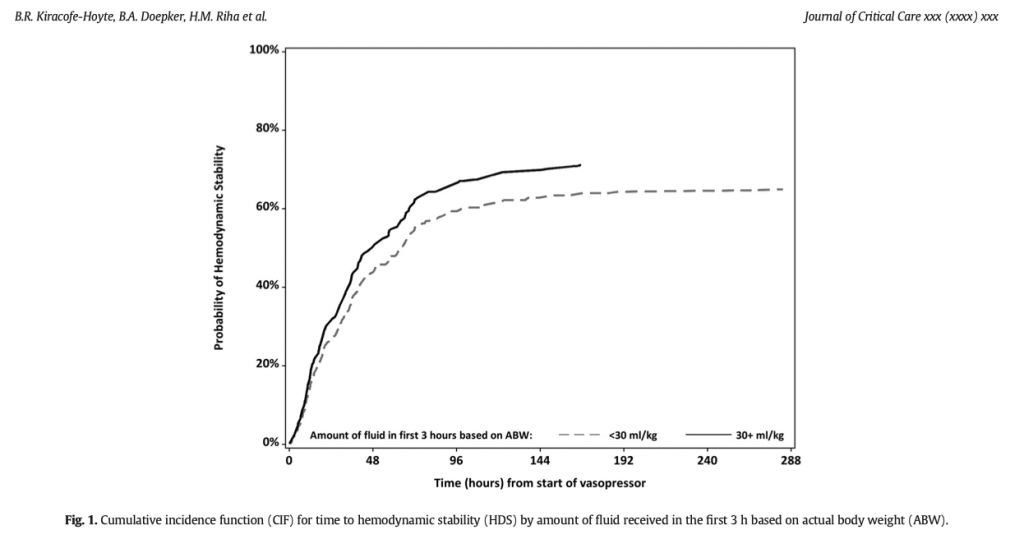
Основным клиническим исходом служило время до наступления ГДС у пациентов с ожирением, страдающих от септического шока, которые при начальной интенсивной терапии получили инфузию кристаллоидов в объеме как <30 мл/кг, так и ≥ 30 мл/кг. Время до наступления ГДС определяли как время в часах от начала вазопрессорной поддержки до отмены вазопрессоров в течение последующих 24 часов. Вторичные исходы включили в себя: свободные от вентилятора дни (СВД), объем инфузии в первые три часа интенсивной терапии; общий и чистый баланс жидкости к 24, 48 и 72 часам интенсивной терапии; использование диуретиков и острое повреждение почек (ОПП) в первые семь дней после установки диагноза сепсис; длительность нахождения пациента в ОИТ и в стацонаре; госпитальная летальность. Определения септического шока и вторичных исходов включены в дополнительные материалы (he Supplementary Appendix Description D1) [3,15-19].
Сбор данных
Данные пациентов собирались ретроспективно и для этого использовались электронные истории болезни (ЭИБ). Демографические данные пациентов при поступлении включали в себя: возраст, пол, этническое происхождение, рост, вес, идеальная масса тела (ИдМТ), скорректированная масса тела (СМТ), индекс массы тела (ИМТ). ИдМТ рассчитывалась как 50 кг (для мужчин) или 45 кг (для женщин) с прибавлением 2,3 кг на каждый дюйм свыше 5 футов. СМТ рассчитывалась по следующей формуле: СМТ=ИдМТ + 0.4(АМТ - ИдМТ). Анамнез включал в себя хроническую обструктивную болезнь легких, обструктивное сонное апноэ, застойную сердечную недостаточность, хронические болезни почек (включая терминальную стадию), цирроз печени, иммуносупрессию, необходимость в искусственной вентиляции на дому, индекс коморбидности Чарлсона (ИКЧ). Тяжесть состояния оценивалась по шкале APACHE II (the Acute Physiology and Chronic Health Evaluation) в первые 24 часа после установки диагноза сепсис. Измерения интенсивной инфузионной терапии заключались в оценке типа инфузионного раствора на начальном этапе интенсивной терапии, объема жидкости в виде общего и чистого жидкостного баланса на 24, 38 и 72 часы терапии. Другие клинические характеристики включали в себя сывороточный креатинин (СКр) и лактат, пиковые значения СКр и лактата, количество диуретиков (эквивалентных в/в фуросемиду) в течение первых семи суток, развитие ОПП или острого респираторного дистресс-синдрома в первые семь суток течения септического шока, применение преднизолона или его эквивалентов более 50 мг или применение мидодрина в схеме вазопрессорной поддержки, начало эмпирической антибактериальной терапии в первые три часа после проявления клинической картины сепсиса, источник инфекции, положительные микробиологические посевы в первые пять суток, адекватность начальной антибактериальной терапии, длительность искусственной вентиляции легких (ИВЛ), СВД, длительность нахождения пациента в ОИТ и в госпитале, госпитальную летальность.
Статистика
Для первичного анализа демографические характеристики были суммированы с использованием соответствующей описательной статистики (частота, процентное соотношение для категориальных переменных и средних, стандартные отклонения или медианы, IQR [25–75%] для непрерывных переменных). Время до ГДС оценивалось с использованием подхода конкурирующих рисков (кумулятивные функции заболеваемости и модель риска подраспределения Fine-Gray) для учета конкурирующего события - смерти в больнице. Обратите внимание, что все пациенты в исследовании либо достигли ГДС, либо умерли в течение 7 дней. Для модели с множеством переменных для включения в качестве вмешивающих факторов рассматривались следующие факторы из-за: (1) их установленной связи с исходами сепсиса, а также из-за (2) их потенциальной роли во влиянии на индивидуальные решения врача относительно выбора объема инфузионной терапии и сюда относятся пол, возраст, этническая принадлежность (белые против не-белых), ИМТ, ИКЧ, оценка APACHE II и антибиотики [8-12,20-24]. Все показатели, включенные в многопараметрическую модель, были собраны или рассчитаны до или близко к начальному объему жидкости. Для всех факторов мы оценили возможное изменение эффекта путем тестирования двусторонних взаимодействий с выбранным объемом жидкости. Не было обнаружено значимых (p <0,05) взаимодействий (данные не показаны). Затем с помощью логистической регрессии оценивали внутрибольничную летальность (да/нет) между группами, различающими по объему инфузии. Подобно времени до достижения ГДС, многомерная модель с использованием тех же факторов, перечисленных выше, соответствовала данным.
Для вторичных исходов для сравнения СВД использовались описательная статистика и критерий суммы рангов Вилкоксона. Непараметрические тесты использовались для сравнения ОИТ и длительности госпитализации между группами. Групповые различия, связанные с категориальными исходами, сравнивались с использованием критерия χ 2 или точного критерия Фишера. Тенденции общего количества введенной жидкости с течением времени оценивались с использованием моделей повторных измерений. P-значения для этих вторичных исходов были скорректированы с использованием процедуры Холма.
И, наконец, был проведен анализ подгрупп для того, чтобы оценить время до достижения ГДС и риск смерти в госпитале среди различных стратегий дозирования жидкости при проведении интенсивной терапии (АМТ, СМТ, ИдМТ). Пациенты были разделены на стратегии дозирования согласно АМТ, СМТ, ИдМТ путем деления общего количества жидкости, полученной за три часа, на 30 мл/кг и определения, является ли это значение наиболее близким к АМТ, СМТ, ИдМТ пациента. Пациенты исключались из анализа подгруппы, если количество жидкости в мл/кг не находилось в пределах, по крайней мере, 10% от стратегии дозирования, основанной на конкретной массе тела. По этому критерию были классифицированы и включены в анализ подгруппы 227 пациентов. Статистические методы анализа подгрупп аналогичны описанным ранее. Все анализы были выполнены с использованием программного обеспечения SAS / STAT v14.1 (SAS v9.4 for Windows, SAS Institute, Inc., Cary, NC).
Результаты
Базовые характеристики
Изначально обследовано 774 пациента. В общей сложности 452 пациента были исключены по основным причинам: перевод из стационара (n = 195), расширенная система жизнеобеспечения сердца (n = 101), альбумин/цирроз печени (n = 57), заключение в тюрьму (n = 17) и другие критерии исключения (n = 82). Из 322 пациентов, отвечающих критериям включения, 106 (33%) получили ≥30 мл/кг первоначальной инфузии на основании АМТ в первые три часа от начала сепсиса. Исходные характеристики показаны в таблице 1, где группа <30 мл/кг имеет более высокие показатели веса, ИМТ и индекса коморбидности Чарльсона.
Вмешательства
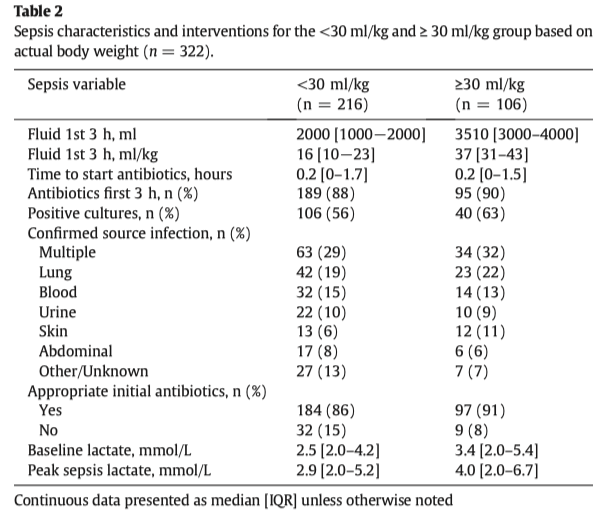
В таблице 2 показано сравнение между вмешательствами для групп <30 мл/кг и ≥ 30 мл/кг (расчет на основе АМТ). Группа <30 мл/кг получила меньший объем жидкости в первые три часа терапии, 16 против 37 мл/кг. Проявился интересный тренд - с увеличением актуальной массы тела пациента количество переливаемой ему жидкости в первые три часа терапии снижалось (Supplementary Appendix Рис. 1). Не было найдено статистически достоверной разницы между группами в проведении инфузионной терапии сбалансированными растворами (<30 мл/кг 16% vs. 24%) или несбалансированными растворами (<30 ml/kg 76% vs. 75%), в большинстве своем назначались несбалансированные растворы (данные не показаны). Также не было строгой разницы в хронической сердечной недостаточности (ХСН), в хронической болезни почек (ХБП), хронической почечной недостаточности в терминальной стадии и в ОРДС. Обе группы имели одинаковое время начала антибактериальной терапии и одинаковую частоту положительных микробиологических посевов (Таб. 2).
Зависимость исходов от выбранной стратегии инфузионной терапии
Исследовательский анализ подгрупп был выполнен в соответствии со стратегией дозирования жидкости (АМТ, ИдМТ или СМТ). В общей сложности, всем 227 пациентам была проведена оценка на основании показателя «мл/кг» жидкости, введенной в первые три часа от начала сепсиса: 118 пациентам расчет проводился на основании АМТ (52%), 63 - на основании ИдМТ (28%) и 46 - на основании СМТ (20%). Исходные характеристики и вмешательства при сепсисе для всех этих стратегий дозирования показаны в дополнительных таблицах S2 и S3 приложения. Подобно нашему первичному анализу, не было значительных различий между стратегиями дозирования в нескорректированном анализе, сравнивающем время до наступления ГДС и смерти в стационаре (таблица S4 дополнительного приложения). Однако, после внесения поправки на клинически значимые факторы, а именно этническая принадлежность, пол, возраст, ИМТ, показатель ИКЧ, показатель APACHE II и адекватность назначения антибиотиков, мы обнаружили, что пациенты, получившие при начальной интенсивной инфузионной терапии ≥30 мл/кг жидкости в соответствии с АМТ, имели более высокую частоту достижения ГДС, чем пациенты, которым расчет объема инфузии проводился по ИдМТ. Кроме того, вероятность смерти в стационаре была выше для пациентов, которым стратегия инфузии выбиралась основе ИдМТ, по сравнению с АМТ [OR 3,05, 95% CI: 1,34, 6,97; p = 0,008 (Таблица дополнительного приложения S5)]. Но вот когда стратегия инфузии выбиралась на основании СМТ, то при сравнении с АМТ не наблюдалось значительных различий во времени достижения ГДС или смерти в стационаре.
Дискуссия
Наше исследование является первым, в котором сравнивались стратегии начальной интенсивной инфузионной терапии в группах <30 мл/кг или ≥ 30 мл/кг исключительно у пациентов с ожирением, страдающих от септического шока, в котором сделана попытка определить, имеется ли значительная разница во времени достижения гемодинамической стабильности (ГДС). После оценки пациентов по этнической принадлежности, полу, возрасту, ИМТ, индексу коморбидности Чарльсона, APACHE II и адекватности антибактериальной терапии, мы нашли, что пациенты с ожирением, у которых развивается септический шок и которым проводят инфузионную терапию в объеме ≥30 мл/кг, основанную на АМТ, имеют лучшие показатели как в достижении ГДС (p = 0.038), так и в риске смерти в госпитале (p = 0.038) по сравнению с теми, кому инфузия проводилась из расчета <30 мл/кг. Также наш исследовательский анализ показал, что начальная интенсивная инфузионная терапия, основанная на ИдМТ, приводит к более длительному времени достижения ГДС и к более высокому риску госпитальной смерти при сравнении с инфузионной терапией, основанной на АМТ или на СМТ. Такие результаты предполагают, что следование клиническому руководству SSC, в котором указан объем необходимой инфузии в 30 мл/кг, основанный на АМТ, может приносить пользу пациентам с ожирением, но необходимы дальнейшие исследования между стратегиями инфузионной терапии, основанными на АМТ (актуальная масса тела) или на СМТ (скорректированная масса тела).
Многочисленные исследования выявили весьма неудовлетворительное соблюдение рекомендованной SSC стратегии инфузионной интенсивной терапии из расчета 30 мл/кг, особенно это касается пациентов с ожирением [6,8-12,25]. Наше исследование тоже показало этот феномен, поскольку только 33% пациентов в первые 3 часа от начала сепсиса получили объем жидкости ≥30 мл/кг. Тем не менее, даже при проведении интенсивной инфузионной терапии, объем которой рассчитывался на основе меньшего веса, ранее проведенные исследования показали, что пациенты с ожирением и сепсисом имеют более низкий уровень общей летальности по сравнению с пациентами без ожирения, что называется парадоксом ожирения. [6,8,10,12-14]. Pepper and colleagues недавно сообщили в своем большом исследовании, в которое было включено более 55 000 пациентов, что у пациентов с ожирением более низкая общая летальность, 14 - 16%, по сравнению с пациентами без ожирения, 24%. В нашем исследовании госпитальная летальность составила 33%, однако все наши пациенты имели критерии септического шока и все они были госпитализированы в ОИТ тогда, когда в исследовании Pepper таких пациентов с септическим шоком в группе ожирения (ИМТ ≥30), переведенных в ОИТ, было только 28% [14]. Наше исследование стало первым, в котором показано, что у пациентов с ожирением, страдающих от септического шока, госпитальная летальность снижается тогда, когда объем инфузионной терапии, рассчитанный на основании АМТ, составляет 30 мл/кг, а рекомендация SSC соблюдается.
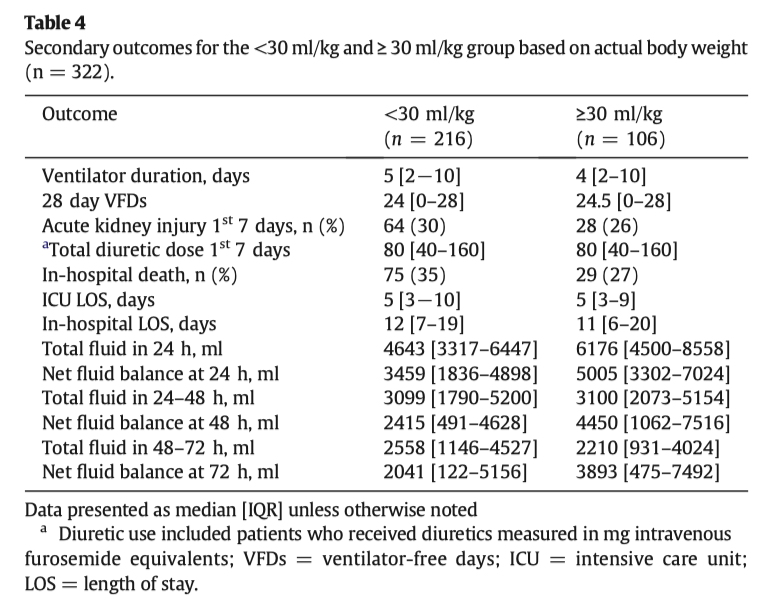
Также наше исследование единственное, в котором используется такой показатель, как время достижения гемодинамической стабильности, как первичный клинический исход при септическом шоке. Мы также сравнили другие клинические вторичные исходы, к которым относятся: количество свободных от вентилятора дней, частота возникновения ОПП и эти исходы могут оказывать свое влияние на длительность нахождения пациента в стационаре, стоимость лечения в госпитале, качество жизни пациента после выписки из стационара. Wacharasint and colleagues сообщили о своем анализе подгруппы пациентов с ожирением, и которые использовали данные исследования VASST (the Vasopressin and Septic Shock Trial). В этом анализе как вторичный исход идентифицировалась 28 дневная органная дисфункция. Авторы отметили, что пациенты с ожирением имели большее количество дней жизни и большее количество свободных дней от дисфункции коагуляции (p ≤ 0.001), а также меньшее количество инцидентов с определением 2 из 4 критериев синдрома системного воспалительного ответа (ССВО) по сравнению с пациентами без ожирения (p = 0.02). Однако, не было выявлено разницы между группами в днях жизни и свободных от вентилятора днях, а также в частоте проведения почечно-заместительный терапии [11]. Популяция пациентов с ожирением в исследовании Wacharasint была похожей на наших пациентов, так как пациенты в обоих исследованиях имели септический шок, похожие оценки по шкале APACHE II (27 vs. 25), а медиана ИМТ составила 34 кг/м2 [11]. Одновременно с этим, есть большие трудности в сравнении наших результатов с результатами других исследований из-за того, что наше исследование первое, в котором проводится сравнение стратегий интенсивной инфузионной терапии исключительно у пациентов с ожирением.
На сегодня только в одном исследовании изучался вопрос, а какой из трех показателей массы тела, АМТ, СМТ или ИдМТ, наиболее полезен для расчета объема интенсивной инфузионной терапии у пациентов с ожирением и сепсисом. Taylor and colleagues показали, что пациенты с ожирением, страдающие от сепсиса или септического шока, получили значительно меньше жидкости по показателю мл/кг в первые три часа терапии (p ≤ 0.001), однако снижение летальности пациентов с ожирением при сравнении с пациентами без ожирения после поправки на вмешивающие факторы/переменные больше не было статистически значимым. Их последующий анализ подгрупп, был направлен на выяснение идеального объема интенсивной инфузионной терапии у пациентов с ожирением. После корректировки на состояние и переменные, связанные с выбором типа терапии, которые могли оказывать влияние на летальность, оказалось, что пациенты с ожирением, которым объем начальной интенсивной инфузионной терапии рассчитывался с помощью СМТ имели снижение летальности на 55.2% по сравнению с АМТ, и на 71% летальность снижалась по сравнению с ИдМТ [8]. Наше исследование имело возможность проведения анализа подгруппы, состоящей из 227 пациентов, а сам анализ базировался на выборе стратегии инфузионной терапии и этот анализ показал, что стратегия выбора объема начальной интенсивной инфузионной терапии, основанная на АМТ, но где общий объем был равен ≥30 мл/кг, показала более короткое время до достижения ГДС и более низкую госпитальную летальность по сравнению со стратегией интенсивной инфузионной терапии, где объём ее рассчитывался на основании ИдМТ. В отличие от исследования Taylor, мы не нашли какой либо строгой разницы в госпитальной летальности при сравнении стратегий, основанных либо на АМТ, либо на СМТ. Основные отличия нашего исследования от исследования Тейлора заключаются в следующем: мы включили в исследование исключительно пациентов с ожирением; в нашем исследовании значительно более высокий уровень госпитальной летальности; все наши пациенты соответствовали критериям септического шока. В исследовании Taylor летальность составила 15% при том, что только 51% пациентов нуждался в вазопрессорной поддержке [8]. Результаты обоих этих исследований предполагают, что использование ИдМТ в целях расчета объема начальной интенсивной инфузионной терапии у пациентов с ожирением и сепсисом приводит к более высокому уровню госпитальной летальности, но, в тоже время, вопрос о том, что приводит к лучшим исходам, использование АМТ или СМТ, представляет интерес в будущем.
И наконец, наше исследование также оценивало маркеры перегрузки жидкостью, одним из них был положительный баланс жидкости в поздней фазе сепсиса, что ассоциируется с увеличением летальности [6,7,26,27].
Несмотря на высокий чистый баланс жидкости на 24, 48 и 72 часы после введения жидкости, мы обнаружили, что начальный болюс жидкости ≥30 мл/кг не увеличивает частоту развития ОПП, ОРДС, применения диуретиков, время искусственной вентиляции легких.
Одним из ограничений этого исследования является то, что оно является многоцентровым и ретроспективным по своей природе, а это приводит к тому, что точность подсчета введенной жидкости, ее баланса, а также и лекарственной терапии зависит исключительно от диаграмм в электронных базах историй болезни. Персоналом больницы или службами скорой медицинской помощи могли быть введены неизвестные жидкости и лекарства. Причину, по которой при проведении интенсивной инфузионной терапии не все пациенты получали 30 мл/кг, нельзя определить ретроспективно, однако различий между группами у пациентов с ХСН, ХПН, терминальной стадией ХПН, не наблюдалось, при этом мы учли некоторые потенциальные дисбалансы в переменных, которые использовались для нашего многомерного анализа. Использование ИМТ в качестве индикатора ожирения также является ограничением, поскольку это несовершенная мера ожирения. Однако, на сегодня этот показатель служит, как наиболее широко цитируемый маркер ожирения, который легко доступен ретроспективной оценке. Наконец, хотя всем включенным в исследование пациентам изначально проводилась вазопрессорная поддержка по причине септического шока, мы не исключаем и того, что пациента вазопрессорная поддержка после разрешения септического шока могла проводиться по другим клиническим показаниям.
Выводы
Наше исследование - первое, в котором сравниваются стратегии интенсивной инфузионной терапии исключительно у пациентов с ожирением и с септическим шоком. Мы обнаружили, что пациенты, которым была проведена начальная инфузионная терапия в объеме ≥30 мл/кг, а сам объем был рассчитан на основе АМТ, имели более короткое время до достижения ГДС и более низкий риск госпитальной летальности по сравнению с объемом жидкости <30 мл/кг. Также, результаты нашего анализа подгруппы предполагают, что пациенты с ожирением, которым вводят объем инфузии, равный 30 мл/кг на основе АМТ, могут иметь более короткое время достижения ГДС и более низкий риск госпитальной смерти по сравнению с расчетом, основанным на ИдМТ. Обращает свое внимание то, что не было обнаружено значительных различий во времени достижения ГДС или в смертельных исходах в стационаре между использованием АМТ и СМТ для расчета объема начальной интенсивной инфузионной терапии. Более того, не наблюдалось статистически значимых различий в других клинических исходах, таких как свободные от вентилятора дни или ОПП, между группами, в которых стратегия инфузионной терапии рассчитывалась на основании АМТ, но которые различались по конечному объему, либо <30 мл/кг, либо ≥30 мл/кг. Необходимы дальнейшие проспективные исследования для подтверждения оптимальной стратегии дозирования жидкости у пациентов с ожирением и сепсисом.
Дополнительные данные к этой статье можно найти в Интернете по адресу https://doi.org/10.1016/j.jcrc.2020.09.006.

Список литературы
[1] Epstein L, Dantes R, Magill S, et al. Varying estimates of sepsis mortality using death certificates and administrative codes–United States, 1999-2014. MMWR Morb Mortal Wkly Rep 2016;65(13):342–5.
[2] Mayr FB, Yende S, Angus DC. Epidemiology of severe sepsis. Virulence 2014;5(1): 4–11.
[3] Rhodes A, Evans LE, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Crit Care Med 2017; 45(3):486–552.
[4] Levy MM, Evans LE, Rhodes A, et al. The surviving sepsis campaign bundle: 2018 update. Crit Care Med 2018;46(s6):997–1000.
[5] Rivers E, Nguyen B, Havstad S, et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med 2001;345(19):1368–77.
[6] Pepper DJ, Sun J, Welsh J, et al. Increased body mass index and adjusted mortality in ICU patients with sepsis or septic shock: a systematic review and meta-analysis. Crit Care 2016;20(1):181.
[7] Boyd JH, Forbes J, Nakada TA, et al. Fluid resuscitation in septic shock: a positive fluid balance and elevated central venous pressure are associated with increased mortality. Crit Care Med 2011;39(2):259–65.
[8] Taylor SP, Karvetski CH, Templin MA, et al. Initial fluid resuscitation following adjusted body weight dosing is associated with improved mortality in obese patients with suspected septic shock. J Crit Care 2018;43:7–12.
[9] Adams C, Tucker C. Allen B, et al; disparities in hemodynamic resuscitation of the obese critically ill septic shock patient. J Crit Care 2017;37:219–23.
[10] Arabi YM, Dara SI, Tamim HM, et al. Clinical characteristics, sepsis interventions and outcomes in the obese patients with septic shock: an international multicenter cohort study. Crit Care 2013;17(2):R72.
[11] Wacharasint P, Boyd JH, Russell JA, et al. One size does not fit all in severe infection: obesity alters outcome, susceptibility, treatment, and inflammatory response. Crit Care 2013;17(3):R122.
[12] Wurzinger B, Dünser MW. Wohlmuth C, et al; the association between body-mass index and patient outcome in septic shock: a retrospective cohort study. Wien Klin Wochenschr 2010;122(1–2):31–6.
[13] Sakr Y, Alhussami I, Nanchal R, et al. Being overweight is associated with greater survival in ICU patients: results from the intensive care over nations audit. Crit Care Med 2015;43(12):2623–32.
[14] Pepper DJ, Demirkale CY, Sun J, et al. Does obesity protect against death in sepsis? A retrospective cohort study of 55,038 adult patients. Crit Care Med 2019;47(5): 643–50.
[15] Heart National. Lung, and blood institute acute respiratory distress syndrome (ARDS) clinical trials network, Wiedemann HP, wheeler AP, et al: comparison of two fluid-management strategies in acute lung injury. N Engl J Med 2006;354(24): 2564–75.
[16] Schoenfeld DA, Bernard GR. ARDS network: statistical evaluation of ventilator-free days as an efficacy measure in clinical trials of treatments for acute respiratory distress syndrome. Crit Care Med 2002;30(8):1772–7.
[17] Brater DC, Day B, Burdette A, et al. Bumetanide and furosemide in heart failure. Kidney Int 1984;26:183–9.
[18] Vargo DL, Kramer WG, Black PK, et al. Bioavailability, pharmacokinetics, and pharmacodynamics of torsemide and furosemide in patients with congestive heart failure. Clin Pharmacol Ther 1995;57:601–9.
[19] Bellomo R, Ronco C, Kellum JA, et al. Acute renal failure - definition, outcome measures, animal models, fluid therapy and information technology needs: the second international consensus conference of the acute Dialysis quality initiative (ADQI) group. Crit Care 2004;8(4):R204–12.
[20] Huang C, Ruan S, Tsia Y, et al. Clinical trajectories and causes of death in septic patients with a low APACHE II score. J Clin Med 2019;8(7):1064.
[21] Liu X, Shen Y, Li Z, et al. Prognostic significance of APACHE II score and plasma suPAR in Chinese patients with sepsis: a prospective observational study. BMC Anesthesiol 2016;16:46.
[22] Andersson M, Östholm-Balkhed Å, Fredrikson M, et al. Delay of appropriate antibiotic treatment is associated with high mortality in patients with community-onset sepsis in a Swedish setting. Eur J Clin Microbiol Infect Dis 2019;38:1223–34.
[23] Oltean S, Tatulescu D, Bondor C, et al. Charlson’s weighted index of comorbidities is useful in assessing the risk of death in septic patients. J Crit Care 2012;27:370–5.
[24] Yokota P, Marra A, Martino M, et al. Impact of appropriate antimicrobial therapy for patients with severe Sepsis and septic shock – a quality improvement study. PLoS One 2014;9(11):e104475.
[25] Truong TN, Dunn AS, McCardle K, et al. Adherence to fluid resuscitation guidelines and outcomes in patients with septic shock: reassessing the “one-size-fits-all” approach. J Crit Care 2019;51:94–8.
[26] DeOliveria FS, Freitas FG, Ferreira EM, et al. Positive fluid balance as a prognostic factor for mortality and acute kidney injury in severe sepsis and septic shock. J Crit Care 2015;30(1):97–101.
[27] Nevra JA, Li X, Canepa-Escaro F, et al. Cumulative fluid balance and mortality in septic patients with or without acute kidney injury and chronic kidney disease. Crit Care Med 2016;44(10):1891–900.
Journal of Critical Care