Array
(
[NAME] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[~NAME] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[PREVIEW_PICTURE] => Array
(
[ID] => 5844
[TIMESTAMP_X] => 11.11.2024 14:31:43
[MODULE_ID] => iblock
[HEIGHT] => 600
[WIDTH] => 900
[FILE_SIZE] => 38738
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j
[FILE_NAME] => der-adsorber-regain-control-cytosorb.jpg
[ORIGINAL_NAME] => der-adsorber-regain-control-cytosorb.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 501a6fe7ceacdb39ebe82b0bddac739b
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j/der-adsorber-regain-control-cytosorb.jpg
[UNSAFE_SRC] => /upload/iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j/der-adsorber-regain-control-cytosorb.jpg
[SAFE_SRC] => /upload/iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j/der-adsorber-regain-control-cytosorb.jpg
[ALT] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[TITLE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
)
[~PREVIEW_PICTURE] => 5844
[DETAIL_TEXT] =>
S Becker, H Lang, C V Barbosa, Z Tian, A Melk, B Schmidt
Efficacy of CytoSorb
®: asystematic review and meta-analysis
Critical Care (2023) 27:215 doi.org/10.1186/s13054-023-04492-9
Абстракт
Адсорбция цитокинов с использованием адсорбера CytoSorb® была предложена при различных клинических ситуациях, включая сепсис, ОРДС, гипервоспалительные синдромы, операции на сердце или восстановление после остановки кровообращения. Целью данного анализа является предоставление доказательств эффективности адсорбера CytoSorb® в отношении смертности в различных условиях. Провели поиск в базе данных PubMed, Cochrane Library и в базе данных Cytosorbents™ (01.1.2010–29.5.2022) и рассмотрели рандомизированные контролируемые исследования и наблюдательные исследования с контрольными группами. Самая поздняя зарегистрированная смертность была определена как первичная конечная точка. Мы рассчитали коэффициенты риска и 95%-ные доверительные интервалы и использовали модель случайных эффектов DerSimonian and Lairds. Проанализировали все исследования вместе и разделили их на подгруппы: сепсис, искусственное кровообращение (CPB), другие тяжелые заболевания, инфекция SARS-CoV-2 и восстановление после остановки сердца. Метаанализ был зарегистрирован заранее (PROSPERO: CRD42022290334). Из первоначальных 1295 публикаций были признаны подходящими 34 исследования, которые включали 1297 пациентов с использованием CytoSorb®, и 1314 пациентов контрольной группы. Вмешательство Cytosorb® не снизило смертность (RR [95%-ДИ]: все исследования 1,07 [0,88; 1,31], сепсис 0,98 [0,74; 1,31], операция искусственного кровообращения 0,91 [0,64; 1,29], другие тяжелые заболевания 0,95 [0,59; 1,55] , SARS-CoV-2 1,58 [0,50; 4,94]). У пациентов с остановкой сердца мы обнаружили значительное преимущество в выживаемости по сравнению с контрольной группой, не получавшей лечения (1,22 [1,02; 1,46]). Мы не обнаружили существенных различий в продолжительности пребывания в ОИТ, уровнях лактата или IL-6 после лечения. Из 34 исследований, отвечающих критериям отбора, только 12 были рандомизированными контролируемыми исследованиями. Все наблюдательные исследования показали риск систематической ошибки от умеренного до серьезного. На сегодняшний день нет доказательств положительного влияния адсорбера CytoSorb® на смертность при различных заболеваниях, что оправдывало бы его широкое использование в интенсивной терапии.
Введение
Массивный выброс цитокинов в кровь является патофизиологическим триггером многих опасных для жизни заболеваний. Провоспалительные цитокины приводят к вазодилатации, капиллярной утечке и коагулопатии. Противовоспалительные цитокины могут вызывать относительную иммуносупрессию, приводящую к вторичным нозокомиальным инфекциям. Неконтролируемый выброс обоих типов цитокинов может привести к развитию мультиорганной недостаточности [1]. Для неселективного снижения уровня цитокинов были предложены различные методы очистки крови, такие как диализ с использованием мембран с высокой точкой отсечки, гемосорбция, высокообъемная гемофильтрация и плазмообмен [2]. CytoSorb® - одно из наиболее широко используемых устройств для очистки крови, которое способно снижать уровень гидрофобных молекул с молекулярной массой до 55 кДа. [3] Таким образом, устройство адсорбирует цитокины, желчные кислоты и миоглобин. CytoSorb® находит клиническое применение у пациентов с избыточным иммунным ответом, например при сепсисе, ОРДС, SARS-CoV-2 инфекции, гиперинтенсивных воспалительных синдромах, а также во время и после кардиохирургических операций с использованием экстракорпорального кровообращения (CPB). Кроме того, CytoSorb® может быть полезен при печеночной недостаточности, для элиминации пероральных антикоагулянтов прямого действия (DOACs) или некоторых острых интоксикациях [4]. Устройство считается безопасным и хорошо переносится. Однако единого мнения по поводу эффективности нет. Целью этого систематического обзора и метаанализа является оценка влияния CytoSorb® на все ранее описанные заболевания. Первичной конечной точкой является самая поздняя зарегистрированная смертность. Кроме того, будут сравниваться продолжительность пребывания в отделении интенсивной терапии, потребности в норэпинефрине, уровни IL-6 и лактата.
Методы
Повели систематический поиск в базе данных PubMed и Cochrane Library, используя «CytoSorb» в качестве ключевого слова. Проверена база данных CytoSorbents https://literature.cytosorb-herapy.com/?_ga=2.58770730.642024760.1646225438-7175153.1645687922). Последнее обновление проведено 29 мая 2022 года. Исследования были выбраны двумя исследователями независимо; в случае разногласий искался консенсус. В соответствии с рекомендациями группы Bias Method Group Кокрейновской сети качество исследований оценивалось с помощью ROBINS-I (Risk of Bias in Non-randomized Studies of Interventions) или инструмента RoB 2 (revised tool for Risk of Bias in randomized trials). Данные были собраны двумя исследователями независимо и обобщены в файле Excel. Если вместо точных значений предоставлялись графики, мы анализировали данные с помощью «WebPlotDigitizer» (https://apps.automeris.io/wpd/). Первичной конечной точкой была самая поздняя зарегистрированная смертность (30-дневная смертность в стационаре или ОИТ). Если было представлено более одного значения, выбиралось значение с самым длительным периодом наблюдения. Первичная конечная точка рассчитывалась как относительный риск. Анализ подгрупп первичной конечной точки проводился для различных заболеваний (сепсис, искусственное кровообращение, тяжелое заболевание, SARS-CoV-2 и остановка сердца). Также был проведен анализ подгрупп для различных дизайнов исследований (рандомизированные контролируемые исследования по сравнению с наблюдательными исследованиями с соответствующими контрольными показателями по показателю предрасположенности и без них).
Для вычисления использовалась модель случайных эффектов (DerSimonian and Laird). Вторичными конечными точками были продолжительность пребывания в ОИТ и стационаре. Мы извлекли информацию о дозе норэпинефрина, среднем артериальном давлении (САД), СРБ, ПКТ, уровни лактата и интерлейкина-6 (IL-6) до и после использования CytoSorb®. Уровни маркеров воспаления после CytoSorb® определялись как первое зарегистрированное значение после начала лечения CytoSorb®. Кроме того, мы оценили показатели SOFA, SAPS-2 и APACHE-2, чтобы сравнить контрольную группу и группу вмешательства. Также проверили все исследования на предмет сообщений о нежелательных явлениях. Вторичные конечные точки были представлены в виде разницы рисков (группа лечения и группа контроля) для всех исследований в совокупности и для отдельных подгрупп. Анализ вторичных конечных точек проводился, если по крайней мере в двух исследованиях сообщалось о соответствующих данных. Для плановых операций с использованием экстракорпорального кровообращения показатели сепсиса и физиологические конечные точки не применялись. В оригинальных исследованиях вторичные конечные точки чаще всего сообщались в виде средних или медианных значений. Мы следовали рекомендациям McGrath et al [5]: при нормальном распределении средние значения считались равными медианам. Медианы с интерквартильным размахом или минимальными и максимальными значения были преобразованы в средние значения и стандартное отклонение по методу Luo et al. [6]. Впоследствии влияние средних значений оценивали с использованием модели случайного эффекта с использованием метода DerSimonian-Laird. Влияние медианных значений рассчитывали методом квантильной оценки. Риск систематической ошибки оценивался с помощью ROBINSI и RoB 2 двумя исследователями независимо. Мы использовали воронкообразные графики для оценки систематической ошибки публикации и применили методологию GRADE для оценки достоверности. Для всех анализов мы использовали R 4.1.0 с пакетами meta, metafor, metamedian, lqmm, hmisc, estmeansd, Forestplot и writexl. Значения P < 0,05 считались статистически значимыми. Гетерогенность оценивалась с использованием I2 и Cochrane’s q. Протокол исследования зарегистрирован в базе данных PROSPERO (регистрационный номер: CRD42022290334).
Полученные результаты
Поиск дал 1295 результатов. Для анализа было доступно 34 исследования (Fig. 1).
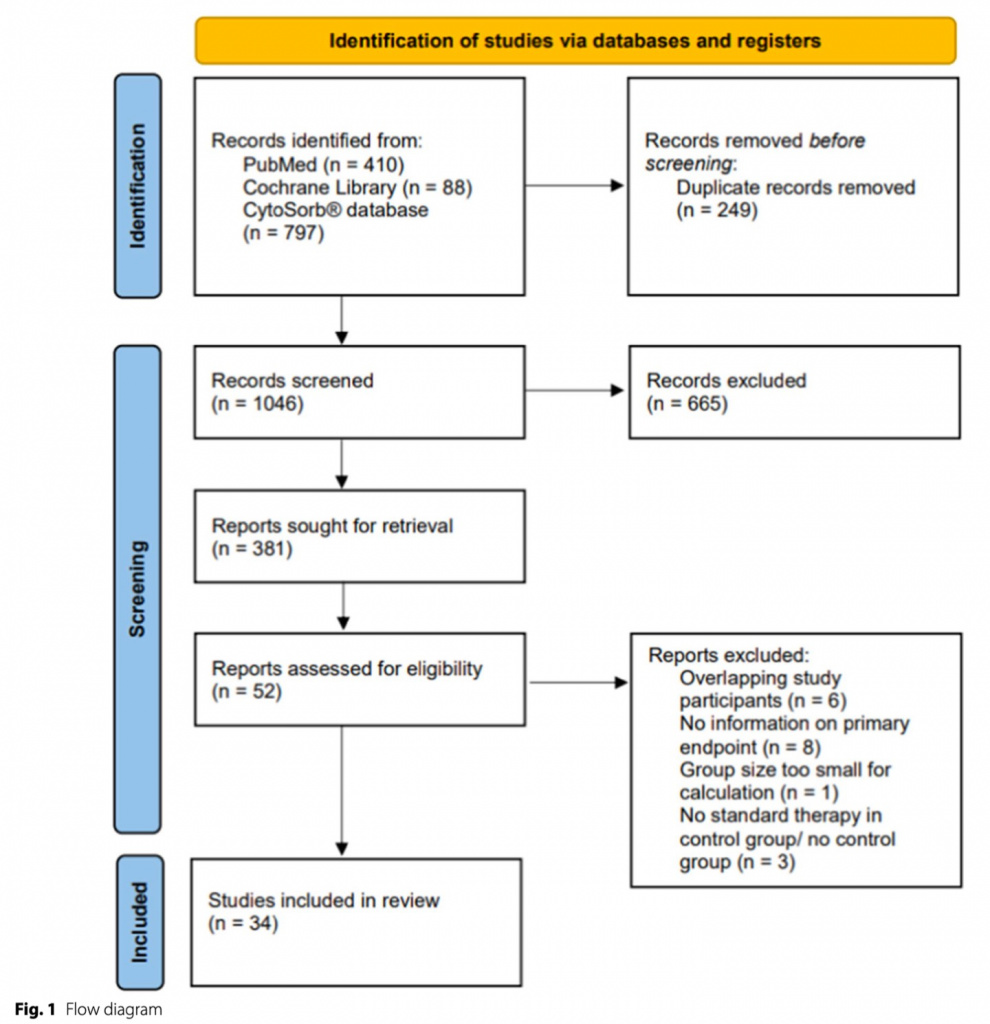
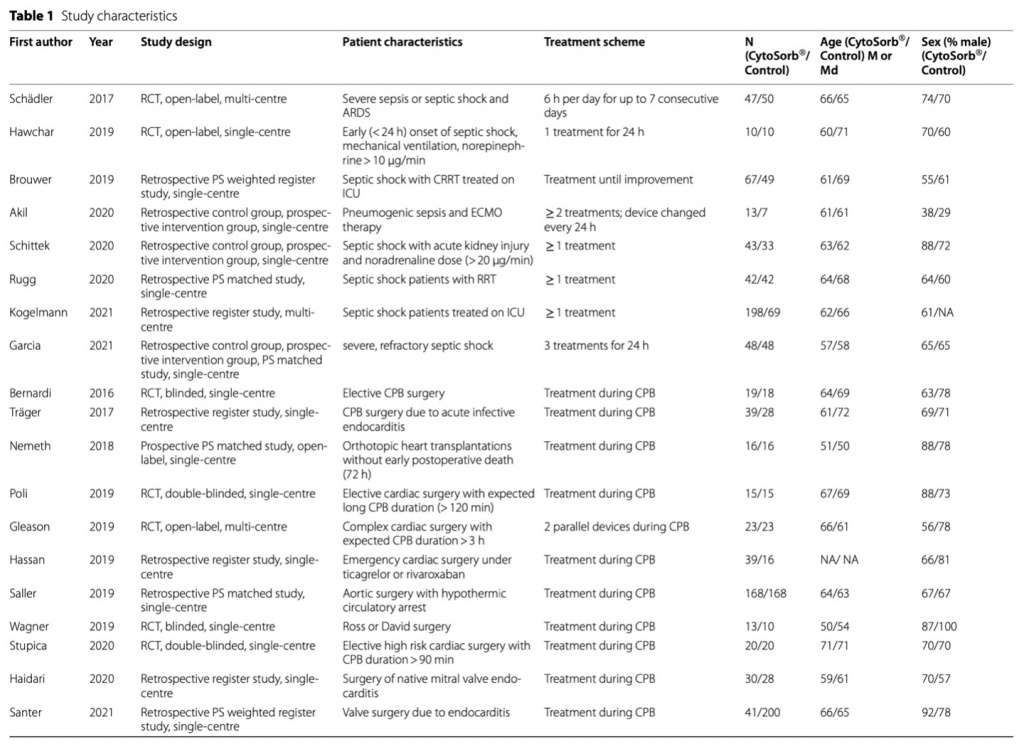
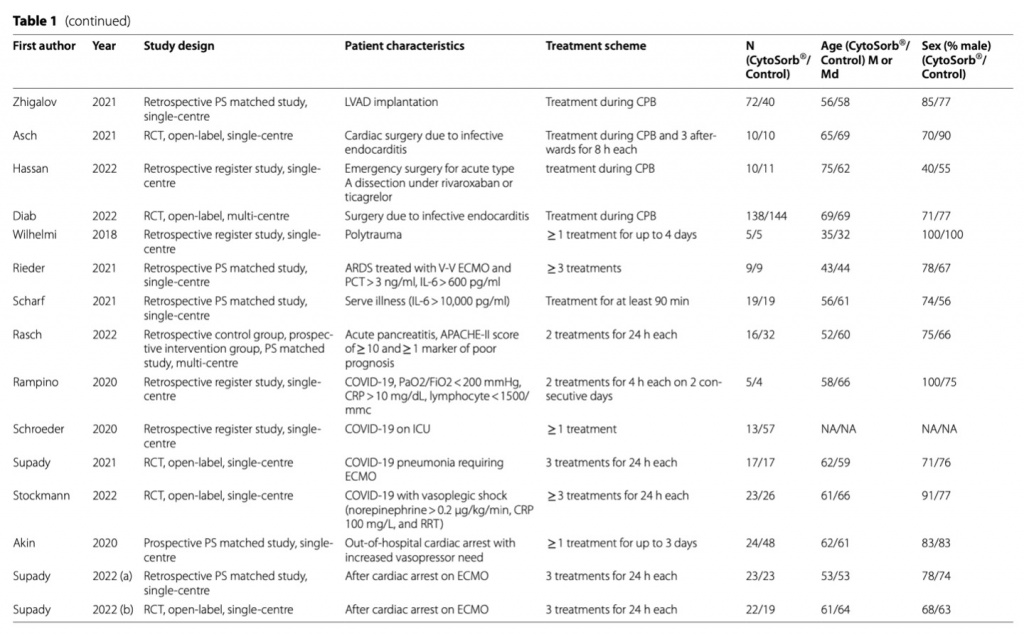
Пациенты детского возраста не были включены, поскольку все исследования с участием детей представляли собой либо сообщения о случаях заболевания, либо не имели контрольной группы. В восьми исследованиях изучалось влияние CytoSorb® на пациентов с сепсисом или септическим шоком [25–32]. В пятнадцати исследованиях его использовали при искусственном кровообращении [33–47]. В четырех исследованиях CytoSorb® применялся у пациентов, страдающих SARS-CoV-2 [48–51]. Еще три исследования использовали CytoSorb® у пациентов после остановки кровообращения [52–54]. Fig. 1. Было проведено еще четыре исследования, в которых изучалось действие CytoSorb®, но их нельзя было отнести ни к одной из ранее упомянутых групп. Мы определили эту группу как «тяжелое заболевание» и включили в нее следующие состояния: пациенты с тяжелыми травмами, пациенты с ОРДС, требующие вено-венозной ЭКМО, тяжелобольные пациенты с уровнем IL-6 ≥ 10 000 пг/мл и пациенты с тяжелым острым панкреатитом [55–58]. Было проведено двенадцать рандомизированных контролируемых исследований (РКИ), двенадцать обсервационных исследований, в которых группы вмешательства и контрольная группы были сопоставлены по показателям склонности (PSM), и десять обсервационных исследований с выбранным иным образом контрольной группой (nPSM) (Table 1). Всего 1297 пациентов получали лечение CytoSorb® по сравнению с 1314 пациентами без CytoSorb®.
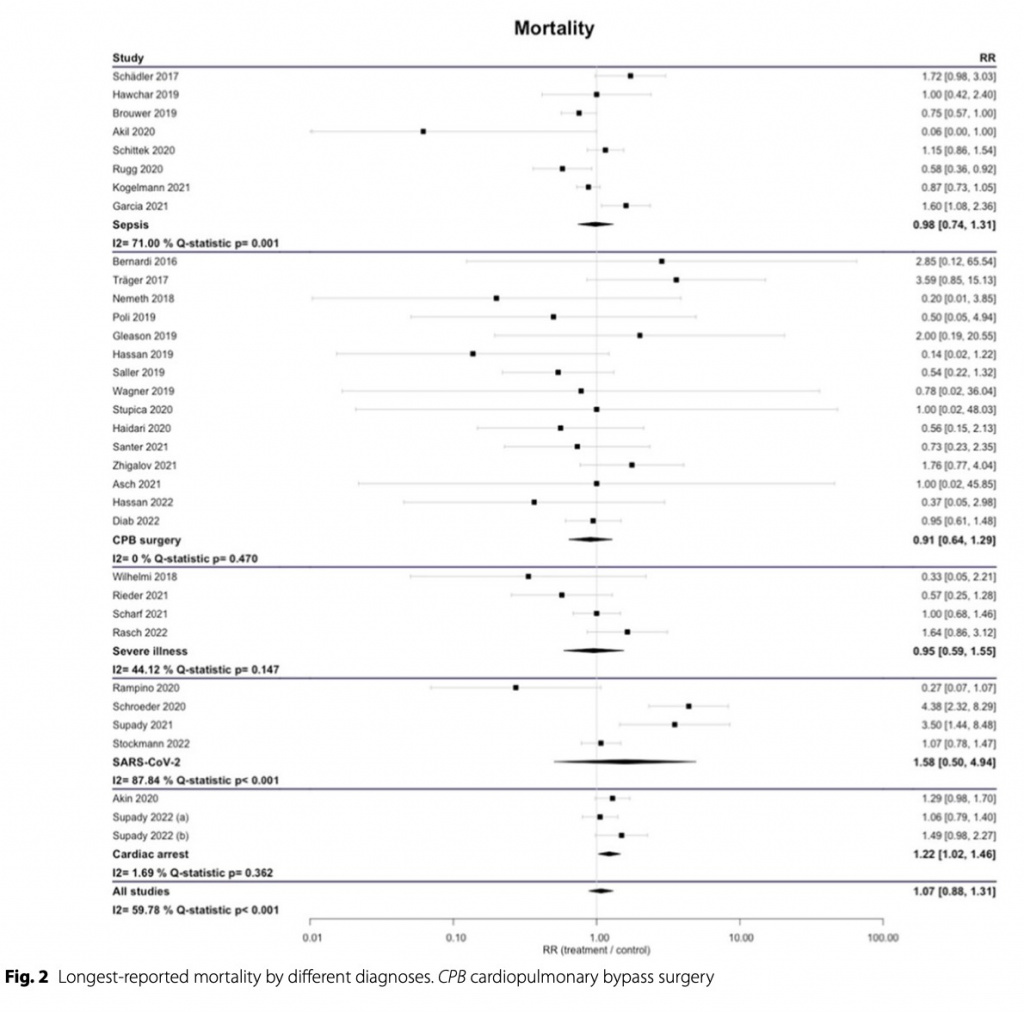
Смертность
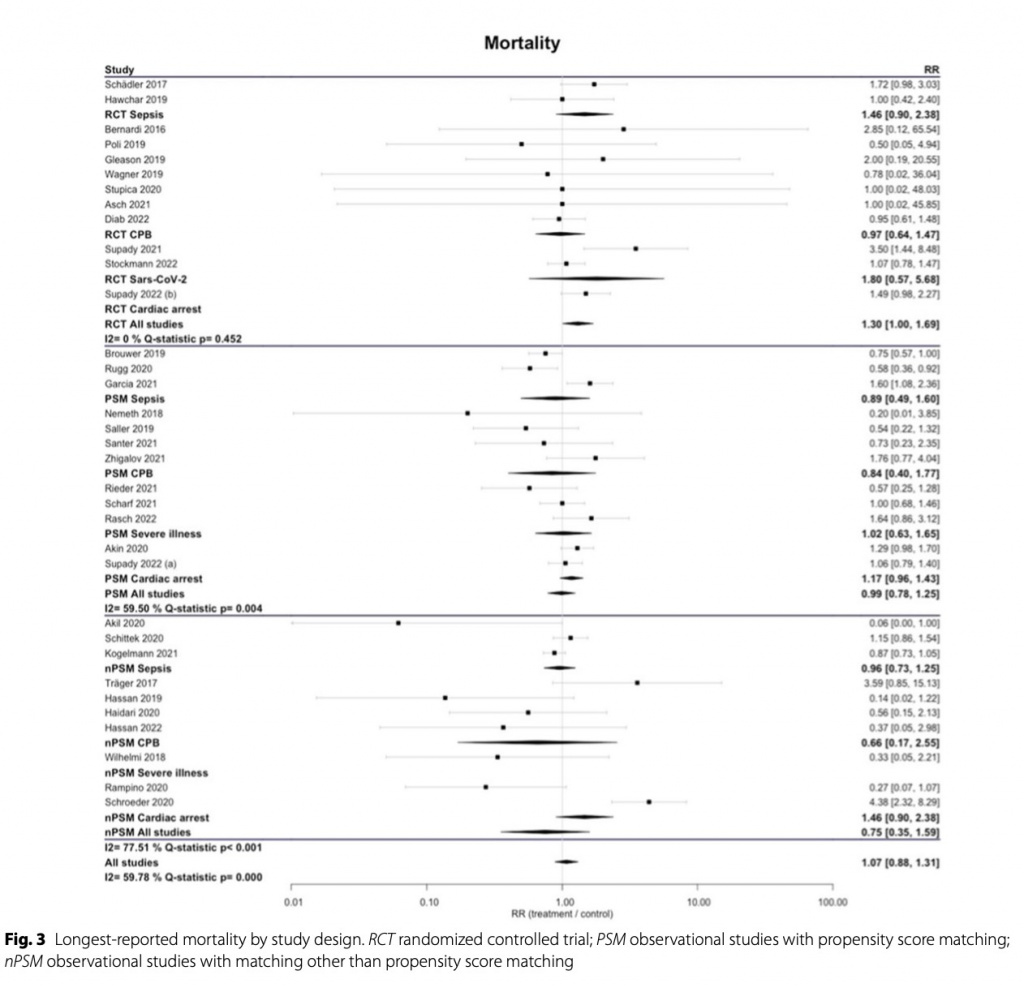
Самая длительная зарегистрированная смертность существенно не отличалась между группами Cytosorb® и контрольной группой во всех исследованиях вместе взятых (RR 1,07 [0,88; 1,31]), а также в подгруппах сепсиса (RR 0,98 [0,74; 1,31]), операции с искусственным кровообращением (RR 0,91 [0,64; 1,31]); 1,29]), тяжелое заболевание (RR 0,95 [0,59; 1,55]) и SARS-CoV-2 (RR 1,58 [0,50; 4,94]). У пациентов с остановкой кровообращения мы обнаружили значительное преимущество в выживаемости по сравнению с контрольной группой, не получавшей лечения (RR 1,22 [1,02; 1,46]) (Fig. 2). Результаты были очень похожими, если оценивать смертность в ОИТ, внутрибольничную или 30-дневную смертность (Additional file 1: Figures S1–S3).
Анализ подгрупп по дизайну исследования показал, что ни в одной из подгрупп, независимо от патологии и качества исследования, не удалось установить значительную разницу в выживаемости. Сравнивая объединенный анализ всех состояний, может сложиться впечатление, что результаты ухудшаются при более высоком качестве дизайна исследования (Fig. 3). В некоторых подгруппах мы обнаружили высокий уровень гетерогенности. РКИ имели значительно меньшую дисперсию между исследованиями (I2 = 0%; Q-statistic p = 0,452), чем наблюдательные исследования (PSM I2 = 59,5%; Q- statistic p = 0,004; nPSM I2 = 77,51%; Q- statistic p < 0,001). ) (Figs. 2, 3).
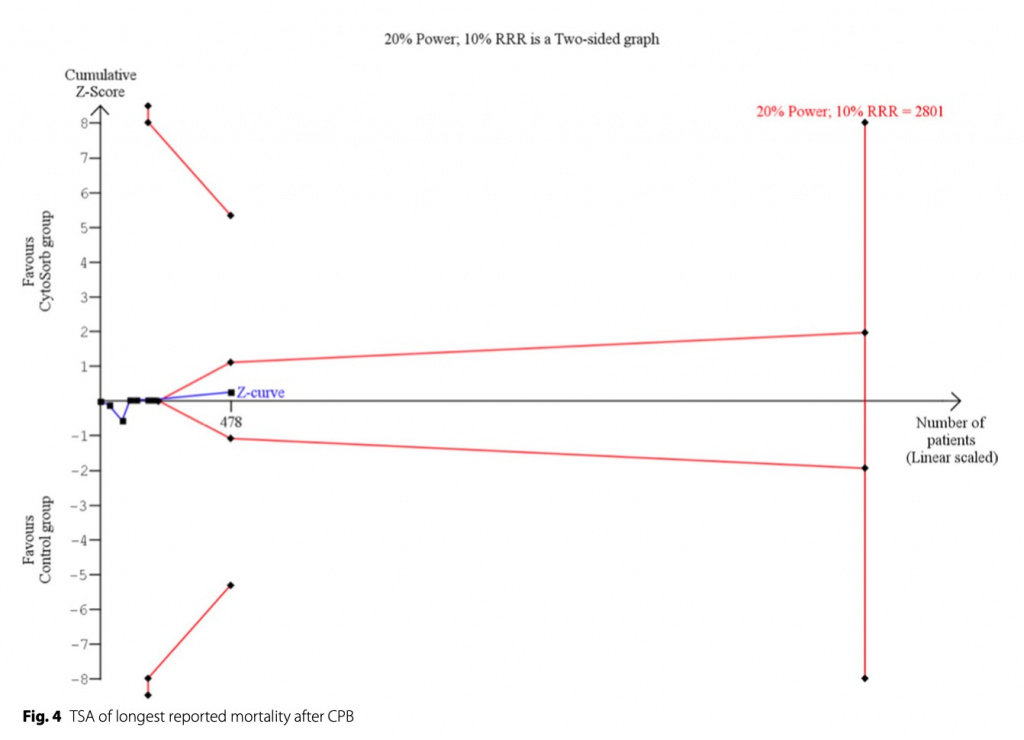
Последовательный анализ
TSA проводился в подгруппе CBP только для первичной конечной точки. На Fig 4 видно, что при фактических 478 пациентах необходимое количество 2801 не достигается. Однако cumulative Z-Score уже находится в области бесполезности, что позволяет предположить, что дополнительные исследования не изменят результат.
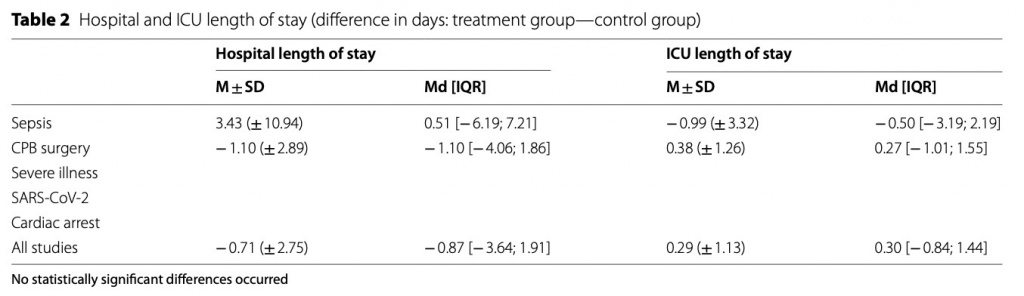
Продолжительность пребывания в ОИТ и стационаре
Продолжительность пребывания в ОИТ существенно не отличалась между CytoSorb® и контрольной группой ни для всех исследований вместе взятых, ни для подгрупп с разными диагнозами. Различия между группами (группа лечения – контрольная группа) сравнивались сначала как средние значения (±SD), а затем как медианные значения [и IQR] (Table 2).
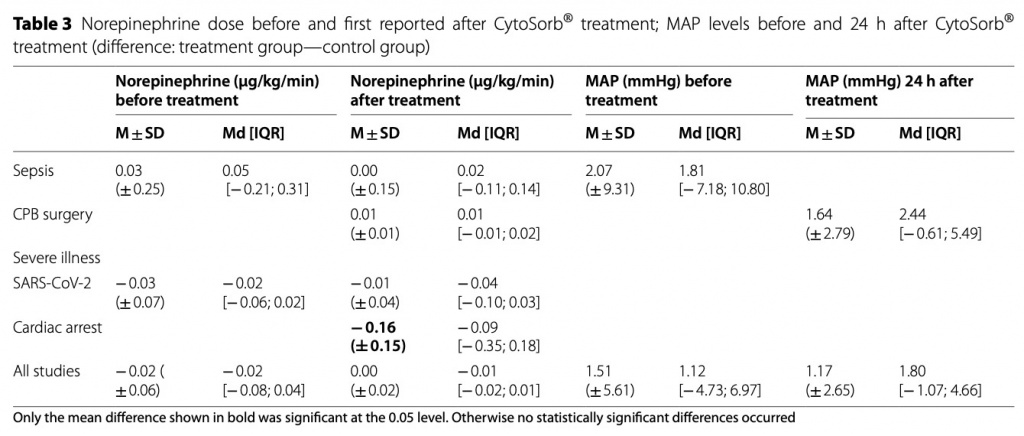
Норадреналин и среднее артериальное давление (САД)
Не было значительной разницы в дозе норадреналина (мкг/кг/мин) или САД на исходном уровне. Пациентам контрольной группы, перенесшим остановку сердца, требовалась значительно более высокая доза норадреналина при сравнении средних значений (-0,16 ( ±0,15). Это наблюдение не могло быть подтверждено при сравнении медиан (- 0,09 ± 0,26)). Все остальные подгруппы не показали существенных различий между CytoSorb® и контрольной группой в дозе норадреналина после начала лечения. Кроме того, не выявлено существенных различий САД через 24 часа после начала лечения (Table 3).
Базовый уровень SOFA, SAPS‑2 и APACHE‑2
Ни один из этих показателей не показал существенных различий между CytoSorb® и контрольными группами на исходном уровне (Additional file 1: Table S1).
Уровни СРБ, ПКТ, лактата и IL-6
Уровни СРБ существенно не отличались ни на исходном уровне, ни при первом измерении после лечения (Additional file 1: Table S2). Уровни ПКТ были значительно выше в контрольной группе у пациентов с сепсисом при учете медианных значений (–7,60 (±7,76) / – 7,13 [– 13,29; – 0,97]). Уровни ПКТ во всех исследованиях вместе взятых и у пациентов с остановкой сердца существенно не различались. Кроме того, после лечения не было выявлено существенных различий в уровнях ПКТ (Additional file 1: Table S2). Не было никаких существенных различий в уровнях лактата на исходном уровне или при первом измерении после начала лечения ни для одной подгруппы (Additional file 1: Table S3). Только в подгруппе «тяжелое заболевание» медианные уровни IL-6 были значительно выше в группе вмешательства, средние значения не показали существенной разницы. После лечения также не было различий в уровнях IL-6 между CytoSorb® и контрольной группой ни в одной подгруппе. (Additional file 1: Table S3).
Неблагоприятные события
Возникновение нежелательных явлений отслеживалось в 22 из 34 исследований. Однако в большинстве исследований не было четко определено, что считать нежелательным явлением. Schädler et al. and Gleason et al. сообщили о снижении количества тромбоцитов, которое они наблюдали в связи с применением CytoSorb® [32, 40]. В других исследованиях также наблюдалось снижение количества тромбоцитов, которое не было связано с специфическое использование адсорбера CytoSorb® и, скорее всего, связано с контактом с экстракорпоральной мембраной в целом [35, 36, 47, 52, 54]. Ни одно из исследований не пришло к выводу, что CytoSorb® опасен.
Риск предвзятости
Риск систематической ошибки оценивался с помощью ROBINSI и RoB 2, а систематической ошибки публикации — с помощью воронкообразных диаграмм. Для оценки достоверности применили методологию GRADE. Некоторые исследования показали значительный риск систематической ошибки (Additional file 1: Figs. S4 and S5). С помощью ROBINS-I все исследования nPSM были оценены как «серьезные риски», поскольку в них не измерялись и не контролировались вмешивающиеся факторы. Кроме того, воронкообразная диаграмма свидетельствует о предвзятом отношении к публикациям в исследованиях nPSM: исследования с отрицательными результатами остались неопубликованными. (Additional file 1: Fig. 6). Напротив, в исследованиях PSM не учитывались искажающие факторы, поэтому большинство исследований PSM были оценены как «умеренный риск». Однако в некоторых исследованиях были исключены некоторые искажающие факторы, которые мы считали значимыми (Nemeth et al. 2018 исключили три значимые исходные характеристики (Heart Failure Score, IMPACT score, and high urgent status) из сопоставления [39]; Rieder et al. [52] не учитывали баллы RESP и PRESERVE при сопоставлении). В целом, воронкообразная диаграмма не свидетельствует о предвзятости публикаций в исследованиях PSM (Additional file 1: Fig. S7). РКИ также вызвали некоторые опасения. В целом оценка риска систематической ошибки проводилась очень строго. Исследования, которые не соответствовали протоколу запланированного лечения, были оценены как «серьезный риск». Аналогичным образом, исследования с выбывшими из них были оценены как «серьезный риск». Если параметр, упомянутый в протоколе исследования, был изменен или не проанализирован без обоснования, это также приводило к присвоению рейтинга «серьезного риска». Тем не менее, мы убеждены, что общее качество РКИ хорошее и нет предвзятости публикации (Additional file 1: Fig. S8).
Обсуждение
Этот метаанализ включает данные 34 исследований, включающих в общей сложности 1297 пациентов, у который использовали CytoSorb®, по сравнению с 1314 контрольными пациентами. Мы не наблюдали значительного снижения смертности благодаря вмешательству CytoSorb®. Использование методов очистки крови при лечении тяжелобольных, страдающих инфекциями, сепсисом и полиорганной недостаточностью, исследуется уже более 30 лет. [59] При цитокиновом шторме массивное высвобождение цитокинов может вызвать тяжелый воспалительный синдром, который приводит к дисфункции органов [60]. Таким образом, удаление провоспалительных цитокинов, таких как IL-1β, IL-6, IL-8 и TNF-α, из кровотока должно сдерживать гиперактивацию иммунной системы и снижать системный ответ. Из этой гипотезы вытекают различные обоснования гемоадсорбции. Удаление одного целевого цитокина в прошлом было безуспешным, поэтому усилия были сосредоточены на неселективном удалении цитокинов с помощью методов очистки крови, таких как гемоперфузия с использованием адсорбирующих систем, таких как CytoSorb® [61, 62].
Применение CytoSorb® и других адсорберов широко распространено, хотя на сегодняшний день нет единого мнения об эффективности лечения. [63, 64] Одним из ограничений нашего метаанализа является неоднородность исследований. Наблюдения отдельных исследований существенно различались, что мы объясняем разными причинами. Во-первых, существует немалое количество исследований с небольшим количеством участников, но с большим эффектом. Восемь исследований включали менее 15 пациентов в каждой группе [26, 28, 39, 45, 46, 51, 56, 58]. Эти исследования достигли больших результатов благодаря использованию CytoSorb®.
Напротив, существуют более крупные РКИ и наблюдательные исследования с сопоставлением показателей склонности (PSM) с заметно меньшим размером эффекта. Во-вторых, использование CytoSorb® во многом отличалось. Количество адсорберов, продолжительность терапии, время от постановки диагноза до первого использования адсорбера и скорость кровотока были очень противоречивыми. В-третьих, сравнивались заболевания, совершенно различающиеся по своей патофизиологии.
По этой причине мы включили анализ подгрупп различных заболеваний. Наконец, дисперсия оказалась довольно большой из-за ненормального распределения некоторых переменных. Мы преодолели это ограничение, проведя анализ подгрупп. Положительного эффекта CytoSorb® мы не обнаружили ни в одной из обследованных подгрупп. Это справедливо для подгрупп различных заболеваний, а также для подгрупп различных типов дизайна исследования.
Мало того, что положительный эффект вмешательства CytoSorb® с точки зрения снижения смертности неясен, даже исследования, изучающие теоретическое обоснование лечения, а именно снижение уровня цитокинов в крови, показывают противоречивые результаты. Было показано, что адсорбер CytoSorb® удаляет IL-1β, IL-6, IL-8 и TNF α в исследованиях in vivo, ex vivo и in vitro [65, 66]. Другие исследования не показали существенного снижения уровня IL-6 [32, 50]. Возможное объяснение стабильного уровня цитокинов, несмотря на их удаление в процессе гемоабсорбции, предложенное Honore et al., заключается в перемещении цитокинов из интерстиция в кровоток [67].
Более того, высвобождение цитокинов происходит непрерывно, поэтому избирательное удаление цитокинов на несколько часов в день может оказаться недостаточным для влияния на успех лечения. Это возможные причины того, почему CytoSorb® не смог снизить смертность. Также утверждается, что некоторые состояния, при которых применяется CytoSorb®, в основном SARS-CoV-2 и операции с использованием искусственного кровообращения, не сопровождаются особенно высокими уровнями цитокинов [32, 50].
Если предположить адекватное удаление провоспалительных цитокинов, то дальнейшим объяснением неспособности снизить смертность с помощью Cytosorb® является неселективное удаление всех гидрофобных компонентов плазмы с молекулярной массой до 55 кДа. Это означает, что также удаляются противовоспалительные медиаторы, гормоны и факторы свертывания крови [68]. Кроме того, Cytosorb® также удаляет антибиотики, что может привести к их субтерапевтическому уровню, что влияет на успех лечения сепсиса и общую выживаемость [69]. Нам срочно нужны данные рандомизированных контролируемых исследований по различным заболеваниям, при которых применяется CytoSorb®. На данный момент только использование при экстракорпоральном кровообращении может быть достаточно оценено, как показал последовательный анализ испытаний.
Заключение
В заключение следует отметить, что нет никаких доказательств снижения смертности при лечении CytoSorb® ни в одном из исследованных состояний. Поэтому мы не можем рекомендовать рутинное использование CytoSorb® пациентам в критическом состоянии, пока не будут получены четкие доказательства. Нам нужны адекватно спланированные РКИ по конкретным медицинским показаниям, нацеленные на нужных пациентов. Следовательно, необходимо провести подготовительную работу для выявления пациентов, которые могут ответить на терапию, например, очень высокие уровни цитокинов и определить оптимальный момент времени для терапии.
Ссылка на документ с дополнительными данными исследования
References
1. Chakraborty RK, Burns B. Systemic inflammatory response syndrome. In:StatPearls. StatPearls Publishing; 2022. Accessed March 7, 2022. http://www. ncbi. nlm. nih. gov/ books/ NBK54 7669/
2. Zhou F, Peng Z, Murugan R, Kellum JA. Blood purification and mortality in sepsis: a meta-analysis of randomized trials*. Crit Care Med. 2013;41(9):2209–20. https:// doi. org/ 10. 1097/ CCM. 0b013 e3182 8cf412.
3. Scharf C, Liebchen U, Paal M, Irlbeck M, Zoller M, Schroeder I. Blood purification with a cytokine adsorber for the elimination of myoglobin in critically ill patients with severe rhabdomyolysis. Crit Care. 2021;25(1):41. https:// doi. org/ 10. 1186/ s13054- 021- 03468-x.
4. Kohler T, Schwier E, Praxenthaler J, Kirchner C, Henzler D, Eickmeyer C. Therapeutic modulation of the host defense by hemoadsorption with CytoSorb®—basics, indications and perspectives—a scoping review. Int J Mol Sci. 2021;22(23):12786. https:// doi. org/ 10. 3390/ ijms2 22312 786.
5. McGrath S, Sohn H, Steele R, Benedetti A. Meta-analysis of the difference of medians. Biom J. 2020;62(1):69–98. https:// doi. org/ 10. 1002/ bimj. 201900036.
6. Luo D, Wan X, Liu J, Tong T. Optimally estimating the sample mean from the sample size, median, mid-range, and/or mid-quartile range. Stat Methods Med Res. 2018;27(6):1785–805. https:// doi. org/ 10. 1177/ 0962280216 669183.
7. Thorlund K, Engstrom J, Wetterslev J, Brok J, Imberger G, Gluud C (2017). User Manual for Trial Sequential Analysis (TSA) [Pdf ]. 2nd Ed. Copenhagen: Copenhagen Trial Unit, pp. 1–119. Downloadable from Ctu.Dk/Tsa. Accessed on: 05.03.2023 Online.
8. Poli E. Effect of cytoadsorbant device on post-cardio-pulmonary bypass inflammation in ESICM LIVES 2018: Effect of cytoadsorbant device on post-cardio-pulmonary bypass inflammation in ESICM LIVES 2018. Intensive Care Med Exp. 2018;6(S2):40. https:// doi. org/ 10. 1186/s40635- 018- 0201-6.
9. Laszlo I, Von Seth M, Hillered L, et al. Effects of adsorption of cytokines early in septic shock (the ‘ACESS-trial’)—results of the pilot study in 37th International Symposium on Intensive Care and Emergency Medicine (part 3 of 3): Brussels, Belgium. 21–24 March 2017. Crit Care.
2017;21(S1):58. https:// doi. org/ 10. 1186/ s13054- 017- 1629-x.
10. Brouwer WP, Duran S, Ince C. Improved survival beyond 28 days up to 1 year after CytoSorb treatment for refractory septic shock: a propensity weighted retrospective survival analysis. Blood Purif. 2021;50(4–5):539–45. https:// doi. org/ 10. 1159/ 00051 2309.
11. Woitsch S. Verbesserung der intrakraniellen Sauerstoffversorgung wahrend Operationen im tiefen hypothermen Kreislaufstillstand mit Hamoadsorption. 2018;(Der Hauptstadtkongress der DGAI fur Anasthesiologie und Intensivtherapie mit Pfl egesymposium und Rettungsdienstforum).
12. Schadler D, Porzelius C, Jorres A, et al. A multicenter randomized controlled study of an extracorporeal cytokine hemoadsorption device in septic patients. Crit Care. 2013;17(S2):P62. https:// doi. org/ 10. 1186/ cc120 00.
13. Schittek G. Beeinflussung des intensivstationaren Therapieverlaufs durch die Einfuhrung der Absorptionstherapie bei Patienten mit septischen Schock und akuten Nierenversagen. Published online 2018.
14. Born, F. Systemic Inflammatory Response Syndrome in der Herzchirurgie_Kardiotechnik 02–2014 - English Translation.pdf. Published online February 2014. http:// armag hansa lamat. com/ media/ brands/ Cytos orben ts/ Liter ature/ 2014_ Born% 20F% 20et% 20al. ,% 20Sys temic% 20Inflamma tory% 20Res ponse% 20Syn drome% 20in% 20der% 20Her zchir urgie_ Kardi otech nik% 2002- 2014% 20-% 20Eng lish% 20Tra nslat ion. pdf
15. Gliga S, Orth HM, Lubke N, Timm J, Luedde T, Jensen BEO. Multicentric Castleman’s disease in HIV patients: a single-center cohort diagnosed from 2008 to 2018. Infection. 2021;49(5):945–51. https:// doi. org/ 10. 1007/s15010- 021- 01618-5.
16. Mehta Y, Singh A, Singh A, Gupta A, Bhan A. Modulating the inflammatory response with hemadsorption (CytoSorb) in patients undergoing major aortic surgery. J Cardiothorac Vasc Anesth. 2021;35(2):673–5. https:// doi. org/ 10. 1053/j. jvca. 2020. 06. 028.
17. Lebreton G, Dorgham K, Quentric P, Combes A, Gorochov G, Schmidt M. Longitudinal cytokine profiling in patients with severe COVID-19 on extracorporeal membrane oxygenation and hemoadsorption. Am J Respir Crit Care Med. 2021;203(11):1433–5. https:// doi. org/ 10. 1164/ rccm.202011- 4140LE.
18. Lewis TC, Merchan C, Toy B, et al. Impact of CytoSorb hemoadsorption on sedation requirements in patients with severe COVID-19 on venovenous extracorporeal membrane oxygenation. ASAIO J. 2021;67(8):856–61. https:// doi. org/ 10. 1097/ MAT. 00000 00000 001513.
19. Garau I, Marz A, Sehner S, et al. Hemadsorption during cardiopulmonary bypass reduces interleukin 8 and tumor necrosis factor α serum levels in cardiac surgery: a randomized controlled trial. Minerva Anestesiol. 2019.https:// doi. org/ 10. 23736/ S0375- 9393. 18. 12898-7.
20. Bok S. CytoSorb: what is the effect on the circulation? in ESICM LIVES 2017: 30th ESICM Annual Congress September 23–27, 2017. Intensive Care Med Exp. 2017;5(S2):44. https:// doi. org/ 10. 1186/ s40635- 017- 0151-4.
21. Laubach CM. Cytokine and DAMP adsorption in septic acute kidney injury in ESICM LIVES 2018: Paris, France. 20-24 October 2018. Intensive Care Med Exp. 2018;6(S2):40. https:// doi. org/ 10. 1186/ s40635- 018- 0201-6.
22. Bottari G, Lorenzetti G, Severini F, Cappoli A, Cecchetti C, Guzzo I. Role of hemoperfusion with CytoSorb associated with continuous kidney replacement therapy on renal outcome in critically III children with septic shock. Front Pediatr. 2021;9:718049. https:// doi. org/ 10. 3389/ fped. 2021.718049.
23. Berlot G, Pintacuda S, Moro E, et al. Effects of tocilizumab versus hemoadsorption
combined with tocilizumab in patients with SARS-CoV-2 pneumonia: preliminary results. Int J Artif Organs. 2022;45(1):75–80. https:// doi. org/ 10. 1177/ 03913 98821 989334.
24. Bottari G, Murciano M, Merli P, et al. Hemoperfusion with CytoSorb to manage multiorgan dysfunction in the spectrum of hemophagocytic lymphohistiocytosis syndrome in critically Ill children. Blood Purif. 2022;51(5):417–24. https:// doi. org/ 10. 1159/ 00051 7471.
25. Schittek GA, Zoidl P, Eichinger M, et al. Adsorption therapy in critically ill with septic shock and acute kidney injury: a retrospective and prospective cohort study. Ann Intensive Care. 2020;10(1):154. https:// doi. org/ 10.1186/ s13613- 020- 00772-7.
26. Akil A, Ziegeler S, Reichelt J, et al. Combined use of CytoSorb and ECMO in patients with severe pneumogenic sepsis. Thorac Cardiovasc Surg. 2021;69(03):246–51. https:// doi. org/ 10. 1055/s- 0040- 17084 79.
27. Wendel Garcia PD, Hilty MP, Held U, Kleinert EM, Maggiorini M. Cytokine adsorption in severe, refractory septic shock. Intensive Care Med. 2021;47(11):1334–6. https:// doi. org/ 10. 1007/ s00134- 021- 06512-0.
28. Hawchar F, Laszlo I, Oveges N, Trasy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: a proof of concept randomized, controlled pilot study. J Crit Care. 2019;49:172–8. https:// doi. org/ 10. 1016/j.jcrc. 2018. 11. 003.
29. Kogelmann K, Hubner T, Schwameis F, Druner M, Scheller M, Jarczak D.First evaluation of a new dynamic scoring system intended to support prescription of adjuvant CytoSorb hemoadsorption therapy in patients with septic shock. J Clin Med. 2021;10(13):2939. https:// doi. org/ 10. 3390/jcm10 132939.
30. Rugg C, Klose R, Hornung R, et al. Hemoadsorption with CytoSorb in septic shock reduces catecholamine requirements and in-hospital mortality: a single-center retrospective ‘Genetic’ matched analysis. Biomedicines.2020;8(12):539. https:// doi. org/ 10. 3390/ biome dicin es812 0539.
31. Brouwer WP, Duran S, Kuijper M, Ince C. Hemoadsorption with CytoSorb shows a decreased observed versus expected 28-day all-cause mortality in ICU patients with septic shock: a propensity-score-weighted retrospective study. Crit Care. 2019;23(1):317. https:// doi. org/ 10. 1186/s13054- 019- 2588-1.
32. Schadler D, Pausch C, Heise D, et al. The effect of a novel extracorporeal cytokine hemoadsorption device on IL-6 elimination in septic patients: A randomized controlled trial. Eller K, ed. PLOS ONE. 2017;12(10):e0187015.https:// doi. org/ 10. 1371/ journ al. pone. 01870 15
33. Poli EC, Alberio L, Bauer-Doerries A, et al. Cytokine clearance with CytoSorb® during cardiac surgery: a pilot randomized controlled trial. Crit Care. 2019;23(1):108. https:// doi. org/ 10. 1186/ s13054- 019- 2399-4.
34. Hassan K, Kannmacher J, Wohlmuth P, Budde U, Schmoeckel M, Geidel S. Cytosorb adsorption during emergency cardiac operations in patients at high risk of bleeding. Ann Thorac Surg. 2019;108(1):45–51. https:// doi.org/ 10. 1016/j. athor acsur. 2018. 12. 032.
35. Bernardi MH, Rinoesl H, Dragosits K, et al. Effect of hemoadsorption during cardiopulmonary bypass surgery—a blinded, randomized, controlled pilot study using a novel adsorbent. Crit Care. 2016;20(1):96. https:// doi. org/ 10. 1186/ s13054- 016- 1270-0.
36. Taleska Stupica G, Sostaric M, Bozhinovska M, et al. Extracorporeal hemadsorption versus glucocorticoids during cardiopulmonary bypass: a prospective, randomized. Controlled Trial Cardiovasc Ther. 2020;2020:1–15. https:// doi. org/ 10. 1155/ 2020/ 78341 73.
37. Saller T, Hagl C, Woitsch S, et al. Haemadsorption improves intraoperative haemodynamics and metabolic changes during aortic surgery with hypothermic circulatory arrest. Eur J Cardiothorac Surg. 2019;56(4):731–7. https:// doi. org/ 10. 1093/ ejcts/ ezz074.
38. Santer D, Miazza J, Koechlin L, et al. Hemoadsorption during cardiopulmonary bypass in patients with endocarditis undergoing valve surgery: a retrospective single-center study. J Clin Med. 2021;10(4):564. https:// doi.org/ 10. 3390/ jcm10 040564.
39. Hassan K, Bruning T, Caspary M, et al. Hemoadsorption of rivaroxaban and ticagrelor during acute type A aortic dissection operations. Ann Thorac Cardiovasc Surg. 2022. https:// doi. org/ 10. 5761/ atcs. oa. 21- 00154.
40. Gleason TG, Argenziano M, Bavaria JE, et al. Hemoadsorption to reduce plasma-free hemoglobin during cardiac surgery: results of REFRESH I pilot study. Semin Thorac Cardiovasc Surg. 2019;31(4):783–93. https:// doi. org/10. 1053/j. semtc vs. 2019. 05. 006.
41. Trager K, Skrabal C, Fischer G, et al. Hemoadsorption treatment of patients with acute infective endocarditis during surgery with cardiopulmonary bypass—a case series. Int J Artif Organs. 2017;40(5):240–9. https:// doi. org/ 10. 5301/ ijao. 50005 83.
42. Nemeth E, Kovacs E, Racz K, et al. Impact of intraoperative cytokine adsorption on outcome of patients undergoing orthotopic heart transplantation-an observational study. Clin Transplant. 2018;32(4):e13211. https:// doi. org/ 10. 1111/ ctr. 13211.
43. Zhigalov K, Van den Eynde J, Zubarevich A, et al. Initial experience with CytoSorb therapy in patients receiving left ventricular assist devices. Artif Organs. 2022;46(1):95–105. https:// doi. org/ 10. 1111/ aor. 14099.
44. Haidari Z, Wendt D, Thielmann M, et al. Intraoperative hemoadsorption in patients with native mitral valve infective endocarditis. Ann Thorac Surg. 2020;110(3):890–6. https:// doi. org/ 10. 1016/j. athor acsur. 2019. 12. 067.
45. Wagner R, Soucek P, Ondrasek J, et al. Plasma levels of myocardial Micro-RNA-133a increase by intraoperative cytokine hemoadsorption in the complex cardiovascular operation. J Clin Med Res. 2019;11(12):789–97. https:// doi. org/ 10. 14740/ jocmr 3989.
46. Asch S, Kaufmann TP, Walter M, et al. The effect of perioperative hemadsorption in patients operated for acute infective endocarditis—a randomized controlled study. Artif Organs. 2021;45(11):1328–37. https://doi. org/ 10. 1111/ aor. 14019.
47. Diab M, Lehmann T, Bothe W, et al. Cytokine hemoadsorption during cardiac surgery versus standard surgical care for infective endocarditis (REMOVE): results from a multicenter randomized controlled trial. Circulation.2022;145(13):959–68. https:// doi. org/ 10. 1161/ CIRCU LATIO NAHA.121. 056940.
48. Schroeder I, Scharf C, Zoller M, et al. Charakteristika und Outcome von 70 beatmeten COVID-19-Patienten: Bilanz nach der ersten Welle an einem universitaren Zentrum. Anaesthesist. 2021;70(7):573–81. https:// doi. org/10. 1007/ s00101- 020- 00906-3.
49. Supady A, Weber E, Rieder M, et al. Cytokine adsorption in patients with severe COVID-19 pneumonia requiring extracorporeal membrane oxygenation (CYCOV): a single centre, open-label, randomised, controlled trial. Lancet Respir Med. 2021;9(7):755–62. https:// doi. org/ 10. 1016/ S2213-2600(21) 00177-6.
50. Stockmann H, Thelen P, Stroben F, et al. CytoSorb rescue for COVID-19 patients with vasoplegic shock and multiple organ failure: a prospective, open-label, randomized controlled pilot study. Crit Care Med. 2022.https:// doi. org/ 10. 1097/ CCM. 00000 00000 005493.
51. Rampino T, Gregorini M, Perotti L, et al. Hemoperfusion with CytoSorb as adjuvant therapy in critically Ill patients with SARS-CoV2 pneumonia. Blood Purif. 2021;50(4–5):566–71. https:// doi. org/ 10. 1159/ 00051 1725.
52. Supady A, Zahn T, Kuhl M, et al. Cytokine adsorption in patients with post-cardiac arrest syndrome after extracorporeal cardiopulmonary resuscitation (CYTER)—a single-centre, open-label, randomised, controlled trial. Resuscitation. 2022. https:// doi. org/ 10. 1016/j. resus citat ion.2022. 02. 001.
53. Akin M, Garcheva V, Sieweke JT, et al. Early use of hemoadsorption in patients after out-of hospital cardiac arrest—a matched pair analysis. Ballotta A, ed. PLOS ONE. 2020;15(11):e0241709. https:// doi. org/ 10. 1371/journ al. pone. 02417 09
54. Supady A, Zahn T, Rieder M, et al. Effect of cytokine adsorption on survival and circulatory stabilization in patients receiving extracorporeal cardiopulmonary resuscitation. ASAIO J. 2021. https:// doi. org/ 10. 1097/MAT. 00000 00000 001441.
55. Scharf C, Schroeder I, Paal M, et al. Can the cytokine adsorber CytoSorb® help to mitigate cytokine storm and reduce mortality in critically ill patients? A propensity score matching analysis. Ann Intensive Care. 2021;11(1):115. https:// doi. org/ 10. 1186/ s13613- 021- 00905-6.
56. Rieder M, Duerschmied D, Zahn T, et al. Cytokine adsorption in severe acute respiratory failure requiring veno-venous extracorporeal membrane oxygenation. ASAIO J. 2021;67(3):332–8. https:// doi. org/ 10. 1097/MAT. 00000 00000 001302.
57. Rasch S, Sancak S, Erber J, et al. Influence of extracorporeal cytokine adsorption on hemodynamics in severe acute pancreatitis: results of the matched cohort pancreatitis cytosorbents inflammatory cytokine removal (PACIFIC) study. Artif Organs. 2022. https:// doi. org/ 10. 1111/ aor.14195.
58. Wilhelmi M. Pilotstudie zur Outcome-Analyse bei Einsatz einer Cytokin-Hamoadsorption bei schwerstverletzten Polytraumapatienten. Published online 2018. https:// cytos orb- thera py. com/ wp- conte nt/ uploa ds/ 2018/12/ 2018_ Wilhe lmi_ Polyt rauma_ DIVI_ Poste r1. pdf
59. Barzilay E, Kessler D, Berlot G, Gullo A, Geber D, Ben ZI. Use of extracorporeal supportive techniques as additional treatment for septic-induced multiple organ failure patients. Crit Care Med. 1989;17(7):634–7. https://doi. org/ 10. 1097/ 00003 246- 19890 7000- 00007.
60. Fajgenbaum DC, June CH. Cytokine storm. N Engl J Med. 2020;383(23):2255–73. https:// doi. org/ 10. 1056/ NEJMr a2026 131.
61. Deans KJ, Haley M, Natanson C, Eichacker PQ, Minneci PC. Novel therapies for sepsis: a review. J Trauma. 2005;58(4):867–74. https:// doi. org/ 10.1097/ 01. ta. 00001 58244. 69179. 94.
62. Rimmele T, Kellum JA. Clinical review: blood purification for sepsis. Crit Care Lond Engl. 2011;15(1):205. https:// doi. org/ 10. 1186/ cc9411.
63. Ricci Z, Romagnoli S, Reis T, Bellomo R, Ronco C. Hemoperfusion in the intensive care unit. Intensive Care Med. 2022;48(10):1397–408. https:// doi.org/ 10. 1007/ s00134- 022- 06810-1.
64. Kielstein JT, Zarbock A. Is this the beginning of the end of cytokine adsorption? Crit Care Med. 2022;50(6):1026–9. https:// doi. org/ 10. 1097/CCM. 00000 00000 005509.
65. Kellum JA, Song M, Venkataraman R. Hemoadsorption removes tumor necrosis factor, interleukin-6, and interleukin-10, reduces nuclear factor-kappaB DNA binding, and improves short-term survival in lethal endotoxemia. Crit Care Med. 2004;32(3):801–5. https:// doi. org/ 10. 1097/ 01. ccm.00001 14997. 39857. 69.
66. Harm S, Schildbock C, Hartmann J. Cytokine removal in extracorporeal blood purification: an in vitro study. Blood Purif. 2020;49(1–2):33–43. https:// doi. org/ 10. 1159/ 00050 2680.
67. Honore PM, Matson JR. Extracorporeal removal for sepsis: acting at the tissue level–the beginning of a new era for this treatment modality in septic shock. Crit Care Med. 2004;32(3):896–7. https:// doi. org/ 10. 1097/ 01.
ccm. 00001 15262. 31804. 46.
68. Harm S, Falkenhagen D, Hartmann J. Pore size–a key property for selective toxin removal in blood purification. Int J Artif Organs. 2014;37(9):668–78. https:// doi. org/ 10. 5301/ ijao. 50003 54.
69. Konig C, Rohr AC, Frey OR, et al. In vitro removal of anti-infective agents by a novel cytokine adsorbent system. Int J Artif Organs. 2019;42(2):57–64. https:// doi. org/ 10. 1177/ 03913 98818 812601.
[~DETAIL_TEXT] =>
S Becker, H Lang, C V Barbosa, Z Tian, A Melk, B Schmidt
Efficacy of CytoSorb
®: asystematic review and meta-analysis
Critical Care (2023) 27:215 doi.org/10.1186/s13054-023-04492-9
Абстракт
Адсорбция цитокинов с использованием адсорбера CytoSorb® была предложена при различных клинических ситуациях, включая сепсис, ОРДС, гипервоспалительные синдромы, операции на сердце или восстановление после остановки кровообращения. Целью данного анализа является предоставление доказательств эффективности адсорбера CytoSorb® в отношении смертности в различных условиях. Провели поиск в базе данных PubMed, Cochrane Library и в базе данных Cytosorbents™ (01.1.2010–29.5.2022) и рассмотрели рандомизированные контролируемые исследования и наблюдательные исследования с контрольными группами. Самая поздняя зарегистрированная смертность была определена как первичная конечная точка. Мы рассчитали коэффициенты риска и 95%-ные доверительные интервалы и использовали модель случайных эффектов DerSimonian and Lairds. Проанализировали все исследования вместе и разделили их на подгруппы: сепсис, искусственное кровообращение (CPB), другие тяжелые заболевания, инфекция SARS-CoV-2 и восстановление после остановки сердца. Метаанализ был зарегистрирован заранее (PROSPERO: CRD42022290334). Из первоначальных 1295 публикаций были признаны подходящими 34 исследования, которые включали 1297 пациентов с использованием CytoSorb®, и 1314 пациентов контрольной группы. Вмешательство Cytosorb® не снизило смертность (RR [95%-ДИ]: все исследования 1,07 [0,88; 1,31], сепсис 0,98 [0,74; 1,31], операция искусственного кровообращения 0,91 [0,64; 1,29], другие тяжелые заболевания 0,95 [0,59; 1,55] , SARS-CoV-2 1,58 [0,50; 4,94]). У пациентов с остановкой сердца мы обнаружили значительное преимущество в выживаемости по сравнению с контрольной группой, не получавшей лечения (1,22 [1,02; 1,46]). Мы не обнаружили существенных различий в продолжительности пребывания в ОИТ, уровнях лактата или IL-6 после лечения. Из 34 исследований, отвечающих критериям отбора, только 12 были рандомизированными контролируемыми исследованиями. Все наблюдательные исследования показали риск систематической ошибки от умеренного до серьезного. На сегодняшний день нет доказательств положительного влияния адсорбера CytoSorb® на смертность при различных заболеваниях, что оправдывало бы его широкое использование в интенсивной терапии.
Введение
Массивный выброс цитокинов в кровь является патофизиологическим триггером многих опасных для жизни заболеваний. Провоспалительные цитокины приводят к вазодилатации, капиллярной утечке и коагулопатии. Противовоспалительные цитокины могут вызывать относительную иммуносупрессию, приводящую к вторичным нозокомиальным инфекциям. Неконтролируемый выброс обоих типов цитокинов может привести к развитию мультиорганной недостаточности [1]. Для неселективного снижения уровня цитокинов были предложены различные методы очистки крови, такие как диализ с использованием мембран с высокой точкой отсечки, гемосорбция, высокообъемная гемофильтрация и плазмообмен [2]. CytoSorb® - одно из наиболее широко используемых устройств для очистки крови, которое способно снижать уровень гидрофобных молекул с молекулярной массой до 55 кДа. [3] Таким образом, устройство адсорбирует цитокины, желчные кислоты и миоглобин. CytoSorb® находит клиническое применение у пациентов с избыточным иммунным ответом, например при сепсисе, ОРДС, SARS-CoV-2 инфекции, гиперинтенсивных воспалительных синдромах, а также во время и после кардиохирургических операций с использованием экстракорпорального кровообращения (CPB). Кроме того, CytoSorb® может быть полезен при печеночной недостаточности, для элиминации пероральных антикоагулянтов прямого действия (DOACs) или некоторых острых интоксикациях [4]. Устройство считается безопасным и хорошо переносится. Однако единого мнения по поводу эффективности нет. Целью этого систематического обзора и метаанализа является оценка влияния CytoSorb® на все ранее описанные заболевания. Первичной конечной точкой является самая поздняя зарегистрированная смертность. Кроме того, будут сравниваться продолжительность пребывания в отделении интенсивной терапии, потребности в норэпинефрине, уровни IL-6 и лактата.
Методы
Повели систематический поиск в базе данных PubMed и Cochrane Library, используя «CytoSorb» в качестве ключевого слова. Проверена база данных CytoSorbents https://literature.cytosorb-herapy.com/?_ga=2.58770730.642024760.1646225438-7175153.1645687922). Последнее обновление проведено 29 мая 2022 года. Исследования были выбраны двумя исследователями независимо; в случае разногласий искался консенсус. В соответствии с рекомендациями группы Bias Method Group Кокрейновской сети качество исследований оценивалось с помощью ROBINS-I (Risk of Bias in Non-randomized Studies of Interventions) или инструмента RoB 2 (revised tool for Risk of Bias in randomized trials). Данные были собраны двумя исследователями независимо и обобщены в файле Excel. Если вместо точных значений предоставлялись графики, мы анализировали данные с помощью «WebPlotDigitizer» (https://apps.automeris.io/wpd/). Первичной конечной точкой была самая поздняя зарегистрированная смертность (30-дневная смертность в стационаре или ОИТ). Если было представлено более одного значения, выбиралось значение с самым длительным периодом наблюдения. Первичная конечная точка рассчитывалась как относительный риск. Анализ подгрупп первичной конечной точки проводился для различных заболеваний (сепсис, искусственное кровообращение, тяжелое заболевание, SARS-CoV-2 и остановка сердца). Также был проведен анализ подгрупп для различных дизайнов исследований (рандомизированные контролируемые исследования по сравнению с наблюдательными исследованиями с соответствующими контрольными показателями по показателю предрасположенности и без них).
Для вычисления использовалась модель случайных эффектов (DerSimonian and Laird). Вторичными конечными точками были продолжительность пребывания в ОИТ и стационаре. Мы извлекли информацию о дозе норэпинефрина, среднем артериальном давлении (САД), СРБ, ПКТ, уровни лактата и интерлейкина-6 (IL-6) до и после использования CytoSorb®. Уровни маркеров воспаления после CytoSorb® определялись как первое зарегистрированное значение после начала лечения CytoSorb®. Кроме того, мы оценили показатели SOFA, SAPS-2 и APACHE-2, чтобы сравнить контрольную группу и группу вмешательства. Также проверили все исследования на предмет сообщений о нежелательных явлениях. Вторичные конечные точки были представлены в виде разницы рисков (группа лечения и группа контроля) для всех исследований в совокупности и для отдельных подгрупп. Анализ вторичных конечных точек проводился, если по крайней мере в двух исследованиях сообщалось о соответствующих данных. Для плановых операций с использованием экстракорпорального кровообращения показатели сепсиса и физиологические конечные точки не применялись. В оригинальных исследованиях вторичные конечные точки чаще всего сообщались в виде средних или медианных значений. Мы следовали рекомендациям McGrath et al [5]: при нормальном распределении средние значения считались равными медианам. Медианы с интерквартильным размахом или минимальными и максимальными значения были преобразованы в средние значения и стандартное отклонение по методу Luo et al. [6]. Впоследствии влияние средних значений оценивали с использованием модели случайного эффекта с использованием метода DerSimonian-Laird. Влияние медианных значений рассчитывали методом квантильной оценки. Риск систематической ошибки оценивался с помощью ROBINSI и RoB 2 двумя исследователями независимо. Мы использовали воронкообразные графики для оценки систематической ошибки публикации и применили методологию GRADE для оценки достоверности. Для всех анализов мы использовали R 4.1.0 с пакетами meta, metafor, metamedian, lqmm, hmisc, estmeansd, Forestplot и writexl. Значения P < 0,05 считались статистически значимыми. Гетерогенность оценивалась с использованием I2 и Cochrane’s q. Протокол исследования зарегистрирован в базе данных PROSPERO (регистрационный номер: CRD42022290334).
Полученные результаты
Поиск дал 1295 результатов. Для анализа было доступно 34 исследования (Fig. 1).

Пациенты детского возраста не были включены, поскольку все исследования с участием детей представляли собой либо сообщения о случаях заболевания, либо не имели контрольной группы. В восьми исследованиях изучалось влияние CytoSorb® на пациентов с сепсисом или септическим шоком [25–32]. В пятнадцати исследованиях его использовали при искусственном кровообращении [33–47]. В четырех исследованиях CytoSorb® применялся у пациентов, страдающих SARS-CoV-2 [48–51]. Еще три исследования использовали CytoSorb® у пациентов после остановки кровообращения [52–54]. Fig. 1. Было проведено еще четыре исследования, в которых изучалось действие CytoSorb®, но их нельзя было отнести ни к одной из ранее упомянутых групп. Мы определили эту группу как «тяжелое заболевание» и включили в нее следующие состояния: пациенты с тяжелыми травмами, пациенты с ОРДС, требующие вено-венозной ЭКМО, тяжелобольные пациенты с уровнем IL-6 ≥ 10 000 пг/мл и пациенты с тяжелым острым панкреатитом [55–58]. Было проведено двенадцать рандомизированных контролируемых исследований (РКИ), двенадцать обсервационных исследований, в которых группы вмешательства и контрольная группы были сопоставлены по показателям склонности (PSM), и десять обсервационных исследований с выбранным иным образом контрольной группой (nPSM) (Table 1). Всего 1297 пациентов получали лечение CytoSorb® по сравнению с 1314 пациентами без CytoSorb®.


Смертность
Самая длительная зарегистрированная смертность существенно не отличалась между группами Cytosorb® и контрольной группой во всех исследованиях вместе взятых (RR 1,07 [0,88; 1,31]), а также в подгруппах сепсиса (RR 0,98 [0,74; 1,31]), операции с искусственным кровообращением (RR 0,91 [0,64; 1,31]); 1,29]), тяжелое заболевание (RR 0,95 [0,59; 1,55]) и SARS-CoV-2 (RR 1,58 [0,50; 4,94]). У пациентов с остановкой кровообращения мы обнаружили значительное преимущество в выживаемости по сравнению с контрольной группой, не получавшей лечения (RR 1,22 [1,02; 1,46]) (Fig. 2). Результаты были очень похожими, если оценивать смертность в ОИТ, внутрибольничную или 30-дневную смертность (Additional file 1: Figures S1–S3).
Анализ подгрупп по дизайну исследования показал, что ни в одной из подгрупп, независимо от патологии и качества исследования, не удалось установить значительную разницу в выживаемости. Сравнивая объединенный анализ всех состояний, может сложиться впечатление, что результаты ухудшаются при более высоком качестве дизайна исследования (Fig. 3). В некоторых подгруппах мы обнаружили высокий уровень гетерогенности. РКИ имели значительно меньшую дисперсию между исследованиями (I2 = 0%; Q-statistic p = 0,452), чем наблюдательные исследования (PSM I2 = 59,5%; Q- statistic p = 0,004; nPSM I2 = 77,51%; Q- statistic p < 0,001). ) (Figs. 2, 3).


Последовательный анализ
TSA проводился в подгруппе CBP только для первичной конечной точки. На Fig 4 видно, что при фактических 478 пациентах необходимое количество 2801 не достигается. Однако cumulative Z-Score уже находится в области бесполезности, что позволяет предположить, что дополнительные исследования не изменят результат.

Продолжительность пребывания в ОИТ и стационаре
Продолжительность пребывания в ОИТ существенно не отличалась между CytoSorb® и контрольной группой ни для всех исследований вместе взятых, ни для подгрупп с разными диагнозами. Различия между группами (группа лечения – контрольная группа) сравнивались сначала как средние значения (±SD), а затем как медианные значения [и IQR] (Table 2).

Норадреналин и среднее артериальное давление (САД)
Не было значительной разницы в дозе норадреналина (мкг/кг/мин) или САД на исходном уровне. Пациентам контрольной группы, перенесшим остановку сердца, требовалась значительно более высокая доза норадреналина при сравнении средних значений (-0,16 ( ±0,15). Это наблюдение не могло быть подтверждено при сравнении медиан (- 0,09 ± 0,26)). Все остальные подгруппы не показали существенных различий между CytoSorb® и контрольной группой в дозе норадреналина после начала лечения. Кроме того, не выявлено существенных различий САД через 24 часа после начала лечения (Table 3).

Базовый уровень SOFA, SAPS‑2 и APACHE‑2
Ни один из этих показателей не показал существенных различий между CytoSorb® и контрольными группами на исходном уровне (Additional file 1: Table S1).
Уровни СРБ, ПКТ, лактата и IL-6
Уровни СРБ существенно не отличались ни на исходном уровне, ни при первом измерении после лечения (Additional file 1: Table S2). Уровни ПКТ были значительно выше в контрольной группе у пациентов с сепсисом при учете медианных значений (–7,60 (±7,76) / – 7,13 [– 13,29; – 0,97]). Уровни ПКТ во всех исследованиях вместе взятых и у пациентов с остановкой сердца существенно не различались. Кроме того, после лечения не было выявлено существенных различий в уровнях ПКТ (Additional file 1: Table S2). Не было никаких существенных различий в уровнях лактата на исходном уровне или при первом измерении после начала лечения ни для одной подгруппы (Additional file 1: Table S3). Только в подгруппе «тяжелое заболевание» медианные уровни IL-6 были значительно выше в группе вмешательства, средние значения не показали существенной разницы. После лечения также не было различий в уровнях IL-6 между CytoSorb® и контрольной группой ни в одной подгруппе. (Additional file 1: Table S3).
Неблагоприятные события
Возникновение нежелательных явлений отслеживалось в 22 из 34 исследований. Однако в большинстве исследований не было четко определено, что считать нежелательным явлением. Schädler et al. and Gleason et al. сообщили о снижении количества тромбоцитов, которое они наблюдали в связи с применением CytoSorb® [32, 40]. В других исследованиях также наблюдалось снижение количества тромбоцитов, которое не было связано с специфическое использование адсорбера CytoSorb® и, скорее всего, связано с контактом с экстракорпоральной мембраной в целом [35, 36, 47, 52, 54]. Ни одно из исследований не пришло к выводу, что CytoSorb® опасен.
Риск предвзятости
Риск систематической ошибки оценивался с помощью ROBINSI и RoB 2, а систематической ошибки публикации — с помощью воронкообразных диаграмм. Для оценки достоверности применили методологию GRADE. Некоторые исследования показали значительный риск систематической ошибки (Additional file 1: Figs. S4 and S5). С помощью ROBINS-I все исследования nPSM были оценены как «серьезные риски», поскольку в них не измерялись и не контролировались вмешивающиеся факторы. Кроме того, воронкообразная диаграмма свидетельствует о предвзятом отношении к публикациям в исследованиях nPSM: исследования с отрицательными результатами остались неопубликованными. (Additional file 1: Fig. 6). Напротив, в исследованиях PSM не учитывались искажающие факторы, поэтому большинство исследований PSM были оценены как «умеренный риск». Однако в некоторых исследованиях были исключены некоторые искажающие факторы, которые мы считали значимыми (Nemeth et al. 2018 исключили три значимые исходные характеристики (Heart Failure Score, IMPACT score, and high urgent status) из сопоставления [39]; Rieder et al. [52] не учитывали баллы RESP и PRESERVE при сопоставлении). В целом, воронкообразная диаграмма не свидетельствует о предвзятости публикаций в исследованиях PSM (Additional file 1: Fig. S7). РКИ также вызвали некоторые опасения. В целом оценка риска систематической ошибки проводилась очень строго. Исследования, которые не соответствовали протоколу запланированного лечения, были оценены как «серьезный риск». Аналогичным образом, исследования с выбывшими из них были оценены как «серьезный риск». Если параметр, упомянутый в протоколе исследования, был изменен или не проанализирован без обоснования, это также приводило к присвоению рейтинга «серьезного риска». Тем не менее, мы убеждены, что общее качество РКИ хорошее и нет предвзятости публикации (Additional file 1: Fig. S8).
Обсуждение
Этот метаанализ включает данные 34 исследований, включающих в общей сложности 1297 пациентов, у который использовали CytoSorb®, по сравнению с 1314 контрольными пациентами. Мы не наблюдали значительного снижения смертности благодаря вмешательству CytoSorb®. Использование методов очистки крови при лечении тяжелобольных, страдающих инфекциями, сепсисом и полиорганной недостаточностью, исследуется уже более 30 лет. [59] При цитокиновом шторме массивное высвобождение цитокинов может вызвать тяжелый воспалительный синдром, который приводит к дисфункции органов [60]. Таким образом, удаление провоспалительных цитокинов, таких как IL-1β, IL-6, IL-8 и TNF-α, из кровотока должно сдерживать гиперактивацию иммунной системы и снижать системный ответ. Из этой гипотезы вытекают различные обоснования гемоадсорбции. Удаление одного целевого цитокина в прошлом было безуспешным, поэтому усилия были сосредоточены на неселективном удалении цитокинов с помощью методов очистки крови, таких как гемоперфузия с использованием адсорбирующих систем, таких как CytoSorb® [61, 62].
Применение CytoSorb® и других адсорберов широко распространено, хотя на сегодняшний день нет единого мнения об эффективности лечения. [63, 64] Одним из ограничений нашего метаанализа является неоднородность исследований. Наблюдения отдельных исследований существенно различались, что мы объясняем разными причинами. Во-первых, существует немалое количество исследований с небольшим количеством участников, но с большим эффектом. Восемь исследований включали менее 15 пациентов в каждой группе [26, 28, 39, 45, 46, 51, 56, 58]. Эти исследования достигли больших результатов благодаря использованию CytoSorb®.
Напротив, существуют более крупные РКИ и наблюдательные исследования с сопоставлением показателей склонности (PSM) с заметно меньшим размером эффекта. Во-вторых, использование CytoSorb® во многом отличалось. Количество адсорберов, продолжительность терапии, время от постановки диагноза до первого использования адсорбера и скорость кровотока были очень противоречивыми. В-третьих, сравнивались заболевания, совершенно различающиеся по своей патофизиологии.
По этой причине мы включили анализ подгрупп различных заболеваний. Наконец, дисперсия оказалась довольно большой из-за ненормального распределения некоторых переменных. Мы преодолели это ограничение, проведя анализ подгрупп. Положительного эффекта CytoSorb® мы не обнаружили ни в одной из обследованных подгрупп. Это справедливо для подгрупп различных заболеваний, а также для подгрупп различных типов дизайна исследования.
Мало того, что положительный эффект вмешательства CytoSorb® с точки зрения снижения смертности неясен, даже исследования, изучающие теоретическое обоснование лечения, а именно снижение уровня цитокинов в крови, показывают противоречивые результаты. Было показано, что адсорбер CytoSorb® удаляет IL-1β, IL-6, IL-8 и TNF α в исследованиях in vivo, ex vivo и in vitro [65, 66]. Другие исследования не показали существенного снижения уровня IL-6 [32, 50]. Возможное объяснение стабильного уровня цитокинов, несмотря на их удаление в процессе гемоабсорбции, предложенное Honore et al., заключается в перемещении цитокинов из интерстиция в кровоток [67].
Более того, высвобождение цитокинов происходит непрерывно, поэтому избирательное удаление цитокинов на несколько часов в день может оказаться недостаточным для влияния на успех лечения. Это возможные причины того, почему CytoSorb® не смог снизить смертность. Также утверждается, что некоторые состояния, при которых применяется CytoSorb®, в основном SARS-CoV-2 и операции с использованием искусственного кровообращения, не сопровождаются особенно высокими уровнями цитокинов [32, 50].
Если предположить адекватное удаление провоспалительных цитокинов, то дальнейшим объяснением неспособности снизить смертность с помощью Cytosorb® является неселективное удаление всех гидрофобных компонентов плазмы с молекулярной массой до 55 кДа. Это означает, что также удаляются противовоспалительные медиаторы, гормоны и факторы свертывания крови [68]. Кроме того, Cytosorb® также удаляет антибиотики, что может привести к их субтерапевтическому уровню, что влияет на успех лечения сепсиса и общую выживаемость [69]. Нам срочно нужны данные рандомизированных контролируемых исследований по различным заболеваниям, при которых применяется CytoSorb®. На данный момент только использование при экстракорпоральном кровообращении может быть достаточно оценено, как показал последовательный анализ испытаний.
Заключение
В заключение следует отметить, что нет никаких доказательств снижения смертности при лечении CytoSorb® ни в одном из исследованных состояний. Поэтому мы не можем рекомендовать рутинное использование CytoSorb® пациентам в критическом состоянии, пока не будут получены четкие доказательства. Нам нужны адекватно спланированные РКИ по конкретным медицинским показаниям, нацеленные на нужных пациентов. Следовательно, необходимо провести подготовительную работу для выявления пациентов, которые могут ответить на терапию, например, очень высокие уровни цитокинов и определить оптимальный момент времени для терапии.
Ссылка на документ с дополнительными данными исследования
References
1. Chakraborty RK, Burns B. Systemic inflammatory response syndrome. In:StatPearls. StatPearls Publishing; 2022. Accessed March 7, 2022. http://www. ncbi. nlm. nih. gov/ books/ NBK54 7669/
2. Zhou F, Peng Z, Murugan R, Kellum JA. Blood purification and mortality in sepsis: a meta-analysis of randomized trials*. Crit Care Med. 2013;41(9):2209–20. https:// doi. org/ 10. 1097/ CCM. 0b013 e3182 8cf412.
3. Scharf C, Liebchen U, Paal M, Irlbeck M, Zoller M, Schroeder I. Blood purification with a cytokine adsorber for the elimination of myoglobin in critically ill patients with severe rhabdomyolysis. Crit Care. 2021;25(1):41. https:// doi. org/ 10. 1186/ s13054- 021- 03468-x.
4. Kohler T, Schwier E, Praxenthaler J, Kirchner C, Henzler D, Eickmeyer C. Therapeutic modulation of the host defense by hemoadsorption with CytoSorb®—basics, indications and perspectives—a scoping review. Int J Mol Sci. 2021;22(23):12786. https:// doi. org/ 10. 3390/ ijms2 22312 786.
5. McGrath S, Sohn H, Steele R, Benedetti A. Meta-analysis of the difference of medians. Biom J. 2020;62(1):69–98. https:// doi. org/ 10. 1002/ bimj. 201900036.
6. Luo D, Wan X, Liu J, Tong T. Optimally estimating the sample mean from the sample size, median, mid-range, and/or mid-quartile range. Stat Methods Med Res. 2018;27(6):1785–805. https:// doi. org/ 10. 1177/ 0962280216 669183.
7. Thorlund K, Engstrom J, Wetterslev J, Brok J, Imberger G, Gluud C (2017). User Manual for Trial Sequential Analysis (TSA) [Pdf ]. 2nd Ed. Copenhagen: Copenhagen Trial Unit, pp. 1–119. Downloadable from Ctu.Dk/Tsa. Accessed on: 05.03.2023 Online.
8. Poli E. Effect of cytoadsorbant device on post-cardio-pulmonary bypass inflammation in ESICM LIVES 2018: Effect of cytoadsorbant device on post-cardio-pulmonary bypass inflammation in ESICM LIVES 2018. Intensive Care Med Exp. 2018;6(S2):40. https:// doi. org/ 10. 1186/s40635- 018- 0201-6.
9. Laszlo I, Von Seth M, Hillered L, et al. Effects of adsorption of cytokines early in septic shock (the ‘ACESS-trial’)—results of the pilot study in 37th International Symposium on Intensive Care and Emergency Medicine (part 3 of 3): Brussels, Belgium. 21–24 March 2017. Crit Care.
2017;21(S1):58. https:// doi. org/ 10. 1186/ s13054- 017- 1629-x.
10. Brouwer WP, Duran S, Ince C. Improved survival beyond 28 days up to 1 year after CytoSorb treatment for refractory septic shock: a propensity weighted retrospective survival analysis. Blood Purif. 2021;50(4–5):539–45. https:// doi. org/ 10. 1159/ 00051 2309.
11. Woitsch S. Verbesserung der intrakraniellen Sauerstoffversorgung wahrend Operationen im tiefen hypothermen Kreislaufstillstand mit Hamoadsorption. 2018;(Der Hauptstadtkongress der DGAI fur Anasthesiologie und Intensivtherapie mit Pfl egesymposium und Rettungsdienstforum).
12. Schadler D, Porzelius C, Jorres A, et al. A multicenter randomized controlled study of an extracorporeal cytokine hemoadsorption device in septic patients. Crit Care. 2013;17(S2):P62. https:// doi. org/ 10. 1186/ cc120 00.
13. Schittek G. Beeinflussung des intensivstationaren Therapieverlaufs durch die Einfuhrung der Absorptionstherapie bei Patienten mit septischen Schock und akuten Nierenversagen. Published online 2018.
14. Born, F. Systemic Inflammatory Response Syndrome in der Herzchirurgie_Kardiotechnik 02–2014 - English Translation.pdf. Published online February 2014. http:// armag hansa lamat. com/ media/ brands/ Cytos orben ts/ Liter ature/ 2014_ Born% 20F% 20et% 20al. ,% 20Sys temic% 20Inflamma tory% 20Res ponse% 20Syn drome% 20in% 20der% 20Her zchir urgie_ Kardi otech nik% 2002- 2014% 20-% 20Eng lish% 20Tra nslat ion. pdf
15. Gliga S, Orth HM, Lubke N, Timm J, Luedde T, Jensen BEO. Multicentric Castleman’s disease in HIV patients: a single-center cohort diagnosed from 2008 to 2018. Infection. 2021;49(5):945–51. https:// doi. org/ 10. 1007/s15010- 021- 01618-5.
16. Mehta Y, Singh A, Singh A, Gupta A, Bhan A. Modulating the inflammatory response with hemadsorption (CytoSorb) in patients undergoing major aortic surgery. J Cardiothorac Vasc Anesth. 2021;35(2):673–5. https:// doi. org/ 10. 1053/j. jvca. 2020. 06. 028.
17. Lebreton G, Dorgham K, Quentric P, Combes A, Gorochov G, Schmidt M. Longitudinal cytokine profiling in patients with severe COVID-19 on extracorporeal membrane oxygenation and hemoadsorption. Am J Respir Crit Care Med. 2021;203(11):1433–5. https:// doi. org/ 10. 1164/ rccm.202011- 4140LE.
18. Lewis TC, Merchan C, Toy B, et al. Impact of CytoSorb hemoadsorption on sedation requirements in patients with severe COVID-19 on venovenous extracorporeal membrane oxygenation. ASAIO J. 2021;67(8):856–61. https:// doi. org/ 10. 1097/ MAT. 00000 00000 001513.
19. Garau I, Marz A, Sehner S, et al. Hemadsorption during cardiopulmonary bypass reduces interleukin 8 and tumor necrosis factor α serum levels in cardiac surgery: a randomized controlled trial. Minerva Anestesiol. 2019.https:// doi. org/ 10. 23736/ S0375- 9393. 18. 12898-7.
20. Bok S. CytoSorb: what is the effect on the circulation? in ESICM LIVES 2017: 30th ESICM Annual Congress September 23–27, 2017. Intensive Care Med Exp. 2017;5(S2):44. https:// doi. org/ 10. 1186/ s40635- 017- 0151-4.
21. Laubach CM. Cytokine and DAMP adsorption in septic acute kidney injury in ESICM LIVES 2018: Paris, France. 20-24 October 2018. Intensive Care Med Exp. 2018;6(S2):40. https:// doi. org/ 10. 1186/ s40635- 018- 0201-6.
22. Bottari G, Lorenzetti G, Severini F, Cappoli A, Cecchetti C, Guzzo I. Role of hemoperfusion with CytoSorb associated with continuous kidney replacement therapy on renal outcome in critically III children with septic shock. Front Pediatr. 2021;9:718049. https:// doi. org/ 10. 3389/ fped. 2021.718049.
23. Berlot G, Pintacuda S, Moro E, et al. Effects of tocilizumab versus hemoadsorption
combined with tocilizumab in patients with SARS-CoV-2 pneumonia: preliminary results. Int J Artif Organs. 2022;45(1):75–80. https:// doi. org/ 10. 1177/ 03913 98821 989334.
24. Bottari G, Murciano M, Merli P, et al. Hemoperfusion with CytoSorb to manage multiorgan dysfunction in the spectrum of hemophagocytic lymphohistiocytosis syndrome in critically Ill children. Blood Purif. 2022;51(5):417–24. https:// doi. org/ 10. 1159/ 00051 7471.
25. Schittek GA, Zoidl P, Eichinger M, et al. Adsorption therapy in critically ill with septic shock and acute kidney injury: a retrospective and prospective cohort study. Ann Intensive Care. 2020;10(1):154. https:// doi. org/ 10.1186/ s13613- 020- 00772-7.
26. Akil A, Ziegeler S, Reichelt J, et al. Combined use of CytoSorb and ECMO in patients with severe pneumogenic sepsis. Thorac Cardiovasc Surg. 2021;69(03):246–51. https:// doi. org/ 10. 1055/s- 0040- 17084 79.
27. Wendel Garcia PD, Hilty MP, Held U, Kleinert EM, Maggiorini M. Cytokine adsorption in severe, refractory septic shock. Intensive Care Med. 2021;47(11):1334–6. https:// doi. org/ 10. 1007/ s00134- 021- 06512-0.
28. Hawchar F, Laszlo I, Oveges N, Trasy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: a proof of concept randomized, controlled pilot study. J Crit Care. 2019;49:172–8. https:// doi. org/ 10. 1016/j.jcrc. 2018. 11. 003.
29. Kogelmann K, Hubner T, Schwameis F, Druner M, Scheller M, Jarczak D.First evaluation of a new dynamic scoring system intended to support prescription of adjuvant CytoSorb hemoadsorption therapy in patients with septic shock. J Clin Med. 2021;10(13):2939. https:// doi. org/ 10. 3390/jcm10 132939.
30. Rugg C, Klose R, Hornung R, et al. Hemoadsorption with CytoSorb in septic shock reduces catecholamine requirements and in-hospital mortality: a single-center retrospective ‘Genetic’ matched analysis. Biomedicines.2020;8(12):539. https:// doi. org/ 10. 3390/ biome dicin es812 0539.
31. Brouwer WP, Duran S, Kuijper M, Ince C. Hemoadsorption with CytoSorb shows a decreased observed versus expected 28-day all-cause mortality in ICU patients with septic shock: a propensity-score-weighted retrospective study. Crit Care. 2019;23(1):317. https:// doi. org/ 10. 1186/s13054- 019- 2588-1.
32. Schadler D, Pausch C, Heise D, et al. The effect of a novel extracorporeal cytokine hemoadsorption device on IL-6 elimination in septic patients: A randomized controlled trial. Eller K, ed. PLOS ONE. 2017;12(10):e0187015.https:// doi. org/ 10. 1371/ journ al. pone. 01870 15
33. Poli EC, Alberio L, Bauer-Doerries A, et al. Cytokine clearance with CytoSorb® during cardiac surgery: a pilot randomized controlled trial. Crit Care. 2019;23(1):108. https:// doi. org/ 10. 1186/ s13054- 019- 2399-4.
34. Hassan K, Kannmacher J, Wohlmuth P, Budde U, Schmoeckel M, Geidel S. Cytosorb adsorption during emergency cardiac operations in patients at high risk of bleeding. Ann Thorac Surg. 2019;108(1):45–51. https:// doi.org/ 10. 1016/j. athor acsur. 2018. 12. 032.
35. Bernardi MH, Rinoesl H, Dragosits K, et al. Effect of hemoadsorption during cardiopulmonary bypass surgery—a blinded, randomized, controlled pilot study using a novel adsorbent. Crit Care. 2016;20(1):96. https:// doi. org/ 10. 1186/ s13054- 016- 1270-0.
36. Taleska Stupica G, Sostaric M, Bozhinovska M, et al. Extracorporeal hemadsorption versus glucocorticoids during cardiopulmonary bypass: a prospective, randomized. Controlled Trial Cardiovasc Ther. 2020;2020:1–15. https:// doi. org/ 10. 1155/ 2020/ 78341 73.
37. Saller T, Hagl C, Woitsch S, et al. Haemadsorption improves intraoperative haemodynamics and metabolic changes during aortic surgery with hypothermic circulatory arrest. Eur J Cardiothorac Surg. 2019;56(4):731–7. https:// doi. org/ 10. 1093/ ejcts/ ezz074.
38. Santer D, Miazza J, Koechlin L, et al. Hemoadsorption during cardiopulmonary bypass in patients with endocarditis undergoing valve surgery: a retrospective single-center study. J Clin Med. 2021;10(4):564. https:// doi.org/ 10. 3390/ jcm10 040564.
39. Hassan K, Bruning T, Caspary M, et al. Hemoadsorption of rivaroxaban and ticagrelor during acute type A aortic dissection operations. Ann Thorac Cardiovasc Surg. 2022. https:// doi. org/ 10. 5761/ atcs. oa. 21- 00154.
40. Gleason TG, Argenziano M, Bavaria JE, et al. Hemoadsorption to reduce plasma-free hemoglobin during cardiac surgery: results of REFRESH I pilot study. Semin Thorac Cardiovasc Surg. 2019;31(4):783–93. https:// doi. org/10. 1053/j. semtc vs. 2019. 05. 006.
41. Trager K, Skrabal C, Fischer G, et al. Hemoadsorption treatment of patients with acute infective endocarditis during surgery with cardiopulmonary bypass—a case series. Int J Artif Organs. 2017;40(5):240–9. https:// doi. org/ 10. 5301/ ijao. 50005 83.
42. Nemeth E, Kovacs E, Racz K, et al. Impact of intraoperative cytokine adsorption on outcome of patients undergoing orthotopic heart transplantation-an observational study. Clin Transplant. 2018;32(4):e13211. https:// doi. org/ 10. 1111/ ctr. 13211.
43. Zhigalov K, Van den Eynde J, Zubarevich A, et al. Initial experience with CytoSorb therapy in patients receiving left ventricular assist devices. Artif Organs. 2022;46(1):95–105. https:// doi. org/ 10. 1111/ aor. 14099.
44. Haidari Z, Wendt D, Thielmann M, et al. Intraoperative hemoadsorption in patients with native mitral valve infective endocarditis. Ann Thorac Surg. 2020;110(3):890–6. https:// doi. org/ 10. 1016/j. athor acsur. 2019. 12. 067.
45. Wagner R, Soucek P, Ondrasek J, et al. Plasma levels of myocardial Micro-RNA-133a increase by intraoperative cytokine hemoadsorption in the complex cardiovascular operation. J Clin Med Res. 2019;11(12):789–97. https:// doi. org/ 10. 14740/ jocmr 3989.
46. Asch S, Kaufmann TP, Walter M, et al. The effect of perioperative hemadsorption in patients operated for acute infective endocarditis—a randomized controlled study. Artif Organs. 2021;45(11):1328–37. https://doi. org/ 10. 1111/ aor. 14019.
47. Diab M, Lehmann T, Bothe W, et al. Cytokine hemoadsorption during cardiac surgery versus standard surgical care for infective endocarditis (REMOVE): results from a multicenter randomized controlled trial. Circulation.2022;145(13):959–68. https:// doi. org/ 10. 1161/ CIRCU LATIO NAHA.121. 056940.
48. Schroeder I, Scharf C, Zoller M, et al. Charakteristika und Outcome von 70 beatmeten COVID-19-Patienten: Bilanz nach der ersten Welle an einem universitaren Zentrum. Anaesthesist. 2021;70(7):573–81. https:// doi. org/10. 1007/ s00101- 020- 00906-3.
49. Supady A, Weber E, Rieder M, et al. Cytokine adsorption in patients with severe COVID-19 pneumonia requiring extracorporeal membrane oxygenation (CYCOV): a single centre, open-label, randomised, controlled trial. Lancet Respir Med. 2021;9(7):755–62. https:// doi. org/ 10. 1016/ S2213-2600(21) 00177-6.
50. Stockmann H, Thelen P, Stroben F, et al. CytoSorb rescue for COVID-19 patients with vasoplegic shock and multiple organ failure: a prospective, open-label, randomized controlled pilot study. Crit Care Med. 2022.https:// doi. org/ 10. 1097/ CCM. 00000 00000 005493.
51. Rampino T, Gregorini M, Perotti L, et al. Hemoperfusion with CytoSorb as adjuvant therapy in critically Ill patients with SARS-CoV2 pneumonia. Blood Purif. 2021;50(4–5):566–71. https:// doi. org/ 10. 1159/ 00051 1725.
52. Supady A, Zahn T, Kuhl M, et al. Cytokine adsorption in patients with post-cardiac arrest syndrome after extracorporeal cardiopulmonary resuscitation (CYTER)—a single-centre, open-label, randomised, controlled trial. Resuscitation. 2022. https:// doi. org/ 10. 1016/j. resus citat ion.2022. 02. 001.
53. Akin M, Garcheva V, Sieweke JT, et al. Early use of hemoadsorption in patients after out-of hospital cardiac arrest—a matched pair analysis. Ballotta A, ed. PLOS ONE. 2020;15(11):e0241709. https:// doi. org/ 10. 1371/journ al. pone. 02417 09
54. Supady A, Zahn T, Rieder M, et al. Effect of cytokine adsorption on survival and circulatory stabilization in patients receiving extracorporeal cardiopulmonary resuscitation. ASAIO J. 2021. https:// doi. org/ 10. 1097/MAT. 00000 00000 001441.
55. Scharf C, Schroeder I, Paal M, et al. Can the cytokine adsorber CytoSorb® help to mitigate cytokine storm and reduce mortality in critically ill patients? A propensity score matching analysis. Ann Intensive Care. 2021;11(1):115. https:// doi. org/ 10. 1186/ s13613- 021- 00905-6.
56. Rieder M, Duerschmied D, Zahn T, et al. Cytokine adsorption in severe acute respiratory failure requiring veno-venous extracorporeal membrane oxygenation. ASAIO J. 2021;67(3):332–8. https:// doi. org/ 10. 1097/MAT. 00000 00000 001302.
57. Rasch S, Sancak S, Erber J, et al. Influence of extracorporeal cytokine adsorption on hemodynamics in severe acute pancreatitis: results of the matched cohort pancreatitis cytosorbents inflammatory cytokine removal (PACIFIC) study. Artif Organs. 2022. https:// doi. org/ 10. 1111/ aor.14195.
58. Wilhelmi M. Pilotstudie zur Outcome-Analyse bei Einsatz einer Cytokin-Hamoadsorption bei schwerstverletzten Polytraumapatienten. Published online 2018. https:// cytos orb- thera py. com/ wp- conte nt/ uploa ds/ 2018/12/ 2018_ Wilhe lmi_ Polyt rauma_ DIVI_ Poste r1. pdf
59. Barzilay E, Kessler D, Berlot G, Gullo A, Geber D, Ben ZI. Use of extracorporeal supportive techniques as additional treatment for septic-induced multiple organ failure patients. Crit Care Med. 1989;17(7):634–7. https://doi. org/ 10. 1097/ 00003 246- 19890 7000- 00007.
60. Fajgenbaum DC, June CH. Cytokine storm. N Engl J Med. 2020;383(23):2255–73. https:// doi. org/ 10. 1056/ NEJMr a2026 131.
61. Deans KJ, Haley M, Natanson C, Eichacker PQ, Minneci PC. Novel therapies for sepsis: a review. J Trauma. 2005;58(4):867–74. https:// doi. org/ 10.1097/ 01. ta. 00001 58244. 69179. 94.
62. Rimmele T, Kellum JA. Clinical review: blood purification for sepsis. Crit Care Lond Engl. 2011;15(1):205. https:// doi. org/ 10. 1186/ cc9411.
63. Ricci Z, Romagnoli S, Reis T, Bellomo R, Ronco C. Hemoperfusion in the intensive care unit. Intensive Care Med. 2022;48(10):1397–408. https:// doi.org/ 10. 1007/ s00134- 022- 06810-1.
64. Kielstein JT, Zarbock A. Is this the beginning of the end of cytokine adsorption? Crit Care Med. 2022;50(6):1026–9. https:// doi. org/ 10. 1097/CCM. 00000 00000 005509.
65. Kellum JA, Song M, Venkataraman R. Hemoadsorption removes tumor necrosis factor, interleukin-6, and interleukin-10, reduces nuclear factor-kappaB DNA binding, and improves short-term survival in lethal endotoxemia. Crit Care Med. 2004;32(3):801–5. https:// doi. org/ 10. 1097/ 01. ccm.00001 14997. 39857. 69.
66. Harm S, Schildbock C, Hartmann J. Cytokine removal in extracorporeal blood purification: an in vitro study. Blood Purif. 2020;49(1–2):33–43. https:// doi. org/ 10. 1159/ 00050 2680.
67. Honore PM, Matson JR. Extracorporeal removal for sepsis: acting at the tissue level–the beginning of a new era for this treatment modality in septic shock. Crit Care Med. 2004;32(3):896–7. https:// doi. org/ 10. 1097/ 01.
ccm. 00001 15262. 31804. 46.
68. Harm S, Falkenhagen D, Hartmann J. Pore size–a key property for selective toxin removal in blood purification. Int J Artif Organs. 2014;37(9):668–78. https:// doi. org/ 10. 5301/ ijao. 50003 54.
69. Konig C, Rohr AC, Frey OR, et al. In vitro removal of anti-infective agents by a novel cytokine adsorbent system. Int J Artif Organs. 2019;42(2):57–64. https:// doi. org/ 10. 1177/ 03913 98818 812601.
[DETAIL_PICTURE] =>
[~DETAIL_PICTURE] =>
[DATE_ACTIVE_FROM] => 20.12.2023
[~DATE_ACTIVE_FROM] => 20.12.2023
[ACTIVE_FROM_X] => 2023-12-20 00:00:00
[~ACTIVE_FROM_X] => 2023-12-20 00:00:00
[ACTIVE_FROM] => 20.12.2023
[~ACTIVE_FROM] => 20.12.2023
[SHOW_COUNTER] => 1061
[~SHOW_COUNTER] => 1061
[ID] => 8397
[~ID] => 8397
[IBLOCK_ID] => 2
[~IBLOCK_ID] => 2
[IBLOCK_SECTION_ID] =>
[~IBLOCK_SECTION_ID] =>
[DETAIL_TEXT_TYPE] => html
[~DETAIL_TEXT_TYPE] => html
[PREVIEW_TEXT] =>
[~PREVIEW_TEXT] =>
[PREVIEW_TEXT_TYPE] => text
[~PREVIEW_TEXT_TYPE] => text
[TIMESTAMP_X] => 11.11.2024 14:31:43
[~TIMESTAMP_X] => 11.11.2024 14:31:43
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/effektivnost-cytosorb-sistematicheskiy-obzor-i-meta-analiz/
[~DETAIL_PAGE_URL] => /library/articles/effektivnost-cytosorb-sistematicheskiy-obzor-i-meta-analiz/
[LANG_DIR] => /
[~LANG_DIR] => /
[CODE] => effektivnost-cytosorb-sistematicheskiy-obzor-i-meta-analiz
[~CODE] => effektivnost-cytosorb-sistematicheskiy-obzor-i-meta-analiz
[EXTERNAL_ID] => 8397
[~EXTERNAL_ID] => 8397
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[IBLOCK_CODE] => articles
[~IBLOCK_CODE] => articles
[IBLOCK_EXTERNAL_ID] => content-articles
[~IBLOCK_EXTERNAL_ID] => content-articles
[LID] => s1
[~LID] => s1
[NAV_RESULT] =>
[NAV_CACHED_DATA] =>
[DISPLAY_ACTIVE_FROM] => 20 декабря 2023
[IPROPERTY_VALUES] => Array
(
)
[FIELDS] => Array
(
[NAME] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[PREVIEW_PICTURE] => Array
(
[ID] => 5844
[TIMESTAMP_X] => 11.11.2024 14:31:43
[MODULE_ID] => iblock
[HEIGHT] => 600
[WIDTH] => 900
[FILE_SIZE] => 38738
[CONTENT_TYPE] => image/jpeg
[SUBDIR] => iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j
[FILE_NAME] => der-adsorber-regain-control-cytosorb.jpg
[ORIGINAL_NAME] => der-adsorber-regain-control-cytosorb.jpg
[DESCRIPTION] =>
[HANDLER_ID] =>
[EXTERNAL_ID] => 501a6fe7ceacdb39ebe82b0bddac739b
[VERSION_ORIGINAL_ID] =>
[META] =>
[SRC] => /upload/iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j/der-adsorber-regain-control-cytosorb.jpg
[UNSAFE_SRC] => /upload/iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j/der-adsorber-regain-control-cytosorb.jpg
[SAFE_SRC] => /upload/iblock/251/78b46n29e7oxxvf21mb0ctxtkez0w67j/der-adsorber-regain-control-cytosorb.jpg
[ALT] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[TITLE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
)
[DETAIL_TEXT] =>
S Becker, H Lang, C V Barbosa, Z Tian, A Melk, B Schmidt
Efficacy of CytoSorb
®: asystematic review and meta-analysis
Critical Care (2023) 27:215 doi.org/10.1186/s13054-023-04492-9
Абстракт
Адсорбция цитокинов с использованием адсорбера CytoSorb® была предложена при различных клинических ситуациях, включая сепсис, ОРДС, гипервоспалительные синдромы, операции на сердце или восстановление после остановки кровообращения. Целью данного анализа является предоставление доказательств эффективности адсорбера CytoSorb® в отношении смертности в различных условиях. Провели поиск в базе данных PubMed, Cochrane Library и в базе данных Cytosorbents™ (01.1.2010–29.5.2022) и рассмотрели рандомизированные контролируемые исследования и наблюдательные исследования с контрольными группами. Самая поздняя зарегистрированная смертность была определена как первичная конечная точка. Мы рассчитали коэффициенты риска и 95%-ные доверительные интервалы и использовали модель случайных эффектов DerSimonian and Lairds. Проанализировали все исследования вместе и разделили их на подгруппы: сепсис, искусственное кровообращение (CPB), другие тяжелые заболевания, инфекция SARS-CoV-2 и восстановление после остановки сердца. Метаанализ был зарегистрирован заранее (PROSPERO: CRD42022290334). Из первоначальных 1295 публикаций были признаны подходящими 34 исследования, которые включали 1297 пациентов с использованием CytoSorb®, и 1314 пациентов контрольной группы. Вмешательство Cytosorb® не снизило смертность (RR [95%-ДИ]: все исследования 1,07 [0,88; 1,31], сепсис 0,98 [0,74; 1,31], операция искусственного кровообращения 0,91 [0,64; 1,29], другие тяжелые заболевания 0,95 [0,59; 1,55] , SARS-CoV-2 1,58 [0,50; 4,94]). У пациентов с остановкой сердца мы обнаружили значительное преимущество в выживаемости по сравнению с контрольной группой, не получавшей лечения (1,22 [1,02; 1,46]). Мы не обнаружили существенных различий в продолжительности пребывания в ОИТ, уровнях лактата или IL-6 после лечения. Из 34 исследований, отвечающих критериям отбора, только 12 были рандомизированными контролируемыми исследованиями. Все наблюдательные исследования показали риск систематической ошибки от умеренного до серьезного. На сегодняшний день нет доказательств положительного влияния адсорбера CytoSorb® на смертность при различных заболеваниях, что оправдывало бы его широкое использование в интенсивной терапии.
Введение
Массивный выброс цитокинов в кровь является патофизиологическим триггером многих опасных для жизни заболеваний. Провоспалительные цитокины приводят к вазодилатации, капиллярной утечке и коагулопатии. Противовоспалительные цитокины могут вызывать относительную иммуносупрессию, приводящую к вторичным нозокомиальным инфекциям. Неконтролируемый выброс обоих типов цитокинов может привести к развитию мультиорганной недостаточности [1]. Для неселективного снижения уровня цитокинов были предложены различные методы очистки крови, такие как диализ с использованием мембран с высокой точкой отсечки, гемосорбция, высокообъемная гемофильтрация и плазмообмен [2]. CytoSorb® - одно из наиболее широко используемых устройств для очистки крови, которое способно снижать уровень гидрофобных молекул с молекулярной массой до 55 кДа. [3] Таким образом, устройство адсорбирует цитокины, желчные кислоты и миоглобин. CytoSorb® находит клиническое применение у пациентов с избыточным иммунным ответом, например при сепсисе, ОРДС, SARS-CoV-2 инфекции, гиперинтенсивных воспалительных синдромах, а также во время и после кардиохирургических операций с использованием экстракорпорального кровообращения (CPB). Кроме того, CytoSorb® может быть полезен при печеночной недостаточности, для элиминации пероральных антикоагулянтов прямого действия (DOACs) или некоторых острых интоксикациях [4]. Устройство считается безопасным и хорошо переносится. Однако единого мнения по поводу эффективности нет. Целью этого систематического обзора и метаанализа является оценка влияния CytoSorb® на все ранее описанные заболевания. Первичной конечной точкой является самая поздняя зарегистрированная смертность. Кроме того, будут сравниваться продолжительность пребывания в отделении интенсивной терапии, потребности в норэпинефрине, уровни IL-6 и лактата.
Методы
Повели систематический поиск в базе данных PubMed и Cochrane Library, используя «CytoSorb» в качестве ключевого слова. Проверена база данных CytoSorbents https://literature.cytosorb-herapy.com/?_ga=2.58770730.642024760.1646225438-7175153.1645687922). Последнее обновление проведено 29 мая 2022 года. Исследования были выбраны двумя исследователями независимо; в случае разногласий искался консенсус. В соответствии с рекомендациями группы Bias Method Group Кокрейновской сети качество исследований оценивалось с помощью ROBINS-I (Risk of Bias in Non-randomized Studies of Interventions) или инструмента RoB 2 (revised tool for Risk of Bias in randomized trials). Данные были собраны двумя исследователями независимо и обобщены в файле Excel. Если вместо точных значений предоставлялись графики, мы анализировали данные с помощью «WebPlotDigitizer» (https://apps.automeris.io/wpd/). Первичной конечной точкой была самая поздняя зарегистрированная смертность (30-дневная смертность в стационаре или ОИТ). Если было представлено более одного значения, выбиралось значение с самым длительным периодом наблюдения. Первичная конечная точка рассчитывалась как относительный риск. Анализ подгрупп первичной конечной точки проводился для различных заболеваний (сепсис, искусственное кровообращение, тяжелое заболевание, SARS-CoV-2 и остановка сердца). Также был проведен анализ подгрупп для различных дизайнов исследований (рандомизированные контролируемые исследования по сравнению с наблюдательными исследованиями с соответствующими контрольными показателями по показателю предрасположенности и без них).
Для вычисления использовалась модель случайных эффектов (DerSimonian and Laird). Вторичными конечными точками были продолжительность пребывания в ОИТ и стационаре. Мы извлекли информацию о дозе норэпинефрина, среднем артериальном давлении (САД), СРБ, ПКТ, уровни лактата и интерлейкина-6 (IL-6) до и после использования CytoSorb®. Уровни маркеров воспаления после CytoSorb® определялись как первое зарегистрированное значение после начала лечения CytoSorb®. Кроме того, мы оценили показатели SOFA, SAPS-2 и APACHE-2, чтобы сравнить контрольную группу и группу вмешательства. Также проверили все исследования на предмет сообщений о нежелательных явлениях. Вторичные конечные точки были представлены в виде разницы рисков (группа лечения и группа контроля) для всех исследований в совокупности и для отдельных подгрупп. Анализ вторичных конечных точек проводился, если по крайней мере в двух исследованиях сообщалось о соответствующих данных. Для плановых операций с использованием экстракорпорального кровообращения показатели сепсиса и физиологические конечные точки не применялись. В оригинальных исследованиях вторичные конечные точки чаще всего сообщались в виде средних или медианных значений. Мы следовали рекомендациям McGrath et al [5]: при нормальном распределении средние значения считались равными медианам. Медианы с интерквартильным размахом или минимальными и максимальными значения были преобразованы в средние значения и стандартное отклонение по методу Luo et al. [6]. Впоследствии влияние средних значений оценивали с использованием модели случайного эффекта с использованием метода DerSimonian-Laird. Влияние медианных значений рассчитывали методом квантильной оценки. Риск систематической ошибки оценивался с помощью ROBINSI и RoB 2 двумя исследователями независимо. Мы использовали воронкообразные графики для оценки систематической ошибки публикации и применили методологию GRADE для оценки достоверности. Для всех анализов мы использовали R 4.1.0 с пакетами meta, metafor, metamedian, lqmm, hmisc, estmeansd, Forestplot и writexl. Значения P < 0,05 считались статистически значимыми. Гетерогенность оценивалась с использованием I2 и Cochrane’s q. Протокол исследования зарегистрирован в базе данных PROSPERO (регистрационный номер: CRD42022290334).
Полученные результаты
Поиск дал 1295 результатов. Для анализа было доступно 34 исследования (Fig. 1).

Пациенты детского возраста не были включены, поскольку все исследования с участием детей представляли собой либо сообщения о случаях заболевания, либо не имели контрольной группы. В восьми исследованиях изучалось влияние CytoSorb® на пациентов с сепсисом или септическим шоком [25–32]. В пятнадцати исследованиях его использовали при искусственном кровообращении [33–47]. В четырех исследованиях CytoSorb® применялся у пациентов, страдающих SARS-CoV-2 [48–51]. Еще три исследования использовали CytoSorb® у пациентов после остановки кровообращения [52–54]. Fig. 1. Было проведено еще четыре исследования, в которых изучалось действие CytoSorb®, но их нельзя было отнести ни к одной из ранее упомянутых групп. Мы определили эту группу как «тяжелое заболевание» и включили в нее следующие состояния: пациенты с тяжелыми травмами, пациенты с ОРДС, требующие вено-венозной ЭКМО, тяжелобольные пациенты с уровнем IL-6 ≥ 10 000 пг/мл и пациенты с тяжелым острым панкреатитом [55–58]. Было проведено двенадцать рандомизированных контролируемых исследований (РКИ), двенадцать обсервационных исследований, в которых группы вмешательства и контрольная группы были сопоставлены по показателям склонности (PSM), и десять обсервационных исследований с выбранным иным образом контрольной группой (nPSM) (Table 1). Всего 1297 пациентов получали лечение CytoSorb® по сравнению с 1314 пациентами без CytoSorb®.


Смертность
Самая длительная зарегистрированная смертность существенно не отличалась между группами Cytosorb® и контрольной группой во всех исследованиях вместе взятых (RR 1,07 [0,88; 1,31]), а также в подгруппах сепсиса (RR 0,98 [0,74; 1,31]), операции с искусственным кровообращением (RR 0,91 [0,64; 1,31]); 1,29]), тяжелое заболевание (RR 0,95 [0,59; 1,55]) и SARS-CoV-2 (RR 1,58 [0,50; 4,94]). У пациентов с остановкой кровообращения мы обнаружили значительное преимущество в выживаемости по сравнению с контрольной группой, не получавшей лечения (RR 1,22 [1,02; 1,46]) (Fig. 2). Результаты были очень похожими, если оценивать смертность в ОИТ, внутрибольничную или 30-дневную смертность (Additional file 1: Figures S1–S3).
Анализ подгрупп по дизайну исследования показал, что ни в одной из подгрупп, независимо от патологии и качества исследования, не удалось установить значительную разницу в выживаемости. Сравнивая объединенный анализ всех состояний, может сложиться впечатление, что результаты ухудшаются при более высоком качестве дизайна исследования (Fig. 3). В некоторых подгруппах мы обнаружили высокий уровень гетерогенности. РКИ имели значительно меньшую дисперсию между исследованиями (I2 = 0%; Q-statistic p = 0,452), чем наблюдательные исследования (PSM I2 = 59,5%; Q- statistic p = 0,004; nPSM I2 = 77,51%; Q- statistic p < 0,001). ) (Figs. 2, 3).


Последовательный анализ
TSA проводился в подгруппе CBP только для первичной конечной точки. На Fig 4 видно, что при фактических 478 пациентах необходимое количество 2801 не достигается. Однако cumulative Z-Score уже находится в области бесполезности, что позволяет предположить, что дополнительные исследования не изменят результат.

Продолжительность пребывания в ОИТ и стационаре
Продолжительность пребывания в ОИТ существенно не отличалась между CytoSorb® и контрольной группой ни для всех исследований вместе взятых, ни для подгрупп с разными диагнозами. Различия между группами (группа лечения – контрольная группа) сравнивались сначала как средние значения (±SD), а затем как медианные значения [и IQR] (Table 2).

Норадреналин и среднее артериальное давление (САД)
Не было значительной разницы в дозе норадреналина (мкг/кг/мин) или САД на исходном уровне. Пациентам контрольной группы, перенесшим остановку сердца, требовалась значительно более высокая доза норадреналина при сравнении средних значений (-0,16 ( ±0,15). Это наблюдение не могло быть подтверждено при сравнении медиан (- 0,09 ± 0,26)). Все остальные подгруппы не показали существенных различий между CytoSorb® и контрольной группой в дозе норадреналина после начала лечения. Кроме того, не выявлено существенных различий САД через 24 часа после начала лечения (Table 3).

Базовый уровень SOFA, SAPS‑2 и APACHE‑2
Ни один из этих показателей не показал существенных различий между CytoSorb® и контрольными группами на исходном уровне (Additional file 1: Table S1).
Уровни СРБ, ПКТ, лактата и IL-6
Уровни СРБ существенно не отличались ни на исходном уровне, ни при первом измерении после лечения (Additional file 1: Table S2). Уровни ПКТ были значительно выше в контрольной группе у пациентов с сепсисом при учете медианных значений (–7,60 (±7,76) / – 7,13 [– 13,29; – 0,97]). Уровни ПКТ во всех исследованиях вместе взятых и у пациентов с остановкой сердца существенно не различались. Кроме того, после лечения не было выявлено существенных различий в уровнях ПКТ (Additional file 1: Table S2). Не было никаких существенных различий в уровнях лактата на исходном уровне или при первом измерении после начала лечения ни для одной подгруппы (Additional file 1: Table S3). Только в подгруппе «тяжелое заболевание» медианные уровни IL-6 были значительно выше в группе вмешательства, средние значения не показали существенной разницы. После лечения также не было различий в уровнях IL-6 между CytoSorb® и контрольной группой ни в одной подгруппе. (Additional file 1: Table S3).
Неблагоприятные события
Возникновение нежелательных явлений отслеживалось в 22 из 34 исследований. Однако в большинстве исследований не было четко определено, что считать нежелательным явлением. Schädler et al. and Gleason et al. сообщили о снижении количества тромбоцитов, которое они наблюдали в связи с применением CytoSorb® [32, 40]. В других исследованиях также наблюдалось снижение количества тромбоцитов, которое не было связано с специфическое использование адсорбера CytoSorb® и, скорее всего, связано с контактом с экстракорпоральной мембраной в целом [35, 36, 47, 52, 54]. Ни одно из исследований не пришло к выводу, что CytoSorb® опасен.
Риск предвзятости
Риск систематической ошибки оценивался с помощью ROBINSI и RoB 2, а систематической ошибки публикации — с помощью воронкообразных диаграмм. Для оценки достоверности применили методологию GRADE. Некоторые исследования показали значительный риск систематической ошибки (Additional file 1: Figs. S4 and S5). С помощью ROBINS-I все исследования nPSM были оценены как «серьезные риски», поскольку в них не измерялись и не контролировались вмешивающиеся факторы. Кроме того, воронкообразная диаграмма свидетельствует о предвзятом отношении к публикациям в исследованиях nPSM: исследования с отрицательными результатами остались неопубликованными. (Additional file 1: Fig. 6). Напротив, в исследованиях PSM не учитывались искажающие факторы, поэтому большинство исследований PSM были оценены как «умеренный риск». Однако в некоторых исследованиях были исключены некоторые искажающие факторы, которые мы считали значимыми (Nemeth et al. 2018 исключили три значимые исходные характеристики (Heart Failure Score, IMPACT score, and high urgent status) из сопоставления [39]; Rieder et al. [52] не учитывали баллы RESP и PRESERVE при сопоставлении). В целом, воронкообразная диаграмма не свидетельствует о предвзятости публикаций в исследованиях PSM (Additional file 1: Fig. S7). РКИ также вызвали некоторые опасения. В целом оценка риска систематической ошибки проводилась очень строго. Исследования, которые не соответствовали протоколу запланированного лечения, были оценены как «серьезный риск». Аналогичным образом, исследования с выбывшими из них были оценены как «серьезный риск». Если параметр, упомянутый в протоколе исследования, был изменен или не проанализирован без обоснования, это также приводило к присвоению рейтинга «серьезного риска». Тем не менее, мы убеждены, что общее качество РКИ хорошее и нет предвзятости публикации (Additional file 1: Fig. S8).
Обсуждение
Этот метаанализ включает данные 34 исследований, включающих в общей сложности 1297 пациентов, у который использовали CytoSorb®, по сравнению с 1314 контрольными пациентами. Мы не наблюдали значительного снижения смертности благодаря вмешательству CytoSorb®. Использование методов очистки крови при лечении тяжелобольных, страдающих инфекциями, сепсисом и полиорганной недостаточностью, исследуется уже более 30 лет. [59] При цитокиновом шторме массивное высвобождение цитокинов может вызвать тяжелый воспалительный синдром, который приводит к дисфункции органов [60]. Таким образом, удаление провоспалительных цитокинов, таких как IL-1β, IL-6, IL-8 и TNF-α, из кровотока должно сдерживать гиперактивацию иммунной системы и снижать системный ответ. Из этой гипотезы вытекают различные обоснования гемоадсорбции. Удаление одного целевого цитокина в прошлом было безуспешным, поэтому усилия были сосредоточены на неселективном удалении цитокинов с помощью методов очистки крови, таких как гемоперфузия с использованием адсорбирующих систем, таких как CytoSorb® [61, 62].
Применение CytoSorb® и других адсорберов широко распространено, хотя на сегодняшний день нет единого мнения об эффективности лечения. [63, 64] Одним из ограничений нашего метаанализа является неоднородность исследований. Наблюдения отдельных исследований существенно различались, что мы объясняем разными причинами. Во-первых, существует немалое количество исследований с небольшим количеством участников, но с большим эффектом. Восемь исследований включали менее 15 пациентов в каждой группе [26, 28, 39, 45, 46, 51, 56, 58]. Эти исследования достигли больших результатов благодаря использованию CytoSorb®.
Напротив, существуют более крупные РКИ и наблюдательные исследования с сопоставлением показателей склонности (PSM) с заметно меньшим размером эффекта. Во-вторых, использование CytoSorb® во многом отличалось. Количество адсорберов, продолжительность терапии, время от постановки диагноза до первого использования адсорбера и скорость кровотока были очень противоречивыми. В-третьих, сравнивались заболевания, совершенно различающиеся по своей патофизиологии.
По этой причине мы включили анализ подгрупп различных заболеваний. Наконец, дисперсия оказалась довольно большой из-за ненормального распределения некоторых переменных. Мы преодолели это ограничение, проведя анализ подгрупп. Положительного эффекта CytoSorb® мы не обнаружили ни в одной из обследованных подгрупп. Это справедливо для подгрупп различных заболеваний, а также для подгрупп различных типов дизайна исследования.
Мало того, что положительный эффект вмешательства CytoSorb® с точки зрения снижения смертности неясен, даже исследования, изучающие теоретическое обоснование лечения, а именно снижение уровня цитокинов в крови, показывают противоречивые результаты. Было показано, что адсорбер CytoSorb® удаляет IL-1β, IL-6, IL-8 и TNF α в исследованиях in vivo, ex vivo и in vitro [65, 66]. Другие исследования не показали существенного снижения уровня IL-6 [32, 50]. Возможное объяснение стабильного уровня цитокинов, несмотря на их удаление в процессе гемоабсорбции, предложенное Honore et al., заключается в перемещении цитокинов из интерстиция в кровоток [67].
Более того, высвобождение цитокинов происходит непрерывно, поэтому избирательное удаление цитокинов на несколько часов в день может оказаться недостаточным для влияния на успех лечения. Это возможные причины того, почему CytoSorb® не смог снизить смертность. Также утверждается, что некоторые состояния, при которых применяется CytoSorb®, в основном SARS-CoV-2 и операции с использованием искусственного кровообращения, не сопровождаются особенно высокими уровнями цитокинов [32, 50].
Если предположить адекватное удаление провоспалительных цитокинов, то дальнейшим объяснением неспособности снизить смертность с помощью Cytosorb® является неселективное удаление всех гидрофобных компонентов плазмы с молекулярной массой до 55 кДа. Это означает, что также удаляются противовоспалительные медиаторы, гормоны и факторы свертывания крови [68]. Кроме того, Cytosorb® также удаляет антибиотики, что может привести к их субтерапевтическому уровню, что влияет на успех лечения сепсиса и общую выживаемость [69]. Нам срочно нужны данные рандомизированных контролируемых исследований по различным заболеваниям, при которых применяется CytoSorb®. На данный момент только использование при экстракорпоральном кровообращении может быть достаточно оценено, как показал последовательный анализ испытаний.
Заключение
В заключение следует отметить, что нет никаких доказательств снижения смертности при лечении CytoSorb® ни в одном из исследованных состояний. Поэтому мы не можем рекомендовать рутинное использование CytoSorb® пациентам в критическом состоянии, пока не будут получены четкие доказательства. Нам нужны адекватно спланированные РКИ по конкретным медицинским показаниям, нацеленные на нужных пациентов. Следовательно, необходимо провести подготовительную работу для выявления пациентов, которые могут ответить на терапию, например, очень высокие уровни цитокинов и определить оптимальный момент времени для терапии.
Ссылка на документ с дополнительными данными исследования
References
1. Chakraborty RK, Burns B. Systemic inflammatory response syndrome. In:StatPearls. StatPearls Publishing; 2022. Accessed March 7, 2022. http://www. ncbi. nlm. nih. gov/ books/ NBK54 7669/
2. Zhou F, Peng Z, Murugan R, Kellum JA. Blood purification and mortality in sepsis: a meta-analysis of randomized trials*. Crit Care Med. 2013;41(9):2209–20. https:// doi. org/ 10. 1097/ CCM. 0b013 e3182 8cf412.
3. Scharf C, Liebchen U, Paal M, Irlbeck M, Zoller M, Schroeder I. Blood purification with a cytokine adsorber for the elimination of myoglobin in critically ill patients with severe rhabdomyolysis. Crit Care. 2021;25(1):41. https:// doi. org/ 10. 1186/ s13054- 021- 03468-x.
4. Kohler T, Schwier E, Praxenthaler J, Kirchner C, Henzler D, Eickmeyer C. Therapeutic modulation of the host defense by hemoadsorption with CytoSorb®—basics, indications and perspectives—a scoping review. Int J Mol Sci. 2021;22(23):12786. https:// doi. org/ 10. 3390/ ijms2 22312 786.
5. McGrath S, Sohn H, Steele R, Benedetti A. Meta-analysis of the difference of medians. Biom J. 2020;62(1):69–98. https:// doi. org/ 10. 1002/ bimj. 201900036.
6. Luo D, Wan X, Liu J, Tong T. Optimally estimating the sample mean from the sample size, median, mid-range, and/or mid-quartile range. Stat Methods Med Res. 2018;27(6):1785–805. https:// doi. org/ 10. 1177/ 0962280216 669183.
7. Thorlund K, Engstrom J, Wetterslev J, Brok J, Imberger G, Gluud C (2017). User Manual for Trial Sequential Analysis (TSA) [Pdf ]. 2nd Ed. Copenhagen: Copenhagen Trial Unit, pp. 1–119. Downloadable from Ctu.Dk/Tsa. Accessed on: 05.03.2023 Online.
8. Poli E. Effect of cytoadsorbant device on post-cardio-pulmonary bypass inflammation in ESICM LIVES 2018: Effect of cytoadsorbant device on post-cardio-pulmonary bypass inflammation in ESICM LIVES 2018. Intensive Care Med Exp. 2018;6(S2):40. https:// doi. org/ 10. 1186/s40635- 018- 0201-6.
9. Laszlo I, Von Seth M, Hillered L, et al. Effects of adsorption of cytokines early in septic shock (the ‘ACESS-trial’)—results of the pilot study in 37th International Symposium on Intensive Care and Emergency Medicine (part 3 of 3): Brussels, Belgium. 21–24 March 2017. Crit Care.
2017;21(S1):58. https:// doi. org/ 10. 1186/ s13054- 017- 1629-x.
10. Brouwer WP, Duran S, Ince C. Improved survival beyond 28 days up to 1 year after CytoSorb treatment for refractory septic shock: a propensity weighted retrospective survival analysis. Blood Purif. 2021;50(4–5):539–45. https:// doi. org/ 10. 1159/ 00051 2309.
11. Woitsch S. Verbesserung der intrakraniellen Sauerstoffversorgung wahrend Operationen im tiefen hypothermen Kreislaufstillstand mit Hamoadsorption. 2018;(Der Hauptstadtkongress der DGAI fur Anasthesiologie und Intensivtherapie mit Pfl egesymposium und Rettungsdienstforum).
12. Schadler D, Porzelius C, Jorres A, et al. A multicenter randomized controlled study of an extracorporeal cytokine hemoadsorption device in septic patients. Crit Care. 2013;17(S2):P62. https:// doi. org/ 10. 1186/ cc120 00.
13. Schittek G. Beeinflussung des intensivstationaren Therapieverlaufs durch die Einfuhrung der Absorptionstherapie bei Patienten mit septischen Schock und akuten Nierenversagen. Published online 2018.
14. Born, F. Systemic Inflammatory Response Syndrome in der Herzchirurgie_Kardiotechnik 02–2014 - English Translation.pdf. Published online February 2014. http:// armag hansa lamat. com/ media/ brands/ Cytos orben ts/ Liter ature/ 2014_ Born% 20F% 20et% 20al. ,% 20Sys temic% 20Inflamma tory% 20Res ponse% 20Syn drome% 20in% 20der% 20Her zchir urgie_ Kardi otech nik% 2002- 2014% 20-% 20Eng lish% 20Tra nslat ion. pdf
15. Gliga S, Orth HM, Lubke N, Timm J, Luedde T, Jensen BEO. Multicentric Castleman’s disease in HIV patients: a single-center cohort diagnosed from 2008 to 2018. Infection. 2021;49(5):945–51. https:// doi. org/ 10. 1007/s15010- 021- 01618-5.
16. Mehta Y, Singh A, Singh A, Gupta A, Bhan A. Modulating the inflammatory response with hemadsorption (CytoSorb) in patients undergoing major aortic surgery. J Cardiothorac Vasc Anesth. 2021;35(2):673–5. https:// doi. org/ 10. 1053/j. jvca. 2020. 06. 028.
17. Lebreton G, Dorgham K, Quentric P, Combes A, Gorochov G, Schmidt M. Longitudinal cytokine profiling in patients with severe COVID-19 on extracorporeal membrane oxygenation and hemoadsorption. Am J Respir Crit Care Med. 2021;203(11):1433–5. https:// doi. org/ 10. 1164/ rccm.202011- 4140LE.
18. Lewis TC, Merchan C, Toy B, et al. Impact of CytoSorb hemoadsorption on sedation requirements in patients with severe COVID-19 on venovenous extracorporeal membrane oxygenation. ASAIO J. 2021;67(8):856–61. https:// doi. org/ 10. 1097/ MAT. 00000 00000 001513.
19. Garau I, Marz A, Sehner S, et al. Hemadsorption during cardiopulmonary bypass reduces interleukin 8 and tumor necrosis factor α serum levels in cardiac surgery: a randomized controlled trial. Minerva Anestesiol. 2019.https:// doi. org/ 10. 23736/ S0375- 9393. 18. 12898-7.
20. Bok S. CytoSorb: what is the effect on the circulation? in ESICM LIVES 2017: 30th ESICM Annual Congress September 23–27, 2017. Intensive Care Med Exp. 2017;5(S2):44. https:// doi. org/ 10. 1186/ s40635- 017- 0151-4.
21. Laubach CM. Cytokine and DAMP adsorption in septic acute kidney injury in ESICM LIVES 2018: Paris, France. 20-24 October 2018. Intensive Care Med Exp. 2018;6(S2):40. https:// doi. org/ 10. 1186/ s40635- 018- 0201-6.
22. Bottari G, Lorenzetti G, Severini F, Cappoli A, Cecchetti C, Guzzo I. Role of hemoperfusion with CytoSorb associated with continuous kidney replacement therapy on renal outcome in critically III children with septic shock. Front Pediatr. 2021;9:718049. https:// doi. org/ 10. 3389/ fped. 2021.718049.
23. Berlot G, Pintacuda S, Moro E, et al. Effects of tocilizumab versus hemoadsorption
combined with tocilizumab in patients with SARS-CoV-2 pneumonia: preliminary results. Int J Artif Organs. 2022;45(1):75–80. https:// doi. org/ 10. 1177/ 03913 98821 989334.
24. Bottari G, Murciano M, Merli P, et al. Hemoperfusion with CytoSorb to manage multiorgan dysfunction in the spectrum of hemophagocytic lymphohistiocytosis syndrome in critically Ill children. Blood Purif. 2022;51(5):417–24. https:// doi. org/ 10. 1159/ 00051 7471.
25. Schittek GA, Zoidl P, Eichinger M, et al. Adsorption therapy in critically ill with septic shock and acute kidney injury: a retrospective and prospective cohort study. Ann Intensive Care. 2020;10(1):154. https:// doi. org/ 10.1186/ s13613- 020- 00772-7.
26. Akil A, Ziegeler S, Reichelt J, et al. Combined use of CytoSorb and ECMO in patients with severe pneumogenic sepsis. Thorac Cardiovasc Surg. 2021;69(03):246–51. https:// doi. org/ 10. 1055/s- 0040- 17084 79.
27. Wendel Garcia PD, Hilty MP, Held U, Kleinert EM, Maggiorini M. Cytokine adsorption in severe, refractory septic shock. Intensive Care Med. 2021;47(11):1334–6. https:// doi. org/ 10. 1007/ s00134- 021- 06512-0.
28. Hawchar F, Laszlo I, Oveges N, Trasy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: a proof of concept randomized, controlled pilot study. J Crit Care. 2019;49:172–8. https:// doi. org/ 10. 1016/j.jcrc. 2018. 11. 003.
29. Kogelmann K, Hubner T, Schwameis F, Druner M, Scheller M, Jarczak D.First evaluation of a new dynamic scoring system intended to support prescription of adjuvant CytoSorb hemoadsorption therapy in patients with septic shock. J Clin Med. 2021;10(13):2939. https:// doi. org/ 10. 3390/jcm10 132939.
30. Rugg C, Klose R, Hornung R, et al. Hemoadsorption with CytoSorb in septic shock reduces catecholamine requirements and in-hospital mortality: a single-center retrospective ‘Genetic’ matched analysis. Biomedicines.2020;8(12):539. https:// doi. org/ 10. 3390/ biome dicin es812 0539.
31. Brouwer WP, Duran S, Kuijper M, Ince C. Hemoadsorption with CytoSorb shows a decreased observed versus expected 28-day all-cause mortality in ICU patients with septic shock: a propensity-score-weighted retrospective study. Crit Care. 2019;23(1):317. https:// doi. org/ 10. 1186/s13054- 019- 2588-1.
32. Schadler D, Pausch C, Heise D, et al. The effect of a novel extracorporeal cytokine hemoadsorption device on IL-6 elimination in septic patients: A randomized controlled trial. Eller K, ed. PLOS ONE. 2017;12(10):e0187015.https:// doi. org/ 10. 1371/ journ al. pone. 01870 15
33. Poli EC, Alberio L, Bauer-Doerries A, et al. Cytokine clearance with CytoSorb® during cardiac surgery: a pilot randomized controlled trial. Crit Care. 2019;23(1):108. https:// doi. org/ 10. 1186/ s13054- 019- 2399-4.
34. Hassan K, Kannmacher J, Wohlmuth P, Budde U, Schmoeckel M, Geidel S. Cytosorb adsorption during emergency cardiac operations in patients at high risk of bleeding. Ann Thorac Surg. 2019;108(1):45–51. https:// doi.org/ 10. 1016/j. athor acsur. 2018. 12. 032.
35. Bernardi MH, Rinoesl H, Dragosits K, et al. Effect of hemoadsorption during cardiopulmonary bypass surgery—a blinded, randomized, controlled pilot study using a novel adsorbent. Crit Care. 2016;20(1):96. https:// doi. org/ 10. 1186/ s13054- 016- 1270-0.
36. Taleska Stupica G, Sostaric M, Bozhinovska M, et al. Extracorporeal hemadsorption versus glucocorticoids during cardiopulmonary bypass: a prospective, randomized. Controlled Trial Cardiovasc Ther. 2020;2020:1–15. https:// doi. org/ 10. 1155/ 2020/ 78341 73.
37. Saller T, Hagl C, Woitsch S, et al. Haemadsorption improves intraoperative haemodynamics and metabolic changes during aortic surgery with hypothermic circulatory arrest. Eur J Cardiothorac Surg. 2019;56(4):731–7. https:// doi. org/ 10. 1093/ ejcts/ ezz074.
38. Santer D, Miazza J, Koechlin L, et al. Hemoadsorption during cardiopulmonary bypass in patients with endocarditis undergoing valve surgery: a retrospective single-center study. J Clin Med. 2021;10(4):564. https:// doi.org/ 10. 3390/ jcm10 040564.
39. Hassan K, Bruning T, Caspary M, et al. Hemoadsorption of rivaroxaban and ticagrelor during acute type A aortic dissection operations. Ann Thorac Cardiovasc Surg. 2022. https:// doi. org/ 10. 5761/ atcs. oa. 21- 00154.
40. Gleason TG, Argenziano M, Bavaria JE, et al. Hemoadsorption to reduce plasma-free hemoglobin during cardiac surgery: results of REFRESH I pilot study. Semin Thorac Cardiovasc Surg. 2019;31(4):783–93. https:// doi. org/10. 1053/j. semtc vs. 2019. 05. 006.
41. Trager K, Skrabal C, Fischer G, et al. Hemoadsorption treatment of patients with acute infective endocarditis during surgery with cardiopulmonary bypass—a case series. Int J Artif Organs. 2017;40(5):240–9. https:// doi. org/ 10. 5301/ ijao. 50005 83.
42. Nemeth E, Kovacs E, Racz K, et al. Impact of intraoperative cytokine adsorption on outcome of patients undergoing orthotopic heart transplantation-an observational study. Clin Transplant. 2018;32(4):e13211. https:// doi. org/ 10. 1111/ ctr. 13211.
43. Zhigalov K, Van den Eynde J, Zubarevich A, et al. Initial experience with CytoSorb therapy in patients receiving left ventricular assist devices. Artif Organs. 2022;46(1):95–105. https:// doi. org/ 10. 1111/ aor. 14099.
44. Haidari Z, Wendt D, Thielmann M, et al. Intraoperative hemoadsorption in patients with native mitral valve infective endocarditis. Ann Thorac Surg. 2020;110(3):890–6. https:// doi. org/ 10. 1016/j. athor acsur. 2019. 12. 067.
45. Wagner R, Soucek P, Ondrasek J, et al. Plasma levels of myocardial Micro-RNA-133a increase by intraoperative cytokine hemoadsorption in the complex cardiovascular operation. J Clin Med Res. 2019;11(12):789–97. https:// doi. org/ 10. 14740/ jocmr 3989.
46. Asch S, Kaufmann TP, Walter M, et al. The effect of perioperative hemadsorption in patients operated for acute infective endocarditis—a randomized controlled study. Artif Organs. 2021;45(11):1328–37. https://doi. org/ 10. 1111/ aor. 14019.
47. Diab M, Lehmann T, Bothe W, et al. Cytokine hemoadsorption during cardiac surgery versus standard surgical care for infective endocarditis (REMOVE): results from a multicenter randomized controlled trial. Circulation.2022;145(13):959–68. https:// doi. org/ 10. 1161/ CIRCU LATIO NAHA.121. 056940.
48. Schroeder I, Scharf C, Zoller M, et al. Charakteristika und Outcome von 70 beatmeten COVID-19-Patienten: Bilanz nach der ersten Welle an einem universitaren Zentrum. Anaesthesist. 2021;70(7):573–81. https:// doi. org/10. 1007/ s00101- 020- 00906-3.
49. Supady A, Weber E, Rieder M, et al. Cytokine adsorption in patients with severe COVID-19 pneumonia requiring extracorporeal membrane oxygenation (CYCOV): a single centre, open-label, randomised, controlled trial. Lancet Respir Med. 2021;9(7):755–62. https:// doi. org/ 10. 1016/ S2213-2600(21) 00177-6.
50. Stockmann H, Thelen P, Stroben F, et al. CytoSorb rescue for COVID-19 patients with vasoplegic shock and multiple organ failure: a prospective, open-label, randomized controlled pilot study. Crit Care Med. 2022.https:// doi. org/ 10. 1097/ CCM. 00000 00000 005493.
51. Rampino T, Gregorini M, Perotti L, et al. Hemoperfusion with CytoSorb as adjuvant therapy in critically Ill patients with SARS-CoV2 pneumonia. Blood Purif. 2021;50(4–5):566–71. https:// doi. org/ 10. 1159/ 00051 1725.
52. Supady A, Zahn T, Kuhl M, et al. Cytokine adsorption in patients with post-cardiac arrest syndrome after extracorporeal cardiopulmonary resuscitation (CYTER)—a single-centre, open-label, randomised, controlled trial. Resuscitation. 2022. https:// doi. org/ 10. 1016/j. resus citat ion.2022. 02. 001.
53. Akin M, Garcheva V, Sieweke JT, et al. Early use of hemoadsorption in patients after out-of hospital cardiac arrest—a matched pair analysis. Ballotta A, ed. PLOS ONE. 2020;15(11):e0241709. https:// doi. org/ 10. 1371/journ al. pone. 02417 09
54. Supady A, Zahn T, Rieder M, et al. Effect of cytokine adsorption on survival and circulatory stabilization in patients receiving extracorporeal cardiopulmonary resuscitation. ASAIO J. 2021. https:// doi. org/ 10. 1097/MAT. 00000 00000 001441.
55. Scharf C, Schroeder I, Paal M, et al. Can the cytokine adsorber CytoSorb® help to mitigate cytokine storm and reduce mortality in critically ill patients? A propensity score matching analysis. Ann Intensive Care. 2021;11(1):115. https:// doi. org/ 10. 1186/ s13613- 021- 00905-6.
56. Rieder M, Duerschmied D, Zahn T, et al. Cytokine adsorption in severe acute respiratory failure requiring veno-venous extracorporeal membrane oxygenation. ASAIO J. 2021;67(3):332–8. https:// doi. org/ 10. 1097/MAT. 00000 00000 001302.
57. Rasch S, Sancak S, Erber J, et al. Influence of extracorporeal cytokine adsorption on hemodynamics in severe acute pancreatitis: results of the matched cohort pancreatitis cytosorbents inflammatory cytokine removal (PACIFIC) study. Artif Organs. 2022. https:// doi. org/ 10. 1111/ aor.14195.
58. Wilhelmi M. Pilotstudie zur Outcome-Analyse bei Einsatz einer Cytokin-Hamoadsorption bei schwerstverletzten Polytraumapatienten. Published online 2018. https:// cytos orb- thera py. com/ wp- conte nt/ uploa ds/ 2018/12/ 2018_ Wilhe lmi_ Polyt rauma_ DIVI_ Poste r1. pdf
59. Barzilay E, Kessler D, Berlot G, Gullo A, Geber D, Ben ZI. Use of extracorporeal supportive techniques as additional treatment for septic-induced multiple organ failure patients. Crit Care Med. 1989;17(7):634–7. https://doi. org/ 10. 1097/ 00003 246- 19890 7000- 00007.
60. Fajgenbaum DC, June CH. Cytokine storm. N Engl J Med. 2020;383(23):2255–73. https:// doi. org/ 10. 1056/ NEJMr a2026 131.
61. Deans KJ, Haley M, Natanson C, Eichacker PQ, Minneci PC. Novel therapies for sepsis: a review. J Trauma. 2005;58(4):867–74. https:// doi. org/ 10.1097/ 01. ta. 00001 58244. 69179. 94.
62. Rimmele T, Kellum JA. Clinical review: blood purification for sepsis. Crit Care Lond Engl. 2011;15(1):205. https:// doi. org/ 10. 1186/ cc9411.
63. Ricci Z, Romagnoli S, Reis T, Bellomo R, Ronco C. Hemoperfusion in the intensive care unit. Intensive Care Med. 2022;48(10):1397–408. https:// doi.org/ 10. 1007/ s00134- 022- 06810-1.
64. Kielstein JT, Zarbock A. Is this the beginning of the end of cytokine adsorption? Crit Care Med. 2022;50(6):1026–9. https:// doi. org/ 10. 1097/CCM. 00000 00000 005509.
65. Kellum JA, Song M, Venkataraman R. Hemoadsorption removes tumor necrosis factor, interleukin-6, and interleukin-10, reduces nuclear factor-kappaB DNA binding, and improves short-term survival in lethal endotoxemia. Crit Care Med. 2004;32(3):801–5. https:// doi. org/ 10. 1097/ 01. ccm.00001 14997. 39857. 69.
66. Harm S, Schildbock C, Hartmann J. Cytokine removal in extracorporeal blood purification: an in vitro study. Blood Purif. 2020;49(1–2):33–43. https:// doi. org/ 10. 1159/ 00050 2680.
67. Honore PM, Matson JR. Extracorporeal removal for sepsis: acting at the tissue level–the beginning of a new era for this treatment modality in septic shock. Crit Care Med. 2004;32(3):896–7. https:// doi. org/ 10. 1097/ 01.
ccm. 00001 15262. 31804. 46.
68. Harm S, Falkenhagen D, Hartmann J. Pore size–a key property for selective toxin removal in blood purification. Int J Artif Organs. 2014;37(9):668–78. https:// doi. org/ 10. 5301/ ijao. 50003 54.
69. Konig C, Rohr AC, Frey OR, et al. In vitro removal of anti-infective agents by a novel cytokine adsorbent system. Int J Artif Organs. 2019;42(2):57–64. https:// doi. org/ 10. 1177/ 03913 98818 812601.
[DETAIL_PICTURE] =>
[DATE_ACTIVE_FROM] => 20.12.2023
[ACTIVE_FROM] => 20.12.2023
[SHOW_COUNTER] => 1061
)
[PROPERTIES] => Array
(
[KEYWORDS] => Array
(
[ID] => 1
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 100
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 102
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 829256
[VALUE] => CytoSorb®, систематический обзор и мета-анализ
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => CytoSorb®, систематический обзор и мета-анализ
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[DESCRIPTION] => Array
(
[ID] => 64
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Описание
[ACTIVE] => Y
[SORT] => 200
[CODE] => DESCRIPTION
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 829258
[VALUE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[~DESCRIPTION] =>
[~NAME] => Описание
[~DEFAULT_VALUE] =>
)
[BROWSER_TITLE] => Array
(
[ID] => 9
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Заголовок окна браузера
[ACTIVE] => Y
[SORT] => 300
[CODE] => BROWSER_TITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => content-articles-property-browser_title
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => Y
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 829257
[VALUE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[~DESCRIPTION] =>
[~NAME] => Заголовок окна браузера
[~DEFAULT_VALUE] =>
)
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 830414
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
)
[vote_count] => Array
(
[ID] => 100
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Количество проголосовавших
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_count
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество проголосовавших
[~DEFAULT_VALUE] =>
)
[vote_sum] => Array
(
[ID] => 101
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Сумма оценок
[ACTIVE] => Y
[SORT] => 500
[CODE] => vote_sum
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Сумма оценок
[~DEFAULT_VALUE] =>
)
[rating] => Array
(
[ID] => 102
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Рейтинг
[ACTIVE] => Y
[SORT] => 500
[CODE] => rating
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Рейтинг
[~DEFAULT_VALUE] =>
)
[FAVORITES] => Array
(
[ID] => 148
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Избранное
[ACTIVE] => Y
[SORT] => 500
[CODE] => FAVORITES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Избранное
[~DEFAULT_VALUE] =>
)
[LIKE] => Array
(
[ID] => 153
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Понравилось
[ACTIVE] => Y
[SORT] => 500
[CODE] => LIKE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Понравилось
[~DEFAULT_VALUE] =>
)
[SUBTITLE] => Array
(
[ID] => 93
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Подзаголовок
[ACTIVE] => Y
[SORT] => 501
[CODE] => SUBTITLE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Подзаголовок
[~DEFAULT_VALUE] =>
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 829262
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
)
[QUOTE] => Array
(
[ID] => 95
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Цитата
[ACTIVE] => Y
[SORT] => 503
[CODE] => QUOTE
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Цитата
[~DEFAULT_VALUE] =>
)
[SLIDER] => Array
(
[ID] => 98
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Слайдер
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] => jpg, gif, bmp, png, jpeg
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер
[~DEFAULT_VALUE] =>
)
[SLIDER_DESC] => Array
(
[ID] => 99
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Слайдер описание
[ACTIVE] => Y
[SORT] => 503
[CODE] => SLIDER_DESC
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Слайдер описание
[~DEFAULT_VALUE] =>
)
[INFO_SOURCES] => Array
(
[ID] => 96
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Информация и источники
[ACTIVE] => Y
[SORT] => 504
[CODE] => INFO_SOURCES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Информация и источники
[~DEFAULT_VALUE] =>
)
[MATERIALS] => Array
(
[ID] => 97
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Материалы к статье
[ACTIVE] => Y
[SORT] => 505
[CODE] => MATERIALS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => Y
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Материалы к статье
[~DEFAULT_VALUE] =>
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 829260
[1] => 829261
)
[VALUE] => Array
(
[0] => statia
[1] => Issledovanie
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => statia
[1] => Issledovanie
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
)
[COMMENTS_COUNT] => Array
(
[ID] => 103
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Количество комментариев
[ACTIVE] => Y
[SORT] => 5010
[CODE] => COMMENTS_COUNT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Количество комментариев
[~DEFAULT_VALUE] =>
)
[FB2] => Array
(
[ID] => 173
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => FB2
[ACTIVE] => Y
[SORT] => 5020
[CODE] => FB2
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] => fb2
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => FB2
[~DEFAULT_VALUE] =>
)
[ADD_DATES] => Array
(
[ID] => 207
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Дата добавления материалов
[ACTIVE] => Y
[SORT] => 5030
[CODE] => ADD_DATES
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => Date
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата добавления материалов
[~DEFAULT_VALUE] =>
)
[LENGHT] =>
[VIDEO_PREVIEW] =>
[VIDEO_FULL] =>
)
[DISPLAY_PROPERTIES] => Array
(
[MAIN] => Array
(
[ID] => 65
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Показывать на главной странице
[ACTIVE] => Y
[SORT] => 500
[CODE] => MAIN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => L
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => C
[MULTIPLE] => N
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] => a:0:{}
[HINT] =>
[PROPERTY_VALUE_ID] => 830414
[VALUE] => да
[DESCRIPTION] =>
[VALUE_ENUM] => да
[VALUE_XML_ID] => Y
[VALUE_SORT] => 500
[VALUE_ENUM_ID] => 1
[~VALUE] => да
[~DESCRIPTION] =>
[~NAME] => Показывать на главной странице
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => да
)
[AUTHOR] => Array
(
[ID] => 94
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Автор
[ACTIVE] => Y
[SORT] => 502
[CODE] => AUTHOR
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => N
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 1
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => UserID
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 829262
)
[VALUE] => Array
(
[0] => 8
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 8
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Автор
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => [8] (info@sepsisforum.ru) Команда Сепсис Форума
)
[SUBJECTS] => Array
(
[ID] => 66
[TIMESTAMP_X] => 2025-08-13 01:26:24
[IBLOCK_ID] => 2
[NAME] => Тематика
[ACTIVE] => Y
[SORT] => 1000
[CODE] => SUBJECTS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] =>
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => directory
[USER_TYPE_SETTINGS] => Array
(
[size] => 1
[width] => 0
[group] => N
[multiple] => N
[TABLE_NAME] => b_hlbd_subjects
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 829260
[1] => 829261
)
[VALUE] => Array
(
[0] => statia
[1] => Issledovanie
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => statia
[1] => Issledovanie
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
)
[~NAME] => Тематика
[~DEFAULT_VALUE] =>
[DISPLAY_VALUE] => Array
(
[0] => Статья
[1] => Исследование
)
)
)
[IBLOCK] => Array
(
[ID] => 2
[~ID] => 2
[TIMESTAMP_X] => 13.08.2025 01:26:24
[~TIMESTAMP_X] => 13.08.2025 01:26:24
[IBLOCK_TYPE_ID] => articles
[~IBLOCK_TYPE_ID] => articles
[LID] => s1
[~LID] => s1
[CODE] => articles
[~CODE] => articles
[API_CODE] =>
[~API_CODE] =>
[NAME] => Статьи
[~NAME] => Статьи
[ACTIVE] => Y
[~ACTIVE] => Y
[SORT] => 200
[~SORT] => 200
[LIST_PAGE_URL] => /library/articles/
[~LIST_PAGE_URL] => /library/articles/
[DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[~DETAIL_PAGE_URL] => /library/articles/#ELEMENT_CODE#/
[SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[~SECTION_PAGE_URL] => /articles/#SECTION_CODE#/
[CANONICAL_PAGE_URL] =>
[~CANONICAL_PAGE_URL] =>
[PICTURE] =>
[~PICTURE] =>
[DESCRIPTION] => Статьи
[~DESCRIPTION] => Статьи
[DESCRIPTION_TYPE] => html
[~DESCRIPTION_TYPE] => html
[RSS_TTL] => 24
[~RSS_TTL] => 24
[RSS_ACTIVE] => Y
[~RSS_ACTIVE] => Y
[RSS_FILE_ACTIVE] => N
[~RSS_FILE_ACTIVE] => N
[RSS_FILE_LIMIT] =>
[~RSS_FILE_LIMIT] =>
[RSS_FILE_DAYS] =>
[~RSS_FILE_DAYS] =>
[RSS_YANDEX_ACTIVE] => N
[~RSS_YANDEX_ACTIVE] => N
[XML_ID] => content-articles
[~XML_ID] => content-articles
[TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[~TMP_ID] => 79a4a50658ff380feeea3c1c690acaa8
[INDEX_ELEMENT] => Y
[~INDEX_ELEMENT] => Y
[INDEX_SECTION] => Y
[~INDEX_SECTION] => Y
[WORKFLOW] => N
[~WORKFLOW] => N
[BIZPROC] => N
[~BIZPROC] => N
[SECTION_CHOOSER] => L
[~SECTION_CHOOSER] => L
[LIST_MODE] =>
[~LIST_MODE] =>
[RIGHTS_MODE] => S
[~RIGHTS_MODE] => S
[SECTION_PROPERTY] => Y
[~SECTION_PROPERTY] => Y
[PROPERTY_INDEX] => I
[~PROPERTY_INDEX] => I
[VERSION] => 1
[~VERSION] => 1
[LAST_CONV_ELEMENT] => 0
[~LAST_CONV_ELEMENT] => 0
[SOCNET_GROUP_ID] =>
[~SOCNET_GROUP_ID] =>
[EDIT_FILE_BEFORE] =>
[~EDIT_FILE_BEFORE] =>
[EDIT_FILE_AFTER] =>
[~EDIT_FILE_AFTER] =>
[SECTIONS_NAME] => Разделы статей
[~SECTIONS_NAME] => Разделы статей
[SECTION_NAME] => Раздел статей
[~SECTION_NAME] => Раздел статей
[ELEMENTS_NAME] => Статьи
[~ELEMENTS_NAME] => Статьи
[ELEMENT_NAME] => Статья
[~ELEMENT_NAME] => Статья
[REST_ON] => N
[~REST_ON] => N
[FULLTEXT_INDEX] => N
[~FULLTEXT_INDEX] => N
[EXTERNAL_ID] => content-articles
[~EXTERNAL_ID] => content-articles
[LANG_DIR] => /
[~LANG_DIR] => /
[SERVER_NAME] => sepsisforum.ru
[~SERVER_NAME] => sepsisforum.ru
)
[SECTION] => Array
(
[PATH] => Array
(
)
)
[SECTION_URL] =>
[META_TAGS] => Array
(
[TITLE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[BROWSER_TITLE] => Эффективность CytoSorb®: систематический обзор и мета-анализ
[KEYWORDS] => CytoSorb®, систематический обзор и мета-анализ
[DESCRIPTION] => Эффективность CytoSorb®: систематический обзор и мета-анализ
)
)







