Диагностика бактериального сепсиса: почему тестов на бактеремию недостаточно?
EXPERT REVIEW OF MOLECULAR DIAGNOSTICS
Статья главного редактора
Перевод оригинальной статьи
Diagnosis of bacterial sepsis: why are tests for bacteremia not sufficient?
Diagnosis of bacterial sepsis: why are tests for bacteremia not sufficient?
Авторы: Timothy E Sweeney, Oliver Liesenfeld and Larissa May
Inflammatix, Inc, Burlingame, CA, USA;
Department of Emergency Medicine, Davis School of Medicine, University of California Davis Health, Sacramento, CA, USA
Цитировать, как: Timothy E Sweeney, Oliver Liesenfeld & Larissa May (2019): Diagnosis of bacterial sepsis: why are tests for bacteremia not sufficient?, Expert Review of Molecular Diagnostics, DOI: 10.1080/14737159.2019.1660644
Keywords: Antibiotics; bacteremia; culture; blood culture; diagnostic; host response; sepsis
1. Введение
Сепсис остается основной причиной заболеваемости и смертности пациентов, а также и высокой финансовой нагрузки на систему здравоохранения, что особенно видно на примере систем здравоохранения в Соединенных Штатах, где в настоящее время выплаты частично привязаны к критериям эффективности терапии сепсиса. Ранее термин «сепсис» часто использовался как синоним термина «бактериемия», но совсем недавно принято новое определение сепсиса «‘Sepsis3», где сепсис определяется, как «жизне-угрожающее нарушение иммунного ответа на инфекцию» [1]. Сепсис, как синдром, может быть вызван бактериальными, вирусными, грибковыми или паразитарными инфекциями, а его клинические проявления схожи с состояниями, этиология которых лежит вне инфекционного поражения, что делает диагностику сепсиса особенно сложной в тех случаях, когда источник инфекции не сразу очевиден. Помимо этого, было показано, что в случаях бактериальной инфекции раннее лечение соответствующими антимикробными препаратами снижает заболеваемость и смертность. С другой стороны, антибиотики могут иметь существенные побочные эффекты. К примеру, у 1 из 5 пациентов госпиталя, которым парентерально вводятся антибиотики, отмечается неблагоприятное лекарственное событие, включая сюда инфекцию C. difficile [2], а неизбирательное и длительное применение антибиотиков ведет к росту резистентности микрофлоры к противомикробным препаратам [3]. Таким образом, быстрая диагностика сепсиса и его основной причины представляет собой большой интерес: как писал Kibe, «поиск биомаркера сепсиса, обладающего высокой диагностической точностью, стал одним из святых Граалей медицины» [4].
2. Основные вопросы
2.1 Диагностика сепсиса в настоящее время
Особенности диагностики сепсиса заключаются в том, что данные физикального обследования и показатели жизненно важных функций, а также лабораторные, рентгенологические и микробиологические данные, в значительной степени неспецифичны [5,6,7]. Несмотря на то, что многие диагностические тесты на сепсис in vitro потенциально информативны, не все они являются клинически эффективными. И для того, чтобы понять, почему, необходимо понимать современный алгоритм диагностики и лечения сепсиса. И клинические рекомендации руководства the Surviving Sepsis Campaign, и алгоритм лечения и диагностики сепсиса 1-ого часа CMS (the Center for Medicare & Medicaid Services) «SEP-1», можно почти полностью свести до двух основных путей лечения: (а) контроль источника инфекции и антимикробная терапия для борьбы с основной инфекцией и (б) терапия, направленная на поддержание физиологии [8]. Также и компоненты диагностики можно разделить на две отдельные, но взаимодополняющие части, а именно: (а) есть ли инфекция и (б) насколько тяжелым является состояние пациента [9,10]. Почти вся диагностика сепсиса in vitro, помимо лактата, нацелена, в первую очередь ,на оценку того, следует ли добиваться контроля источника и как правильно это сделать и, собственно, надлежащего назначения антимикробных препаратов.
Текущие клинические рекомендации в основном направлены на начало лечения в течение 60 минут после постановки диагноза сепсиса. Многочисленные ретроспективные исследования показали, что у пациентов с тяжелыми формами сепсиса, которым назначают антибиотики согласно текущей рекомендации, клинические результаты лучше, чем у пациентов с отсроченным лечением [11–14]. Примером этому могут служить отделения неотложной помощи (emergency department или ED), на долю которых приходится почти 500 000 случаев сепсиса в год, что составляет примерно две трети от всех пациентов с сепсисом, поступающих в больницу через ED [15].
2.2 Посевы крови - несовершенный золотой стандарт, так как сепсис не равен бактериемии
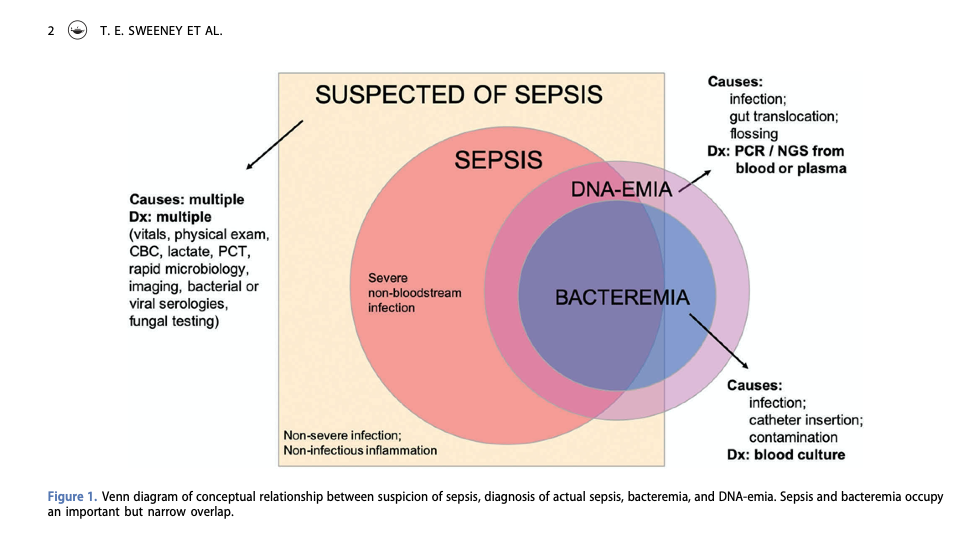
Для установления диагноза острой инфекции может применяться множество разнообразных тестов, но диагностическим тестом, который чаще всего ассоциируется с бактериальным сепсисом, остается микробиологический посев крови. Бактериальные инфекции кровотока распространены при сепсисе, но бактериемия отличается от сепсиса (рис. 1). Фактически, только у 38–69% пациентов с сепсисом определяются бактериальные инфекции кровотока [7]. У большинства пациентов острые бактериальные инфекции относятся к локальным инфекциям, что не проникают в системный кровоток [7], и ярким примером тому может служить пневмония. И метод полимеразной цепной реакции (ПЦР), и технологии секвенирования следующего поколения могут определить наличие патогенов в крови, но обычно эти методы дают отрицательные результаты у пациентов, у которых, по мнению врачей, имеется инфекция, но могут показывать положительные результаты ДНК патогенов в крови у пациентов, у которых инфекции нет [16,17]. Иными словами, даже лучшие технологии не могут найти иголку в стоге сена, когда ее там нет. Кроме того, получение результатов патоген-ориентированными методами может занять часы или даже дни. Таким образом, для первоначального принятия клинических решений у пациентов с сепсисом эти методы имеют ограниченную полезность.
Мы также знаем то, что многие пациенты с клиническими признаками и симптомами сепсиса на самом деле не имеют основной инфекции [18]. Просто у них развивается воспалительный ответ на другие острые состояния (послеоперационная травма, тромбообразование, аутоиммунные состояния и т. д.). Точные цифры сильно зависят от клинических обстоятельств. К примеру, пациенты после хирургических вмешательств показывают гораздо более высокий уровень неинфекционного воспаления, чем пациенты среднего возраста [19]. В одном одно-центровом исследовании междисциплинарных отделений интенсивной терапии (ОИТ) из четырех-пяти пациентов, отвечающих критериям системного воспалительного ответа (ССВО), инфекция (сепсис) обнаруживается только у одного [20]. Получается так, что клиницисты не могут просто лечить всех, кто «плохо выглядит», антибиотиками. Но не только ненадлежащее применение антибиотиков нанесет прямой вред пациенту, но и отсутствие лечения основного процесса, того, что привел к развитию ССВО у пациента без инфекции. К сожалению, доступные инструменты скрининга, такие как лактат и прокальцитонин, часто применяемыми в алгоритмах скрининга в ED, не обладают достаточной специфичностью (и даже чувствительностью) [21], что объясняется самой природой критического состояния, а это приводит к консервативным управленческим подходам.
2.3 Микробиологический посев крови нечувствителен, требует много времени и зависит от объема и времени взятия пробы крови
Популяция, подвергаемая скринингу на сепсис, часто может не иметь бактериальной инфекции, а у популяции, у которой может быть бактериальная инфекция, микробиологические посевы крови могут быть отрицательными. Чувствительность и специфичность микробиологического посева крови в общем целом низки отчасти потому, что результат зависит от объема крови и сроков взятия пробы крови, предшествующего лечения любыми антибиотиками и наличия в крови жизнеспособных микроорганизмов [22]. Можно сделать вывод о том, что отрицательный тест на бактериемию является (а) распространенным и (б) относительно неинформативным в отношении того, нуждается ли пациент в назначении антибактериальной терапии. Нельзя забывать и о ложно-положительных посевах в результате контаминации (например, Staphylococcus epidermidis), что так распространены и, отсюда, проблематичны даже при тщательном соблюдении протокола взятия пробы крови на микробиологический посев [23]. Вдобавок к этому, самые тяжелые пациенты, у которых наиболее часто определяется бактериемия (например, пациенты с септическим шоком), почти всегда уже получают антибиотики широкого спектра действия, что делает микробиологический посев крови плохим тестом на предмет назначения антибиотиков (хотя тест на чувствительность к антибиотикам, безусловно, помогает определить, какие именно антибиотики самые лучшие). Более того, задержки в получении результата из-за длительного анализа также часто приводят к неоправданно длительным курсам антибиотиков широкого спектра действия, назначенных эмпирически, без знания этиологического агента, подвергая тем самым пациентов ненужному риску развития побочных эффектов и приводя к развитию резистентности.
Технологические лидеры Roche's и Abbott выпустили быстрые платформы SeptiFast ™ IRIDICA ™ для обнаружения бактериемии, но эти устройства так и не принесли ожидаемой коммерческой выгоды и, в конечном итоге, были выведены с рынка. Мы предполагаем, что корень неудачи лежал в неправильных вопросах, что могли задаваться на ранних этапах разработки этих высокоточных, но неудачных систем. Спросите врача, захочет ли он или она узнать, есть ли у его пациента бактериемия, то почти все ответят «Да». Спросите далее, а будет ли в результате предпринято какое либо клиническое действие, то ответ будет зависит от множества нюансов.
В настоящее время разрабатывается новое поколение диагностических технологий для обнаружения бактериемии, что может сократить время обнаружения до нескольких часов (например, T2 Bacteremia Panel; Qvella Fast-ID, в разработке). При тщательном рассмотрении, внедрение и интеграция этих технологий в клинический процесс сможет не только сделать терапию бактериальной инфекции и сепсиса более эффективной, но и сыграет определяющую роль в контроле за назначением противомикробных препаратов как в ED, так и в больнице, сделать первоначальный выбор антибиотиков более адекватным и снизить опасения относительно развития устойчивости к противомикробным препаратам, но все это требует дальнейшего изучения [24]. Помимо обнаружения бактерий в пробах цельной крови, быстрые бактериальные панели ПЦР могут сократить время идентификации бактерий в посеве крови до одного дня и обеспечить генотипический или фенотипический тест на чувствительность к антибиотикам всего через несколько часов после получения положительных результатов посева крови. Несмотря на то, что это все еще слишком долго для первоначальной стратификации пациентов, но и при таком положении дел польза от новых технологий будет существенна и заключаться в сокращении длительности антибактериальной терапии у госпитализированных пациентов.
2.4 Начало антибиотикотерапии - часто игра в «угадайку»
Врач, после проведения осмотра пациента с симптомами острой инфекции или сепсиса, должен решить, следует ли назначать пациенту эмпирическую антимикробную терапию антибиотиками только лишь на основании клинической картины и результатов неспецифических тестов [5]. И несмотря на то, что антибиотики имеют значительные побочные эффекты и для пациента, и для общества (резистентность к противомикробным препаратам), не назначение антибиотиков пациенту с бактериальным сепсисом несет в себе существенные риски. Таким образом, лечение антибиотиками часто начинают в основном из-за страха пропустить сепсис [25].
В настоящий момент выбор антибиотика для начальной терапии часто основан не на микробиологических данных, а на предполагаемом месте инфекции и клинических рекомендациях. Большинство людей, не связанных с медициной, с удивлением узнают, что рекомендации по эмпирической антибактериальной терапии часто довольно ограничены в выборе; например, взрослого амбулаторного больного с подозрением на внебольничную пневмонию следует лечить либо (1) макролидом, либо доксициклином в случае, если он здоров и без факторов риска для резистентных организмов, (2) фторхинолоном или макролидом + бета-лактамом в случае наличия сопутствующих заболеваний [26]. Другими словами, первоначальный выбор, следует ли назначать антибиотики, намного сложнее, чем следующий шаг, какой антибиотик, или их комбинацию, следует назначать пациенту.
Конечно, эмпирическая антибактериальная терапия несет в себе риск ошибки в виде возможной устойчивости микроорганизма к выбранным антибиотикам или в том, что выбранный режим антибактериальной терапии не покрывает весь спектр микроорганизмов. Выбор между «не лечить», «лечить эмпирически», можно облегчить с помощью микробиологических данных, но только после того, как результаты микробиологических посевов станут доступны, но это возможно со значительной задержкой из-за ограничений у текущей диагностики, как обсуждалось выше. И это особенно неприятно при сепсисе, учитывая высокие показатели заболеваемости и смертности в случаях, когда выявление сепсиса не проводится своевременно. Таким образом, у пациентов с подозрением на сепсис первоначально часто используют антибиотик широкого спектра действия или комбинацию антибиотиков (например, ванкомицин и пиперациллин-тазобактам). В этом распространенном сценарии ценность микробиологического тестирования заключается в получении результата, указыающего на восприимчивость микроорганизма к антибиотикам и к последующему назначению узкоспециализированной терапии. Таким образом, мы полагаем, что диагностические инструменты, которые могут обеспечить идентификацию микробов с одновременным пониманием чувствительности этих микробов к антибиотикам быстрее, чем существующие методы культивирования, должны быть приняты в клиническую практику.
2.5 Исследование иммунного ответа, как альтернативного подхода к диагностике сепсиса
Ограничения в клинической применимости технологий обнаружения патогена в контексте эффективной антибактериальной терапии сепсиса привели к тому, что повышенный интерес приобрело исследование иммунного ответа на инфекцию. Это особенно правильно в педиатрии, где объем крови для получения анализа ограничен. Иммунная система может послужить потенциальным информатором, ставя нас в известность как о наличии инфекции, так и о ее типе (бактериальная, вирусная, грибковая). Более того, иммунная система может оценивать риск развития сепсиса и/или смерти [10]. Биомаркеры, основанные на реакции иммунной системы, могут быть измерены за считанные минуты. Таким образом иммунный ответ является потенциально лучшим способом диагностики и лечения сепсиса. Общепринятыми на сегодня биомаркерами являются: количество лейкоцитов, С-реактивный белок и прокальцитонин. Однако наиболее точный из них, прокальцитонин, может быть полезен в качестве маркера определения эффективности выбранной антибактериальной терапии [27], применение которого в таком качестве потенциально снижает общую смертность [28]. Тем не менее, точность его, без внедрения программы менеджмента, еще вызывает сомнения [10,29]. Совсем недавно возродился интерес к мультимаркерной диагностике иммунного ответа, в частности, к новым панелям иммунной митохондриальной РНК хозяина [30–33]. Объединение надежных биомаркеров с надежным машинным обучением показало высокую точность в определении наличия инфекции и ее типа в любом месте тела, а не только в кровотоке.
Таким образом, мы полагаем, что начало лечения пациентов с сепсисом будет основано на ультрабыстрых инструментах диагностики, которые смогут уже на этапе первичного клинического осмотра информировать клиницистов о «двух осях» сепсиса: первая - диагностика инфекции и вторая - оценка степени тяжести. Результаты, полученные с помощью таких диагностических тестов, позволят на самом раннем этапе определить, следует ли лечить пациента антибиотиками, какие необходимы последующие диагностические процедуры и какой уровень медицинской помощи необходим. Такие инструменты могут оказаться полезными не только в отделениях неотложной помощи, но и по всему спектру медицинских учреждений, от отделения интенсивной терапии до кабинетов врачей, клиник неотложной помощи и аптек. Это будет особенно полезно при включении в состав новых или существующих программ по борьбе с сепсисом и антимикробных программ управления, с возможностью более ранней адаптации оптимальной терапии, а также ускорения де-эскалации антибактериальной терапии. Все это может привести к улучшению результатов.
Будущие исследования должны показать, как диагностика на основе иммунного ответа может дополнить расширенную диагностику на основе патогенов. Слепые проспективные исследования являются ключом к установлению точности, но для того, чтобы полностью показать потенциальную клиническую ценность, необходимы рандомизированные интервенционные исследования [33,34]. Тем не менее, мы полагаем, что в больнице будущего, скорее всего, будет применен трехсторонний подход к диагностике сепсиса, в том числе (1) быстрый скрининг и диагностические тесты на основе иммунного ответа на начальном этапе оказания госпитальной пополощи, что может сообщить, следует ли лечить пациентов антибиотиками, какие необходимы последующие методы диагностики и на каком уровне лечения; (2) быстрые тесты на идентификацию бактерий и определения чувствительности их к антибиотикам, которые могут определить необходимую терапию у пациентов с положительными результатами тестов иммунного ответа, и (3) более длительные, основанные на результатах микробиологических посевов или на новых тестах секвенирования следующего поколения у пациентов с персистирующим заболеванием, несмотря на выполнение пунктов (1) и (2). У каждого из этих новых методов уже имеются обнадеживающие результаты и, вероятно, в конечном итоге внедрение их в клиническую практику приведет к решению имеющихся проблем, что в настоящее время затрудняют диагностику острых инфекций и сепсиса.

EXPERT REVIEW OF MOLECULAR DIAGNOSTICS